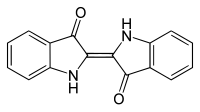
indigo
| Strukturel formel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Generel | |||||||||||||||||||
| Efternavn | indigo | ||||||||||||||||||
| andre navne |
|
||||||||||||||||||
| Molekylær formel | C 16 H 10 N 2 O 2 | ||||||||||||||||||
| Kort beskrivelse |
mørkeblå, lugtfri krystallinsk fast stof |
||||||||||||||||||
| Eksterne identifikatorer / databaser | |||||||||||||||||||
| |||||||||||||||||||
| ejendomme | |||||||||||||||||||
| Molar masse | 262,27 g mol −1 | ||||||||||||||||||
| Fysisk tilstand |
fast |
||||||||||||||||||
| Smeltepunkt |
390-392 ° C |
||||||||||||||||||
| opløselighed |
|
||||||||||||||||||
| Sikkerhedsinstruktioner | |||||||||||||||||||
| |||||||||||||||||||
| Så vidt muligt og sædvanligt anvendes SI-enheder . Medmindre andet er angivet, gælder de givne data for standardbetingelser . | |||||||||||||||||||
Indigo (fra det gamle græske ἰνδικόν indikón , tysk 'indianeren' ; efter oprindelsesregionen Østindien ) er en dybblå, krystallinsk organisk-kemisk forbindelse . Det er et organisk pigment med høj farvestyrke og lidt opløseligt i vand. Indigo er navnebror til gruppen af indigoidfarvestoffer , hvis kemiske struktur er tæt forbundet med indigos.
Farven med samme navn, indigo, er også opkaldt efter ham. Det kan bedst beskrives som den sidste genkendelige blå nuance, før den bliver til en blålig lilla . Indigo er opført i farveindekset som et pigment under navnet CI Pigment Blue 66 og som et farvestof under CI Vat Blue 1.
Indigo er et af de ældste og mest kendte pigmenter og blev brugt til at farve tekstiler allerede i forhistorisk tid. Tidligere blev indigo opnået fra vegetabilske kilder såsom blade af woad eller fra indigo-planten . Fra 1865 gennemførte Adolf von Baeyer en række undersøgelser, hvor han udviklede forskellige syntetiske ruter for indigo og bestemte dets kemiske struktur. For sit arbejde med farvestofkemi modtog han Nobelprisen i kemi i 1905 . Indigo spillede en vigtig rolle i den videre udvikling af organisk kemi , især forholdet mellem molekylets farve og struktur og dets derivater blev intensivt undersøgt og bidrog således til udviklingen af en generel teori om farvestoffer.
Med udviklingen af industrielle synteseprocesser mod slutningen af det 19. århundrede begyndte den store og dermed billige produktion af indigo, hvorefter markedet for naturlig indigo kollapsede. I dag produceres titusindvis af ton indigo syntetisk om året, der hovedsagelig bruges til at farve bomuldsstof i denim til fremstilling af blå jeans .
Hændelse
Indigo kan fås fra den indiske indigo-plante ( Indigofera tinctoria ) eller fra woad ( Isatis tinctoria ), som blev naturaliseret i Europa i antikken . Indigo-planten i Indien leverede tredive gange mængden af farvestof sammenlignet med woad, så dyrkning i Europa blev urentabel i det 17. århundrede. Amerikanske bosættere brugte bastardindigo ( Amorpha fruticosa ) som erstatning for indigo, og i Japan blev farvestofens knude ( Polygonum tinctorium , syn. Persicaria tinctoria ) brugt til farvning af blå. En række andre planter er velegnede til produktion af indigo, herunder den almindelige djævelens bid ( Succisa pratensis ), indigolupinen ( Baptisia australis ), farvestofens oleander ( Wrightia tinctoria ) eller ternwort ( Marsdenia tinctoria ). I Kina blev den kinesiske woad ( Isatis indigotica ) brugt. Indigo dyrkes stadig i Brasilien og El Salvador . Den farvestofrige art Indigofera arrecta og Indigofera sumatrana anvendes . Den UNESCO fremmer forskellige projekter til anlæg indigo bærende planter, herunder Jordandalen og Aralsøen .
historie
Indigo var og er et af de mest udbredte og hyppigst anvendte farvestoffer siden oldtiden . Før begyndelsen af syntetisk produktion blev den hentet fra forskellige planter, der indeholder indigo. Disse omtales ofte med den artsspecifikke epithet tinctoria , et latinsk ord for farvning.
I Europa blev woad, Isatis tinctoria , fra korsfamilien brugt til farvning af blå indtil det 17. århundrede . Det kommer oprindeligt fra Mellemøsten , men blev allerede dyrket som en farvestofplante i førkristen tid i Europa . I Asien og Sydamerika blev arter af slægten Indigofera brugt, såsom den tropiske indigo-plante Indigofera tinctoria , de europæiske bosættere i Nordamerika brugte hybridindigo , Amorpha fruticosa , til farvning af blå.
Farvning med indigo danner grundlaget for århundredgamle tekstiltraditioner i hele Vestafrika. Den indigofarvede Tagelmust , der bæres af Tuareg- nomaderne i Sahara, symboliserer rigdom og sundhed. På grund af den vandfattige farvningsproces der er indigo ikke meget slidbestandig og trænger igennem bærerens hud, hvorfor Tuareg er kendt som "de blå mænd i ørkenen". Den Yoruba , Mandinka og hausa også farve deres tøj med indigo.
Antikken til den sene middelalder
Spor af brugen af indigo kan spores tilbage til 6000 år gamle bomuldsstoffer fra den prækeramiske fabrik Huaca Prieta de Chicama på Perus nordkyst . Forskellige indigofera-arter, der er hjemmehørende i Sydamerika, blev sandsynligvis brugt som indigo-leverandører. I Egypten, mumier fra femte dynasti af gamle kongerige , omkring 4.400 år før den nuværende, blev fundet svøbt i indigo-farvet mumie bånd. Japan og sydøstasiatiske lande har brugt indigo som farvestof i århundreder. Farvestoffet var fortsat kendt i de tidlige kulturer i Mesopotamien , Iran og Afrika. Planter til produktion af indigo blev primært dyrket i Indien , det første vigtige center for dets produktion og forarbejdning. Indigo blev sendt til Egypten via Barbarikon på Indus . Derefter tog den vej til Grækenland og Italien, hvor den blev betragtet som et luksusprodukt.
Caesar rapporterede omkring 50 f.Kr. F.Kr. i De bello Gallico , at kelterne brugte woad før væbnede konflikter for at få deres hud til at blive blå. Den romerske lærde Plinius den ældre beskrev indigo omkring 77 e.Kr. i sit arbejde Naturalis historia . Ifølge Plinius havde indigo den højeste agtelse efter lilla i den antikke verden . Han angav Indien som oprindelsesland, som udtrykkes i det latinske ord indicum , hvorfra det nuværende navn indigo stammer. Et andet udtryk for farvestoffet er anil , der er afledt af det arabiske udtryk for blå, an-nul , og findes som en komponent af navne som anilin . I middelalderen var der intet andet farvestof end indigo kendt i Europa. I det 8. århundrede regulerede Karl den Store dyrkning af woad til indigoproduktion i hans landgodsforordning Capitulare de villis vel curtis imperii .
Farvestoffet fra indigo-planten var sjældent i Europa indtil det 12. århundrede; det blev kun importeret fra Indien i små mængder via Syrien og Alexandria . Indtil det 17. århundrede blev woad dyrket til indigoproduktion i England, Frankrig og Tyskland. I Tyskland var det største dyrkningsområde i Thüringen , hvor ca. 3750 hektar blev dyrket sammen med planten.
Tidlig moderne tidsalder
Med opdagelsen af søvejen til Indien af Vasco da Gama begyndte portugisiske søfarendes direkte import af indisk indigo (også kaldet "den lige indigo, der vokser i indiske rør") til Europa. De hollandske handelsselskaber grundlagde det hollandske østindiske selskab i 1602 og øgede efterfølgende importen af indigo fra Indien og Indonesien. Spanien begyndte at vokse i Guatemala og Venezuela på dette tidspunkt , Frankrig havde indigo vokset i San Domingo, og England begyndte at vokse i Carolina omkring 1700 . Da indigo-indholdet af woad kun var omkring 3-4% af indigofera-planten, fortrængte indigo til sidst den tropiske Indigofera tinctoria på trods af protektionistiske importbestemmelser.
Efter nederlaget i den amerikanske uafhængighedskrig i 1783 og det dermed forbundne tab af nordamerikanske dyrkningsområder øgede England indigodyrkning i Bengalen . Især tidligere ansatte i East India Company , såkaldte planter, begyndte at kommercialisere indigodyrkning i Bihar og Bengal. Ved falske kontrakter og for høje rentesatser for indkøb af frøene opnåede avlerne store overskud, mens landmændene havde ringe fortjeneste. Omstændighederne førte til Indigo-oprørene i 1859–1862 , den første bondebevægelse i Bengalen og Bihar mod de europæiske plantageres udbyttende metoder. Selvom uroen sluttede med afskaffelsen af obligatorisk dyrkning af indigo, fortsatte indigodyrkning i Indien at være en enorm gren af industrien, der overvejende var britisk ejet. Tunika nederdele, sømandsuniformer og arbejdernes blå arbejdstøj blev farvet med dette farvestof. I Bihar alene var omkring 1,5 millioner mennesker involveret i indigodyrkning. I 1897 var dyrkningsarealet i Indien omkring 7.000 kvadratkilometer, og på det tidspunkt blev der produceret omkring 8.000 tons rene indigos til en værdi af 100 millioner mark hvert år.
Kemisk syntese mod slutningen af det 19. århundrede
Med den første vellykkede syntese af farvestof mauvein i 1856 af William Henry Perkin begyndte en konkurrence inden for videnskab og industri om udvikling af nye tjærefarver . Syntese af indigo, "farvenes konge", blev opnået i 1878 af den tyske kemiker Adolf von Baeyer, som i 1883 klargjorde dens kemiske struktur . De kemiske virksomheder BASF og Farbwerke vorm. Meister, Lucius & Brüning , den senere Farbwerke Hoechst, blev enige om i 1880 at udvikle Baeyers synteseruter til en teknisk proces. Imidlertid var Baeyers syntetiske ruter uegnede til industriel produktion, da de krævede råvarer ikke kunne produceres billigt på det tidspunkt.
En vigtig opfindelse til karfarvning med indigo blev foretaget af Paul Schützenberger i 1873 med indførelsen af natriumdithionit som reduktionsmiddel. Med reduktionsmidlet produceret i industriel skala af BASF fra 1906 var det muligt at producere leuco indigo i en simpel form.
I 1881 begyndte BASF at producere "Little Indigo", hvor et indledende produkt af den syntetiske indigo blev reduceret til indigo direkte på tekstilfiberen. På grund af dårlig markedsaccept ophørte imidlertid BASF processen kort tid senere. En syntese udviklet af Karl Heumann i 1890 baseret på N- phenylglycin , den såkaldte 1. Heumann-syntese , syntes mere lovende. Men da udbytterne i denne proces var meget lave, stoppede BASF denne procesudvikling igen i 1893.
De dårlige udbytter af den første Heumann-syntese kunne forbedres ved anvendelse af anthranilinsyre som udgangsmateriale. Den utilsigtede opdagelse af Eugen Sapper af den katalytiske oxidation af naphthalen med oleum med tilsætning af kviksølvsulfat til phthalsyre gav BASF det nødvendige råmateriale til syntese af anthranilinsyre. Det producerede svovldioxid kunne oparbejdes ved hjælp af den kontaktproces, der blev udviklet af Rudolf Knietsch hos BASF for at nå industriel modenhed . Baseret på denne syntesevariant bragte BASF den første syntetiske indigo på markedet i juli 1897 med høje investeringer.
I 1901 fandt Johannes Pfleger en variant af Heumann-syntesen ved Degussa , som også tillod Degussa og Farbwerke Hoechst at kommercialisere indigo. Som et resultat af konkurrence mellem kemiske virksomheder faldt prisen på indigo pr. Kg fra omkring 20 til 4 rigsmarker . I 1904 underskrev BASF og Farbwerke Hoechst "Indigo-konventionen", et kartel for at eliminere konkurrencen, der fastsatte en markedspris på 8 rigsmarker pr. Kg. Med starten på den industrielle produktion mistede naturlig indigo store markedsandele inden for få år. I 1914 havde naturlig indigo kun en andel på 4% af verdensmarkedet.
En kort stigning i vegetabilsk indigoproduktion opstod som et resultat af første verdenskrig og den tilhørende havblokade , som ikke tillod Tyskland at eksportere. Efter verdenskrig erstattede den syntetiske produktion af indigo den besværlige ekstraktion fra plantemateriale. Den syntetiske indigo tilbød en højere og konstant renhed og var derfor lettere at bruge. Derudover var farvestofferne ikke længere afhængige af resultatet af farvestoffets høst.
Efter første verdenskrig
Indigo mistede i stigende grad markedsandele på grund af nyudviklede syntetiske blå farvestoffer såsom indanthren . Det var kun med spredningen af jeansmode fra midten af 1960'erne, at der var fornyet efterspørgsel efter indigo. I 2011 brugte farvning af denim mere end 95% af de ca. 50.000 tons syntetiske indigoer, der produceres årligt. Dette gør det til et af de mest anvendte pigmenter til tekstilfarvning, som over en milliard blå jeans farves med hvert år.
Forskning inden for indigo-produktion og -anvendelse i dag fokuserer på udviklingen af farveprocesser med lavt vandindhold eller den elektrokemiske reduktion til leuko-indigo samt brugen af vand som opløsningsmiddel til syntese og omkrystallisering af indigo.
Fremstilling
Hentet fra farvestofplanter
Farvestofplanterne indeholder ikke indigo, men en forløber, indican , et glycosid af indoxyl .
Dette omdannes først til indoxyl, et derivat af indol , ved gæring med opsplitning af sukkerresten .
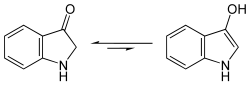
- Strukturformel for indoxyl, ligevægt mellem keto- og enolformer
Efterfølgende oxidation i luft forvandler den gule indoxyl til blå indigo.
Den traditionelle udvinding i Indien fandt sted i såkaldte indigofabrikker . Ekstraktionen finder sted i to højdeforskellige bassiner. Den friskhøstede indigoplante blev lagdelt i et første, højere bassin og doused med vand. Dele af planten blev nedvejet med sten og bjælker for at holde dem helt under vand. I dette bassin begyndte fermentering af indikanen til indoxyl ved tilsvarende høje omgivelsestemperaturer. Efter at gæringsprocessen var afsluttet blev det indoxylholdige vand drænet i et dybere bassin og ventileret mekanisk der. Arbejdstagerne klatrede ind i puljen og ramte den vandige opløsning med lameller eller lignende for at bringe luft ind. Indigo produceret ved oxidation blev derefter filtreret fra og kogt ned. Portionering og endelig tørring i luft fandt derefter sted. Renheden af indigo opnået på denne måde var mellem 15 og 70%. Dette blev forøget med fraktioneret udfældning fra svovlsyre. Ud over organiske urenheder indeholder naturlig indigo spor af uorganiske komponenter såsom silica , fosforsyre , ler og mange andre.
Biosyntesen af indigo-forløberne i højere planter blev undersøgt ved hjælp af isotopmærkning og finder sandsynligvis sted via shikiminsyrevejen :
I dette tilfælde shikimate ( 1 i flere faser til) korisere ( 2 konverteret). Dette omdannes til anthranilat ( 3 ) af anthranilatsyntase . Enzymet anthranilatphosphoribosyltransferase (EC 2.4.2.18) katalyserer reaktionen til N - (5- phospho - D- ribosyl) -anthranilat , som igen ved phosphoribosylantranilatisomerase (EC 5.3.1.24) til 1- (o-carboxyphenylamino) -1-deoxribulose-5-phosphat ( 4 ) reagerer. Ringlukning med decarboxylering giver indolderivatet 5 , som til sidst omdannes til aminosyren tryptophan ( 6 ). Dannelsen af indoxyl ( 7 ) fra tryptophan, hvor enzymerne tryptophanase og dioxygenase spiller en rolle, er endnu ikke fuldt klarlagt.
Synteser ifølge Adolf von Baeyer
Adolf von Baeyers første fuldt syntetiske produktion af indigo blev udført ved reduktion af isatin , som han tidligere var blevet identificeret som et nedbrydningsprodukt af indigo. Startende med phenyleddikesyre ankom han til oxindol i flere trin , som han yderligere oxiderede til isatin. Ved at klorere isatin med phosphorpentachlorid til dannelse af isatinchlorid og derefter reducere det med zink i eddikesyre ankom han til indigo.
En syntesevej udviklet af Baeyer og Drewsen ( Baeyer-Drewson reaktion ) førte til indigo via aldoladditionen af ortho- nitrobenzaldehyd og acetone via mellemtrin o -nitrophenyl mælkesyre keton. Denne syntetiske vej er enkel og nyttig til fremstilling af indigo og mange af dets derivater i laboratorieskala.
Begge synteseruter kunne ikke konverteres billigt til en industriel proces.
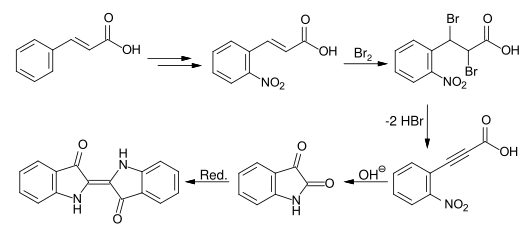
Baeyer udviklede en anden syntetisk rute, der startede fra kanelsyre . Den nitrering af den esterificerede kanelsyre giver, efter esterhydrolyse den o -Nitrozimtsäure. O- nitrophenylpropiolsyre opnås ved bromering og dobbelt dehydrobromering , som kan omdannes til isatin ved kogning med alkali og derefter reduceres til indigo.
Forskningslederen hos BASF og nær ven af Baeyers, Heinrich Caro , opdagede, at det isolerbare mellemprodukt o- nitrophenylpropiolsyre kunne omdannes til indigo direkte på fiberen under milde alkaliske forhold med natriumxanthat . BASF producerede denne såkaldte “lille indigo” i en årrække, men uden nogen stor succes på markedet.
Synteser ifølge Karl Heumann
I 1890 udviklede Zürichs kemiker Karl Heumann en ny syntesevej baseret på N- phenylglycin (1. Heumann-syntese ). Kemifirmaet BASF og Farbwerke Hoechst patenterede og videreudviklede processen. Serien af eksperimenter med phenylglycin blev afbrudt af BASF i 1893, fordi indigo-udbyttet var meget lavt.

- 1. Heumann-syntese (anilin ( 1 ), chloreddikesyre ( 2 ), N- phenylglycin ( 3 ), indoxyl ( 4 ), indigo ( 5 ))
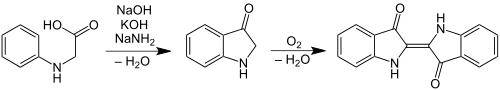
Heumann udviklede en alternativ syntesevej i 1897. Ved at reagere anthranilinsyre med chloreddikesyre ankom Heumann til phenylglycin- o- carboxylsyre. Hvis dette stof opvarmes til 200 ° C i en inert atmosfære med kaliumhydroxid , dannes der 2-indoxylcarboxylsyre. Dette materiale decarboxyleres let til indoxyl, som oxideres til indigo i luft (2. Heumann-syntese).

- 2. Heumann-syntese (anthranilinsyre ( 1 ), chloreddikesyre ( 2 ), phenylglycin- o- carboxylsyre ( 3 ), 2-indoxylcarboxylsyre ( 4 ), indoxyl ( 5 ), indigo ( 6 ))
industriel produktion
Et heldigt sammenfald med et ødelagt termometer førte til opdagelsen af, at kviksølvsulfat var en egnet katalysator til oxidation af naphthalen, der produceres i store mængder i tjærefarvestoffet til phthalsyre . Phthalsyren kunne omdannes til syreamidet ved reaktion med ammoniak . Ved hjælp af en efterfølgende Hofmann-omlægning opnåede BASF anthranilinsyre, som var påkrævet i industriel skala som et udgangsmateriale til Heumann-syntesen.

- Produktion af anthranilinsyre ved hjælp af Hofmann-omlejring af phthalimidet
Ved hjælp af 2. Heumann-syntese kunne anthranilinsyren behandles til indigo i udbytter på 70 til 90%. Fra 1897 og frem producerede BASF syntetisk indigo i industriel skala ved hjælp af denne proces.
I 1901 lykkedes Degussa at bruge en proces af Johannes Pfleger til at opnå indigo i høje udbytter ved hjælp af natriumamid , som blev produceret i Castner-Kellner-processen til produktion af natriumcyanid , og en alkalismelt N- phenylglycin ved en temperatur på omkring 200 ° C (Heumann-Pleger-syntese). Natriumamidet tjener som et dehydratiseringsmiddel. Denne proces blev markedsført sammen med Farbwerke Hoechst:
BASF har produceret indigo ved hjælp af denne proces siden 1926.
I 1905 udviklede BASF en procesvariant af Heumann-Pfleger-syntesen, hvor det dyre natriumamid blev erstattet af billigere calciumoxid . Processen blev overført til en tidligere udviklet syntetisk rute. Anilin er omsat med ethylenchlorhydrin til dannelse 2-anilinoethanol , som omdannes til indoxyl i en natriumhydroxid - kalium hydroxid - calciumoxid smelte ved temperaturer på ca. 280 ° C med tilfredsstillende udbytter . BASF produceret i henhold til denne proces fra 1909 til 1924.
Fra 1924 var indigosyntese ved BASF baseret på phenylglycinnitril, som var fremstillet af anilin. I alle tilfælde dannes indoxyl, som oxideres til indigo af atmosfærisk ilt. Den åbenlyse antagelse om, at dannelsen af indigo sker gennem basekatalyseret kondens mellem isatin og indoxyl, kunne udelukkes ved mekanistiske undersøgelser. Oxidationen af indoxyl i basisk opløsning sker sandsynligvis via et radikalt mellemprodukt . Uanset om dannelsen finder sted via koblingen af to indoxylradikaler eller koblingen af en indoxylradikal og en indoxylanion, kunne det ikke klart fastslås eksperimentelt.
Mikrobiologisk syntese
Allerede i 1920'erne blev det observeret, at jordbakterier kunne syntetisere indigo fra indol . I mellemtiden kendes et antal mikrobielle indigoproducenter såsom Pseudomonas putida , som kan danne indigo fra aromatiske carbonhydrider såsom naphthalen , cumen eller styren . Enzymsystemet, der er ansvarligt for dannelse af indigo, består af et eller flere enzymer, typisk monooxygenaser , dioxygenaser eller hydroxylaser .
De største problemer ved den mikrobiologiske vej er den høje fortynding af indigo og den indsats, der er forbundet med at adskille den betydelige mængde organisk materiale. Indtil videre er en mikrobiologisk syntesevej derfor ikke kommercialiseret.
Handelsformer
Store europæiske producenter af indigo er DyStar , oprindeligt et joint venture mellem Bayer , Hoechst og BASF og siden 2010 i kinesisk-indisk ejerskab samt Archroma , en spin-off af den schweiziske koncern Clariant . Der er et stort antal producenter i Asien, herunder TaiFeng Chemical Industrial , Zhejiang Runtu og Bodal Chemicals . Indigo fås i en ikke-reduceret eller pre-reduceret form. De ikke-reducerede kvaliteter fås som granuler , pulver eller alkalisk pasta. Typiske kommercielle former for pastaen indeholder 20 til 30% indigo. De præ-reducerede opløsninger fås i koncentrationer på 20 til 60%.
ejendomme
Fysiske egenskaber
Indigo har et ret højt smeltepunkt på omkring 390-392 ° C og sublimerer ved en temperatur på 170 ° C. Det er dårligt opløseligt i vand, ethanol og diethylether. Dette skyldes det faktum, at indigo danner en hydrogenbinding polymer i fast tilstand . Røntgenstrukturanalyser har vist, at hvert indigomolekyle er bundet til fire omgivende molekyler. Indigo krystalliserer monoklinisk i rumgruppen P 2 1 / c (nr. 14) med gitterparametrene a = 924 pm ; b = 577 pm; c = 1222 pm og P = 117,0 °, Z = 2.
Det infrarøde spektrum kan bestemmes ved hjælp af ATR infrarød spektroskopi . Strækningsvibrationen af carbonylgruppen ved et bølgetal på 1623 cm -1 er karakteristisk . Et intens bånd på 1065 cm -1 tildeles vibrationen i den femleddede ring.
Molekylære egenskaber
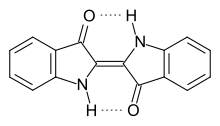
Indigo har en plan struktur med en C 2h symmetri . Den fotokemiske stabilitet af indigo skyldes intramolekylære hydrogenbindinger mellem de nærliggende carbonyl- og sekundære aminogrupper . Disse stabiliserer molekylet i en plan trans- konfiguration og hæmmer således en fotokemisk cis-trans- isomerisering .
Farven på et molekyle skyldes dets evne til at absorbere elektromagnetisk stråling. Hvis dette finder sted i området med synligt lys, ser stoffet ud som farvet. Den komplementære farve til farven på det absorberede lys opfattes altid som farven. Betingelsen for farve er derfor tilstedeværelsen af elektroner, der ophidses af synligt lys. Ifølge Witt's farvestofteori består et farvestof af en kromofor ( gammel græsk χρῶμα chrṓma , tysk 'farve' , gammelgræsk φορός phorós , tysk 'bærer' ), for eksempel et delokaliseret π-elektron-system, der gør farven mulig og en auxochrome (fra gammel græsk αὐξεῖν auxein , tysk 'vokse' og oldgræsk χρῶμα Chroma , tysk 'farve' ), for eksempel en elektrondonor med en + M virkning at skift absorptionsmaksimum kromoforen i det længere bølge område af spektret . Indigo har to konjugerede carbonylgrupper som kromofor. På grund af dette strukturelle element tilhører indigo gruppen af carbonylfarvestoffer .
Absorptionen af elektromagnetisk stråling forårsager en elektronoverførsel fra den højest optagne molekylære orbital ( HOMO ) til den laveste ledige molekylære orbital ( LUMO ). Hvis der ikke er nogen auxokrom gruppe, er energiforskellen mellem HOMO og LUMO relativt stor, og absorptionen gennem π → π * overgangen finder sted i det usynlige område. Det ene par elektroner fra den sekundære aminogruppe i indigo tjener som en elektrondonor og interagerer med π-systemet i kromoforen. Dette skaber tre nye molekylære orbitaler π 1 , π 2 og π * 3 , hvorved energiforskellen mellem HOMO og LUMO bliver mindre. Overgangen π 2 → π * 3 sker med indigo gennem lys i det orange område. Indigo ser derfor ud til at være blå.
Kemiske egenskaber
Den elementaranalyse af indigo tilvejebringer en empirisk molekylformel C 8 H 5 NO. Ved cryoscopic målinger resulterer i en molekylformel C 16 H 10 N 2 O 2 . Indigo er et meget let og temperaturstabilt molekyle. Ved højere temperaturer på omkring 460 ° C omarrangeres det til dannelse af dibenzonaphthyridinedion , hvorved bindingerne mellem carbonylgrupperne og den centrale carbon-carbon-dobbeltbinding brydes .
I det alkaliske miljø nedbrydes molekylet ved højere temperaturer i forbindelser som anilin og anthranilinsyre. Sulfoneringen til indigokarmin finder sted i koncentreret svovlsyre . Oxidation med kaliumpermanganat tilvejebringer isatin.
Indigo kan let reduceres i det svagt sure og alkaliske område. Den leucoform er i ketoformen under en pH-værdi på 5,5. I området mellem 5,5 og 11 er mono-enolatet til stede, og fra en pH-værdi på 11 er di-enolatet til stede.

- Reduktion af indigo til leukoform (afhængigt af pH-værdien som di-enolat, mono-enolat eller diketon)
Med chlorsulfonsyre danner leuco-formen natriumsalte af svovlsyreestere, såkaldte indigosoler . Indigosolerne er vandopløselige og egner sig til farvning af uld, som derefter oxideres med salpetersyre , hvor forsæbning finder sted på samme tid . Som en monokelaterende ligand danner indigo opløselige metalkomplekser med palladium- og platinsalte, der hverken har intra- eller intermolekylære hydrogenbindinger.
brug
Moms farve
Indigo bruges til farvning blandt andet på grund af dets fremragende lysstabilitet. Forbindelsen absorberes stærkt af bomuldsfibre og er meget vaskbar. Indigo i sig selv er næsten uopløselig i vand og skal omdannes til den vandopløselige leuco indigo (fra græsk leukós : hvid, skinnende) ved reduktion inden farvning , for eksempel ved anvendelse af natriumdithionit , den såkaldte vatting.
Før anvendelsen af natriumdithionit bestod den såkaldte gæringsbeholder traditionelt af et fermenterbart materiale såsom sirup eller andre kulhydratholdige stoffer og et alkalisk tilsætningsstof, såsom kalk eller urin . De kulhydrater tjente som et reduktionsmiddel . Andre reduktionsmidler såsom arsen sulfid , jern (II) sulfat eller zinkstøv blev brugt senere .
Til farvning placeres bomuldsstoffet derefter i den vandige beholderopløsning med den reducerede, farveløse leukoform. Den opløselige komponent absorberes af fiberen, og når den tørres i luften, dannes indigo igen gennem oxidation. Følgelig opstår den blå farve kun efter kontakt med ilt. Indigo danner ikke en kemisk binding med fiberen, men klæber til den gennem klæbende kræfter .
Denne proces er kendt som farvning af kar og bruges også til andre tekstilfarvestoffer. Tidligere blev stofferne anbragt i solen på en eng for at oxidere farvestoffet, hvor indigo blev oxideret ved blegning af plænen . Syntetisk produceret indigo anvendes i vid udstrækning som et farvestof i tekstilindustrien. Det meste af tiden bruges indigo til at farve denimstoffer .
Andre metoder til farvning af tekstiler
I England udviklede farvestoffer to andre metoder til indigofarvning i det 18. og 19. århundrede. Den første metode er kendt som "Pencil Blue". Arsen-trisulfid og et fortykningsmiddel blev tilsat til leuco indigo til stabilisering . Arsenforbindelsen forsinkede oxidationen af indigo, så den kunne påføres tekstiler med blyanter eller børster.
I den anden metode blev den uopløselige indigo trykt direkte på stoffet og derefter reduceret under anvendelse af jern (II) sulfat . Oxidation med luft fandt derefter sted igen. Denne såkaldte "China blue" -proces producerede klare designs. Mod slutningen af det 19. århundrede udviklede John Bracewell glukoseprocessen, som tillod direkte udskrivning med indigo.
Den plan er en traditionel tekstiltryk teknologi samt navnet på den mørkeblå stof med hvide mønstre produceret med denne trykmetode. Det er et reservetryk , hvor stoffet er trykt med en beskyttende forbindelse for at holde det hvidt. Efter udskrivning med den beskyttende forbindelse er stoffet farvet med indigo.
Traditionel kinesisk medicin
I traditionel kinesisk medicin anvendes Indigo Naturalis i kombination med realgar indeholdende arsen til behandling af promyelocytisk leukæmi . Indigo Naturalis bruges også mod psoriasis . Imidlertid synes den aktive ingrediens i Indigo Naturalis-præparater at være indirubin , der fungerer som en hæmmer af cyclinafhængige kinaser . Banlangen , et traditionelt kinesisk middel, er for eksempel lavet af woad eller indigo-planten og bruges til at behandle ondt i halsen og strubehovedet og en række andre sygdomme.
Andre anvendelser
Den Maya har været at gøre det mayaernes blå pigment siden omkring 800 e.Kr.. Pigmentet er blevet identificeret som en sammensætning af palygorskit og indigo, sandsynligvis afledt af bladene af en indfødt art af indigofera. En nuværende opskrift til fremstilling af Maya blå blev offentliggjort i 1993.
Til tekniske formål kan indigo bruges i form af tynde organiske film til konstruktion af solceller . Forskning har vist, at indigo kan bruges i felteffekt-transistorer . En tynd film af halvkrystallinsk indigo er en halvleder med et båndgab på 1,7 eV og dermed et potentielt materiale til organisk elektronik .
Indigo blev sjældent brugt i oliemaleri indtil omkring slutningen af det 17. århundrede. Et af de mest berømte eksempler er Vermeers værk ” Kristus med Maria og Martha ”, hvor både Kristi blå kappe og Marias nederdel er malet med indigo.
Indigo kan bruges til at måle koncentrationen af ozon i luften. Til dette formål er kromatografipapir gennemblødt i indigo. Isatin dannes, når det kommer i kontakt med ozon i luften. Dette bestemmes fotometrisk efter eluering . Et andet reaktionsprodukt er isatoinsyreanhydrid. Indigoidfarvestoffer kan også bruges til at detektere ozon.
I Japan blev Indigo Naturalis brugt i traditionel medicin som et antiinflammatorisk stof. Den samurai bar tøj farvet med indigo til at helbrede sår og skader. På grund af de mistænkte positive helbredseffekter er indigofarvede tæpper og tøj stadig traditionelle gaver til nyfødte for at beskytte dem mod sygdom. Nogle romerske og græske midler indeholdt indigo.
Indigoid farvestoffer
Indigoidfarvestoffer er strukturelt relateret til indigo. Disse inkluderer for eksempel de varianter, der er skabt ved at ændre indigo-rygraden, for eksempel ved at erstatte den sekundære aminogruppe med andre elektrondonorer, såsom selen , svovl eller ilt . Tabellen viser sammenligningen af det længste bølgeabsorptionsbånd for disse forbindelser sammenlignet med indigo (λ max. Ved 606 nm).
| Efternavn | Grundlæggende struktur | x | λ max (nm) (i ethanol ) |
|---|---|---|---|
| indigo |

|
NH | 606 |
| Selen indigo | Se | 562 | |
| Thioindigo | S. | 543 | |
| Oxindigo | O | 432 |
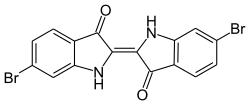
Syntesen af strukturelle isomerer eller derivatisering af benzenringen åbner yderligere muligheder for farvevariation. Den strukturelle isomer indirubin er et rødviolet farvestof, og indigokarmin (5,5'-indigodisulfonsyre dinatriumsalt) er et blåt farvestof. Ringsubstituerede derivater af indigo kan syntetiseres på forskellige måder. Anvendelsen af bromsubstitueret nitrobenzaldehyd i den klassiske syntese ifølge Baeyer fører til dannelsen af lilla (6,6'-dibromoindigo), et gammelt farvestof opnået fra lilla snegle . Dens struktur blev afklaret i 1909 af Paul Friedlaender . Yderligere eksempler på indigoidfarvestoffer er 5,5 ', 7,7'-tetrabromindigo (strålende indigo B) eller 2- (5-bromindol) -5-brom-2'-thionaphthenindigo (Cibaviolet 3B). Mange forskellige indigoidfarvestoffer såsom thioindigo eller tetrachlorindigo er kommercielt tilgængelige. Sammenlignet med indigo er derivaternes økonomiske betydning imidlertid ret lille.
Toksikologi og miljømæssige aspekter
Indigo har lav pattedyrstoksicitet. Den LD 50 værdien i musen er 32 g / kg. Der er ingen tegn på sensibilisering hos mennesker efter gentagne hudanvendelser. Fodringsforsøg på rotter og hunde med op til 3 vægtprocent indigo i foderet viste ingen alvorlige skadelige sundhedsmæssige konsekvenser.
Nogle af de kemikalier, der anvendes til fremstilling af indigo, såsom anilin, formaldehyd eller hydrogencyanid, er giftige og miljøfarlige og håndteres derfor kun i lukkede systemer. Indigo har ingen skadelige virkninger på aktiveret slamsystemer i biologiske spildevandsrensningsanlæg på grund af dets lave opløselighed, men graden af bionedbrydning er lav. Ultrafiltreringssystemer er egnede til fjernelse af pigmentet, før det indføres i spildevandsbehandlingsanlægget. Uomsatte råmaterialer såsom anilin eller anthranilinsyre er let biologisk nedbrydelige. For at reducere saltbelastningen i den egentlige farvningsproces tilbydes præ-reducerede applikationer, der gør brugen af natriumdithionit som reduktionsmiddel unødvendig. En ny form for handel med indigo er derfor blevet etableret i de senere år. En indigo-suspension reduceres katalytisk til leukoform med hydrogen og markedsføres som et præ-reduceret, koncentreret flydende indigo-mærke.
litteratur
- Elmar Steingruber: Indigo og indigo farvestoffer. I: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2004 doi: 10.1002 / 14356007.a14 149.pub2 .
- Renate Kaiser-Alexnat: Indigo. Farvenes konge. I: Sydøstasien Magazine . Bind 3, 2008, s. 110-121, (PDF; 3,3 MB) , (specialudgave) .
- Helmut Schmidt: Indigo. 100 års industriel syntese. I: Kemi i vores tid . Bind 3, 1997, s. 121-128, doi: 10.1002 / ciuz.19970310304 .
- Paul Rys, Heinrich Zollinger: Farvestofkemi - En guide. 3. revideret udgave, Wiley-VCH, Weinheim 1982, ISBN 3-527-25964-3 .
Weblinks
Individuelle beviser
- ↑ en b c d indtastning på indigo i GESTIS stof database af den IFA , adgang den 1. februar, 2016. (JavaScript krævet)
- Mar a b c d e f g h Elmar Steingruber: Indigo og indigo farvestoffer . I: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2004, doi: 10.1002 / 14356007.a14 149.pub2 .
- ↑ a b post om indigo. I: Römpp Online . Georg Thieme Verlag, adgang til 4. maj 2014.
- ↑ Albert Gossauer: Struktur og reaktivitet af biomolekyler. Verlag Helvetica Chimica Acta, Zürich 2006, s. 477, ISBN 978-3-906390-29-1 .
- ↑ Christian-Herbert Fischer: Historiske organiske farvestoffer. I: Spectrum of Science . Oktober 1997, s. 104.
- ↑ a b c d e f g Renate Kaiser-Alexnat: Indigo - Kongen af farvestoffer . I: Sydøstasien Magazine . 3/2008; Pp. 110-121, ISBN 978-3-7375-9664-0 .
- ^ Genindførelse af Indigo .
- ↑ Kan et blåt farvestof hjælpe med at redde Aralhavet?
- ↑ a b R. Hegnauer, M. Hegnauer: Chemotaxonomy of plants. Bind XI: Leguminosae. Birkhäuser, Basel / Boston / Berlin 1994, ISBN 978-3-0348-9392-3 , s. 1047.
- ↑ a b Colleen E. Kriger: Tøj i vestafrikansk historie. Altamira Press, New York 2006, ISBN 978-0-7591-0421-1 , s. 120-124.
- ↑ Jeffrey C. Splitstoser, Tom D. Dillehay, Jan Wouters, Ana Claro: Tidlig præ-spansktalende brug af indigoblå i Peru. I: Videnskabelige fremskridt . Bind 2, 2016, s. E1501623; doi: 10.1126 / sciadv.1501623 .
- ^ W. Conard Fernelius, Edgar E. Renfrew: Indigo. I: Journal of Chemical Education . Bind 60, 1983, s. 633, doi: 10.1021 / ed060p633 .
- ↑ Gaius Iulius Caesar, De bello Gallico 5,14,2 ( online ).
- ↑ M. Van der Veen, AR Hall, J. May: Woad and the Britons Painted Blue. I: Oxford Journal of Archaeology . Bind 12, nr. 3, 1993, s. 367-371; doi: 10.1111 / j.1468-0092.1993.tb00340.x .
- Ete Margarete Bruns: Fra azurit, indigo og anilin. Om historien om den blå farve. I: Emil Ernst Ploß: En bog med gamle farver. Tekstil af tekstilfarver i middelalderen med udsigt til solide farver. 6. udgave, Impuls Verlag, München 1989, ISBN 978-3-89164-060-9 , s. 14-20.
- Hard Reinhard Schneider : Capitulare de villis. I: Kortfattet ordbog om tysk juridisk historie . Bind 1, 2. udgave, Schmidt, Berlin, ISBN 978-3-503-07912-4 , s. 809-811.
- ^ Robin JH Clark, Christopher J. Cooksey, Marcus AM Daniels, Robert Withnall: Indigo, woad og Tyrian Purple: vigtige karfarvestoffer fra antikken til nutiden. I: Endeavour . Neue Serie, bind 17/4, 1993, 192, s. 191-199; doi: 10.1016 / 0160-9327 (93) 90062-8 .
- ^ Wilhelm Hassenstein, Hermann Virl : Fyrværkeribogen fra 1420. 600 års tysk pulvervåben og våbensmed. Genoptryk af det første tryk fra 1529 med oversættelse til højtysk og forklaringer af Wilhelm Hassenstein. Verlag der Deutsche Technik, München 1941, s. 108 ( Indig, indicum eller Waidtsblau og Waidblum ).
- ↑ a b c d e f g h i j k l Helmut Schmidt: Indigo - 100 års industriel syntese. I: Kemi i vores tid . Bind 31, 1997, s. 121-128; doi: 10.1002 / ciuz.19970310304 .
- ^ David Paterson: Vedrørende indigo, naturlig og kunstig. I: Oil and Colourman's Journal . Bind 28, nr. 357 og 358, august 1905.
- ↑ Sabine Struckmeier: Tekstilfarvning fra den sene middelalder til den tidlige moderne periode . Waxmann, Münster 2011, ISBN 978-3-8309-2527-9 , s. 177-178.
- ↑ Werner Abelshauser: BASF: En virksomhedshistorie. 2. udgave, Beck, München 2003, ISBN 3-406-49526-5 , s. 132.
- ↑ Lauren Wolf: Hvad er det der? Blå jeans . I: Chemical & Engineering News . 24. oktober 2011, bind 89, nummer 43, s.44.
- ^ AD Kinghorn, H. Falk, J. Kobayashi: Fremskridt inden for kemi af organiske naturlige produkter. Bind 99, Springer-Verlag, Heidelberg / New York 2014, ISBN 978-3-319-04899-4 , s.88 .
- ↑ Wrangler-denim vedtager branchens første "tørfarvning" -proces.
- ^ Elektrokemisk indigomaskine debuterer i Pakistan .
- ↑ M. Josef Taublaender, Florian Glöcklhofer, Martina Marchetti-Deschmann, Miriam M. Unterlass: Indvendigt omslag: Grøn og Rapid Hydrotermisk Krystallisation og syntese af Fully konjugerede aromatiske forbindelser. I: Angewandte Chemie International Edition . Bind 57, 2018, s. 12180; doi: 10.1002 / anie.201808280 .
- ↑ Indtastning i enzymnomenklaturdatabasen for anthranilatphosphoribosyltransferase .
- ↑ a b A. D. Kinghorn, H. Falk, J. Kobayashi: Progress in the Chemistry of Organic Natural Products. Bind 99.Springer-Verlag, Heidelberg / New York 2016, ISBN 978-3-319-34645-8 , s.82 .
- ↑ Indtastning i enzymnomenklaturdatabasen for phosphoribosylantranilatisomerase .
- ↑ a b Arne Andersen: Historisk teknologivurdering ved hjælp af eksemplet på metalbearbejdning og den kemiske industri 1850-1933 (== Zeitschrift Fur Unternehmensgeschichte - Supplements. Volume 90). Steiner, Stuttgart 1996, s. 238.
- Olf Adolf Baeyer, Viggo Drewsen: Repræsentation af indigblåt fra orthonitrobenzaldehyd. I: Rapporter fra det tyske kemiske selskab . Bind 15, 1882, s. 2856-2864; doi: 10.1002 / cber.188201502274 .
- ^ Fritz Mayer: Kemi af organiske farvestoffer . Springer-Verlag, Berlin, Heidelberg 1921, ISBN 978-3-662-05490-1 , pp. 199 ( begrænset forhåndsvisning i Google Book-søgning).
- ↑ BASF-patent DE 171.172, indgivet 23. januar 1904
- ^ Glen Allan Russell, Gerd Kaupp: Reaktioner fra resonansstabiliserede carbanions. XXXI. Oxidation af carbanions. 4. Oxidation af indoxyl til indigo i basisk opløsning. I: Journal of the American Chemical Society . Bind 91, 1969, s. 3851-3859; doi: 10.1021 / ja01042a028 .
- ↑ PHH Grey: Den Dannelse af indigotin fra indol ved jordbakterier. I: Proceedings of the Royal Society B: Biological Sciences . Bind 102, 1928, s. 263-281; doi: 10.1098 / rspb.1928.0003 .
- Bh B. Bhushan, SK Samanta, RK Jain: Indigoproduktion af naphthalen-nedbrydende bakterier. I: Letters in Applied Microbiology . Bind 31, 2000, s. 5; doi: 10.1046 / j.1472-765x.2000.00754.x .
- ^ Klaus Hunger: Industrielle farvestoffer: Kemi, egenskaber, applikationer. Wiley-VCH, Weinheim 2003, ISBN 3-527-30426-6 , s. 231.
- ^ Paul Rys, Heinrich Zollinger: farvestofkemi. En guide. 3. revideret udgave, Wiley-VCH, Weinheim 1982, ISBN 3-527-25964-3 , s.137 .
- ↑ H. v. Eller i: Bulletin de la Société Chimique de France . Bind 106, 1955, s. 1426.
- ↑ Peter Süsse, Manfred Steins, Vladimir Kupcik: Indigo: Krystalstrukturforfining baseret på synkrotrondata. I: Journal of Crystallography - Crystalline Materials. Bind 184, 1988, s. 269-273; doi: 10.1524 / zkri.1988.184.14.269 .
- ↑ Anna Baran, Andrea Fiedler, Hartwig Schulz, Malgorzata Baranska: In situ Raman og IR spektroskopisk analyse af indigofarvestof. I: Analytiske metoder . Bind 2, 2010, s. 1372; doi: 10.1039 / c0ay00311e .
- ↑ en b Stefan Bienz, Laurent Bigler, Thomas Fox, Herbert Meier: Spektroskopiske metoder i organisk kemi. 9. udgave, Thieme, Stuttgart / New York 2016, ISBN 978-3-13-576109-1 .
- ↑ Vu Thi Ngan, G. Gopakumar, Tran Thanh Hue, Minh Tho Nguyen: Indigoens triplettilstand: Elektroniske strukturberegninger . I: Chemical Physics Letters . Bind 449, 2007, s. 11-17; doi: 10.1016 / j.cplett.2007.10.015 .
- ^ J. Seixas de Melo, AP Moura, MJ Melo: Fotofysiske og spektroskopiske undersøgelser af indigoderivater i deres keto- og leukoform . I: Journal of Physical Chemistry A . Bind 108, nr. 34, 2004, s. 6975-6981; doi: 10.1021 / jp040753y .
- ↑ Eberhard Breitmaier, Günther Jung: Organisk kemi. Udgave 5, Thieme, Stuttgart / New York 2005, ISBN 978-3-13-541505-5 , s. 728-734.
- ↑ Günter Hauke, Gerhard Graneß: Termisk isomerisering af indigo. I: Angewandte Chemie International Edition på engelsk . Bind 34, 1995, s. 67; doi: 10.1002 / anie.199500671 .
- ↑ GA Baig: Farvning af nylon med indigo i forskellige pH-regioner . I: AUTEX Research Journal . Bind 10, 2010, s. 21-25.
- ↑ F. Weiss: Indigosålene og deres anvendelse . I: Karfarvestoffer og deres anvendelse til farvning og stofprint. Springer-Verlag, Wien 1953, ISBN 978-3-7091-7827-0 , s. 313-364.
- ↑ Wolfgang Beck, Christoph Schmidt, Rolf Wienold, Manfred Steimann, Barbara Wagner: Indigo-Metal Complexes: Synthesis and Structure of Pd II and Pt II Compounds Containing the Anions of Indigo and Octahydroindigo as Mono- and Bis-Chelate Ligands. I: Angewandte Chemie International Edition på engelsk. Bind 28, 1989, s. 1529-1531; doi: 10.1002 / anie.198915291 .
- ↑ Izumi Iwakura, Atushi Yabushita, Takayoshi Kobayashi: Hvorfor er Indigo fotostabil over ekstremt lange perioder?. I: Chemistry Letters . Bind 38, 2009, s. 1020; doi: 10.1246 / cl.2009.1020 .
- ↑ Laksanawadee Saikhao, Jantip Setthayanond, Thitinun Karpkird, Thomas Bechtold, Potjanart Suwanruji: Grøn reduktionsmidler til indigo farvning på bomuldsstoffer. I: Journal of Cleaner Production. Bind 197, 2018, s. 106-113; doi: 10.1016 / j.jclepro.2018.06.199 .
- ^ KG Gilbert nee Stoker, DT Cooke: Farvestoffer fra planter: Tidligere brug, nuværende forståelse og potentiale . I: Plantevækstregulering . Bind 34, nr. 1, 2001, s. 57-69; doi: 10.1023 / A: 1013374618870 .
- ^ DS Balan, RT Monteiro: Affarvning af tekstilindigofarvestof af ligninolytiske svampe . I: Journal of Biotechnology . Bind 89, nr. 2-3, 2001, s. 141-145; PMID 11500207 .
- ↑ a b P. C. Floud: Det engelske bidrag til den tidlige historie med indigotrykning . I: Journal of the Society of Dyers and Colourists . Bind 76, 1960, s. 344-349; doi: 10.1111 / j.1478-4408.1960.tb02382.x .
- ↑ Patent US409906 : Fremgangsmåde til udskrivning af mørkeblå farver.
- ↑ Landsdækkende bibliotek over immateriel kulturarv: plan .
- ↑ L. Wang, G.-B. Zhou, P. Liu, J.-H. Song, Y. Liang, X.-J. Yan, F. Xu, B.-S. Wang, J.-H. Mao, Z.-X. Shen, S.-J. Chen, Z. Chen: Dissektion af mekanismer med kinesisk medicinsk formel Realgar-Indigo naturalis som en effektiv behandling for promyelocytisk leukæmi. I: Proceedings of the National Academy of Sciences . Bind 105, 2008, s. 4826-4831; doi: 10.1073 / pnas.0712365105 .
- ↑ John Koo, Sumaira Arain: Traditionel kinesisk medicin til behandling af dermatologiske lidelser. I: Dermatology Archives . Bind 134, 1998, s. 1388-1393. doi: 10.1001 / archderm.134.11.1388 .
- ↑ Ralph Hoessel, Sophie Leclerc, Jane A. Endicott, Martin EM Nobel, Alison Lawrie, Paul Tunnah, Maryse Leost, Eve Damiens, Dominique Marie, Doris Marko, Ellen Niederberger, Weici Tang, Gerhard Eisenbrand, Laurent Meijer: indirubin, den aktive bestanddel af et kinesisk antileukæmemedicin, hæmmer cyklinafhængige kinaser. I: Naturcellebiologi . Bind 1, 1999, s. 60-67; doi: 10.1038 / 9035 .
- ↑ Antonio Doménech-Carbó, Sigrid Holmwood, Francesca Di Turo, Noemí Montoya, Francisco Manuel Valle-Algarra, Howell GM Edwards, María Teresa Doménech-Carbó: Sammensætning og farve af Maya Blue: Reexamination of Literature Data Based on the Dehydroindigo Model. I: Journal of Physical Chemistry C . Bind 123, 2018, s. 770-782; doi: 10.1021 / acs.jpcc.8b08448 .
- ↑ Constantino Reyes-Valerio: De Bonampak al Templo borgmester. I: El azul maya en Mesoamerica. Siglo XXI Editores, Mexico DF 1993, s. 157. Azul Maya - Maya Blue Pigment. (Engelsk).
- ↑ K. Uehara, K. Takagishi, M. Tanaka: Al / Indigo / Au solcelle. I: Solceller . Bind 22, 1987, s. 295-301; doi: 10.1016 / 0379-6787 (87) 90059-7 .
- ↑ Roswitha Harrer: Indigo på hukommelseschips. I: Kemi i vores tid . Bind 46, 2012, s.136; doi: 10.1002 / ciuz.201290032 .
- ↑ Mihai Irimia-vládu, Eric D. Głowacki, Pavel A. Troshin, Günther Schwabegger, Lucia Leonat, Diana K. Susarova, Olga Krystal, Mujeeb Ullah, Yasin Kanbur, Marius A. Bodea, Vladimir F. Razumov, Helmut sitter, Siegfried Bauer, Niyazi Serdar Sariciftci: Indigo - Et naturligt pigment til højtydende ambipolære organiske felteffekttransistorer og kredsløb. I: Avancerede materialer . Bind 24, 2012, s. 375-380; doi: 10.1002 / adma.201102619 .
- ^ H. Schweppe: Indigo og Woad . I: EW FitzHugh (red.): Kunstneres pigmenter. En håndbog om deres historie og egenskaber. Bind 3, Oxford University Press, Oxford 1997, s. 81-107 ([Artists Pigments: A Handbook of their History and Characteristics Digitalisat]).
- ^ Vermeer, Kristus i Marta og Marys hus, ColourLex.
- ↑ P. Remler, W. Kosmus: Integral langsigtet metode til bestemmelse af ozon i atmosfæren. I: Fresenius magasin til analytisk kemi . Bind 329, 1988, s. 871-874; doi: 10.1007 / BF00471974 .
- ^ Daniel Grosjean, Paul M. Whitmore, Glen R. Cass, James R. Druzik: Ozonfading af naturlige organiske farvestoffer: mekanismer og produkter til reaktion mellem ozon og indigos. I: Miljøvidenskab og teknologi . Bind 22, 1988, s. 292-298; doi: 10.1021 / es00168a009 .
- ↑ Samurai Blue: A History of Indigo
- ^ Rebecca Futo Kennedy, Molly Jones-Lewis: Routledge-håndbogen om identitet og miljø i de klassiske og middelalderlige verdener . Routledge, New York 2016, ISBN 978-0-415-73805-7 , s. 155-161.
- ^ Paul Rys, Heinrich Zollinger: farvestofkemi. En guide. 3. revideret udgave, Wiley-VCH, Weinheim 1982, ISBN 3-527-25964-3 , s.136 .
- ^ Gundula Voss, Hans Gerlach: Regioselektiv brom / lithium-udveksling i 2,5-dibrom-1-nitrobenzen. - En simpel syntese af 4-brom-2-nitrobenzaldehyd og 6,6'-dibromoindigo. I: Kemiske rapporter . Bind 122, 1989, s. 1199-1201; doi: 10.1002 / cber.19891220628 .
- ↑ Paul Friedländer: Om farvestoffet i gammel lilla fra murex brandaris. I: Rapporter fra det tyske kemiske selskab . Bind 42, 1909, s. 765-770; doi: 10.1002 / cber.190904201122 .
- ↑ E. Grandmougin, P. Seyder: Om Indigo. V: Om halogeneret indigo og derivater. I: Rapporter fra det tyske kemiske selskab . Bind 47, 1914, s. 2365-2373; doi: 10.1002 / cber.191404702154 .
- ↑ Dataark Indigo (CI 73000) synt. (PDF) fra Carl Roth , tilgængelig den 3. november 2019.
- ↑ Anne Vuorema: Reduktions- og analysemetoder for indigo. University of Turku, 2008, ISBN 978-9-51293781-3 , s. 14.
- ↑ Abraham Reife, Harold S. Freeman: Miljøkemi af farvestoffer og pigmenter. John Wiley and Sons, New York 1996, ISBN 0-471-58927-6 , s. 208-209.
- ↑ Patentansøgning DE19831291 : Koncentreret leuco-indigo-opløsning, især til farvning af bomuldsgarp til blå denim, indeholder leuco-indigo i form af en blanding af salte af mindst to alkalimetalhydroxider. Registreret den 13. juli 1998 , offentliggjort den 20. februar 2000 , ansøger: BASF AG, opfinder: Manfred Gäng, Rudolf Krüger, Peter Miederer.