Rundorminfektioner hos hunden
Nematodeinfektioner hos hunden - infektion ( infektion , også angreb ) hos hunde med parasitiske levende nematoder (Nematoda) - udover bændelormangreb og infektioner med protozoer ( giardiasis , neosporose ) almindelige parasitiske sygdomme i veterinærpraksis. Som såkaldte endoparasitter ("indre parasitter") koloniserer rundorm forskellige indre organer - de fleste af dem fordøjelseskanalen - og huden. Indtil videre er der identificeret omkring 30 forskellige nematodearter hos husdyr; de er i det væsentlige også i naturenAt finde hundearter . Imidlertid forårsager de fleste af disse ofte små eller ingen sygdomssymptomer hos voksne dyr. Infektionen behøver ikke nødvendigvis at manifestere sig i en ormesygdom ( helminthosis ). For de fleste rundorme kan infektion påvises ved at undersøge afføringen for æg eller larver. I Centraleuropa er angreb med rundorm og hundekrogorm af særlig betydning med hensyn til sundhedspolitik , da de også kan sprede sig til mennesker ( zoonose ). Regelmæssig aformning kan markant reducere antallet af angreb og dermed risikoen for infektion hos mennesker og hunde.

Parasitose i fordøjelseskanalen
Rundormangreb
Der er to typer rundorm hos hunde : Toxocara canis og Toxascaris leonina .
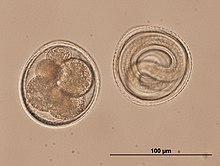
T. canis er en 8 til 18 cm lang nematode, der parasiterer (lever som en parasit) i tyndtarmen . Der afgiver de voksne hunner cirka 85 µm store, ikke-rillede æg, hvis skal er tyk og ru (svarende til en golfbold) og som kommer ud i omverdenen gennem ekskrementer. Perioden fra infektion til æglægning ( præpatens ) er tre til seks uger afhængigt af infektionsvejen og hundens alder. T. canis har ikke brug for en mellemvært til udvikling , men hundene kan inficeres via kollektive værter som gnavere og fugle . I kollektive værter (parateniske værter) er der ingen fuldstændig udviklingscyklus for parasitterne, men flere infektioner kan akkumuleres i dem infektiøse stadier. I princippet er der tre mulige infektionsveje for T. canis : Peroral infektion og transplacental og galactogen infektion, som er meget mere almindelig hos hvalpe .
- Den perorale infektion (infektion i munden) udføres ved registrering af æg fra miljøet eller fra larver fra samlende værter. Ormeægene er kun smitsomme omkring to uger efter, at de udskilles i afføringen i omverdenen. I løbet af denne tid udvikler det andet larvestadium (larve L2) sig inden i æggeskallen , som - ligesom larver fra samlende værter - frigives under fordøjelsen i tyndtarmen hos den nye vært. Disse larver gennembore tarmvæggen og nå den leveren via portåren , hvor de udvikles til larver L3. Dette bevæger sig gennem blodbanen til lungerne , hvor det hostes op og sluges igen. Først nu smelt larven til de voksne orme. Når de vandrer gennem kroppen, kan larverne også komme ind i andre organer, især skeletmusklerne og forårsage vævsdestruktion der. Ofte danner de imidlertid også vedvarende stadier i vævet (stadier hvor larverne fortsætter i vævet), som er vigtige for de to andre infektionsveje.
- I tilfælde af transplacental infektion (infektion via moderkagen ) migrerer de vedvarende larver L3 fra livmoderen gennem moderkagen og inficerer de ufødte hvalpe, mens de stadig er i livmoderen.
- Den galaktogene infektion (infektion via modermælken) hos hvalpene opstår ved udskillelse af rundormslarverne, som vedbliver i brystkirtlen, i modermælken i diende periode.

T. leonina er 6 til 10 cm lang, æggene er ca. 80 µm i størrelse og har tykke skaller. I modsætning til æggene fra T. canis har de en glat overflade. Infektion forekommer peroralt ved indtagelse af forurenet mad (forurenet) med æg eller via samlende værter såsom gnavere, fugle, krybdyr eller leddyr . Forberedelsestiden er 7 til 10 uger.
I en tysk undersøgelse blev T. canis påvist i en frekvens ( prævalens ) på 22,4%, T. leonina kun hos 1,8% af husdyrene. I Østrig viste T. canis sig at have en prævalens på 5,7% og T. leonina på 0,6%. Begge orme findes over hele verden. En tjekkisk undersøgelse viser store forskelle i prævalensen afhængigt af levevilkårene: 6% af hundene, der holdes privat i Prag, 6,5% af hundene i dyrehjem og næsten 14% af hundene fra landdistrikterne var inficeret med T. canis . Derudover blev der vist en stigning i prævalensen om efteråret. Husdyr i Belgien viste en gennemsnitlig infektionsrate på 4,4% for T. canis , dem fra større kenneler på op til 31%. Hos husdyr i Serbien kunne T. canis påvises hos 30% af dyrene, hos hyrde- og jagthunde i Grækenland i 12,8% og T. leonina hos 0,7% af dyrene. T. canis har en prævalens på 3,9% i Canada og 12,6% i det nordøstlige USA. I Australien blev T. canis fundet hos 38% af husdyrene hos dyr inden for det første leveår, selv hos 73%. I Brasilien blev T. canis fundet hos omkring 9% af husdyrene, i Thailand i 7,4%. I Nigeria blev T. canis observeret med en hyppighed på 9%, T. leonina kun hos en på 0,6%, i Gabon var 58,5% af husdyr hunde inficeret med T. canis . Hos ulve, der lever i den tempererede klimazone, er T. leonina imidlertid den mest almindelige tarmnematode (prævalens 74%). Undersøgelser af rødreven i det sydlige England viste en prævalens på 56% ( T. canis ) og 1,5% ( T. leonina ) i Danmark på 59 og 0,6%. Ræve repræsenterer således et naturligt reservoir af patogener .
Mens infektion med T. leonina kun meget sjældent forårsager kliniske symptomer som diarré, er den patogene virkning af T. canis signifikant stærkere. Hvalpe har en dårlig generel tilstand, lurvet pels, hæmmet vækst, skiftevis diarré og forstoppelse , en udspændt mave ("ormemaven") og anæmi . Komplikationer af T. canis- angreb, hvoraf nogle er dødelige, er tarmobstruktion på grund af en ormekugle, brud i tyndtarmen , lungebetændelse , leverbetændelse eller neurologiske symptomer på grund af omstrejfende vandrende larver i centralnervesystemet .
Den diagnose af orme i opkast kan ske uden særlige undersøgelser. Rundormangreb kan påvises relativt pålideligt ved mikroskopisk bevis for, at æggene fjernes fra fæces ved hjælp af flotationsprocessen , men først efter at den præpatente periode er udløbet.
Hookworm angreb (ankylostomyasis)


Der er to primære hageorm arter i hunde : Ancylostoma caninum og Uncinaria stenocephala . De parasiterer i tyndtarmen og forårsager anæmi og beskadiger tarmslimhinden ved at suge blod . Ormene har med ca. 5-15 mm kun ca. en tiendedel af rundormene, en krogformet vinklet forende (deraf navnet "hookworm") og en stor mundkapsel med skæreplader.
Kvinder af A. caninum giver æg på ca. 65 × 40 µm i størrelse, som allerede viser 4-10 spaltningsstadier, når de lægges . De er ovale og tyndhudede og kommer ud i omverdenen gennem fæces. Forberedelsestiden er to til fire uger. Larverne, der frigøres fra æggene, kan bore sig gennem huden ind i en ny vært ( perkutan infektion ) eller indtages oralt - hovedsageligt via foderværter såsom gnavere. Som med T. canis kan hvalpene også inficeres gennem modermælk ( galaktogen infektion ). Larverne, der er sovende i brystkirtlen, kan udskilles efter en enkelt tæveinfektion i en periode på op til tre diende perioder.
Æggene fra U. stenocephala ligner A. caninum , men har en større længdeakse på 85 × 45 µm. Infektion sker udelukkende gennem peroral indtagelse af larver via forurenet mad eller opsamlingsværter.
I Tyskland blev en infektionsrate på 8,6% bestemt, i Østrig på 0,1% for A. caninum og 0,2% for U. stenocephala . En tjekkisk undersøgelse fastslog en prævalens på 0,4% for begge krogeorme, en græsk undersøgelse på 2,8% sammen. I undersøgelser af husdyrhunde i Serbien og Nigeria kunne der konstateres hookworms i en fjerdedel af de undersøgte husdyrshunde , men U. stenocephala kun hos 0,4% af dyrene. I Gabon var begge hageorme detekterbare hos 35% af husdyrene. I Canada blev A. caninum kun fundet hos 1,3% af husdyrene sammenlignet med 12% i det nordøstlige USA. I en brasiliansk undersøgelse (37,8% af husdyrhunde) og en thailandsk undersøgelse (58,1% af husdyrhunde) var A. caninum faktisk den mest almindelige rundorm af alle. U. stenocephala har en prævalens på 26% i Australien . Hos ulve, der koloniserer tundraer , er U. stenocephala imidlertid den mest almindelige tarmnematode (prævalens 45%). Denne parasit er også meget almindelig hos røde ræve med en forekomst på 68%.
Mens angreb med U. stenocephala ofte kun forårsager mindre symptomer såsom diarré, kan angreb med A. caninum forårsage alvorlige kliniske billeder , især hos hvalpe. Blodig diarré, alvorlig udmattelse og anæmi kan forekomme, undertiden med et akut eller perakut forløb og pludselig død. I tilfælde af et kronisk forløb halter de unge dyr bagud i vækst, er sløv, viser manglende appetit, diarré og afmagring. Lungebetændelse forårsaget af vandrende larver er ret sjælden. En hookworm-angreb kan diagnosticeres ved at detektere æggene i fæces ved hjælp af en flotationsmetode.
Whipworm angreb (trichuriasis)
Den mest almindelige piskorm hund er Trichuris vulpis . Den er 4–8 cm lang, har en lang tynd front og en fortykket bagende. Æggene er citronformede, 80 × 40 µm i størrelse, brunlige, tykhudede og har fortykninger (”polskind”) ved polerne. De er ikke bange, når de lægger deres æg. Infektion opstår ved indtagelse af æg, der embryonerer (indeholdende en larve) i omverdenen. Forberedelsestiden er relativt lang efter 9-10 uger. T. vulpis parasiterer i tillægget og tyktarmen .
T. vulpis distribueres over hele verden. I Tyskland er omkring 4% af husdyrene smittet, i Østrig 3,1%. I Tjekkiet blev en prævalens på ca. 1% bestemt, i Grækenland på 9,6%. I en undersøgelse af husdyrhunde i Serbien var T. vulpis på den anden side den mest almindelige tarmparasit og blev fundet hos 47% af de undersøgte dyr. I det nordøstlige USA blev 15% af husdyrene angrebet. I Nigeria blev det kun fundet hos 0,5% af dyrene i en undersøgelse, i en anden undersøgelse var det signifikant mere almindeligt, i Gabon var 50% af husdyrene inficeret. I Brasilien var angrebsgraden 7%, i Thailand 20,5%. I Australien var T. vulpis den mest almindelige nematode hos voksne hunde med en prævalens på 41%. Forekomsten af angreb hos rød ræv er 0,5%.
Den sygdomsfremkaldende virkning af T. vulpis er moderat. Berørte hunde viser diarré, der er blodig og, hvis forløbet er mindre alvorligt, med slim. Dyrene taber sig, unge dyr halter bagud i vækst, og anæmi kan udvikle sig i tilfælde af alvorlig angreb. En pålidelig diagnose kan kun stilles via detektion i fæces ved hjælp af flotationsmetoden.
Dværg threadworm angreb (strongyloidiasis)
Infektion med dværgtrådormen Strongyloides canis kan forekomme ved indtagelse af smitsomme larver gennem modermælken oralt eller gennem aktiv penetration af larverne gennem huden. En autoinfektion, dvs. infektion af det samme dyr med larver, det udskilles, er mulig. S. canis parasiterer i tyndtarmen. Æggene er ca. 50 µm lange og indeholder den infektiøse larve, når de udskilles med fæces. En prævalens på 1,8% blev fundet for græsk hyrde- og jagthunde og 2% for husdyrshunde i Thailand.
Strongyloidiasis forårsager akut til kronisk diarré hos hvalpe og lejlighedsvis forstoppelse. Diagnosen kan stilles ved at detektere æggene i afføringen ved hjælp af en flotationsmetode.
Maveorm angreb
Maveorm ( Physaloptera spp.) Tilhører en verdensomspændende almindelig slægt af rundorm, som kan angribe slimhinden i mave og tolvfingertarm . Mandlige orme er op til 30 mm lange og hunner op til 40 mm lange. Æggene er ovale, tykafskallede, 55 × 32 µm i størrelse og indeholder allerede en larve. Larverne danner cyster i forskellige insekter - især biller , kakerlakker og crickets er mellemværter. Mus og frøer kan også inficere hunden som indsamlingsværter. Larverne klækkes i maven, fastgør sig direkte til slimhinden og smeltes ind i voksne (kønsmodne orme).
Maveormene forårsager skade på slimhinden i maven , hvilket fører til gastritis , blødning og kronisk opkastning. Kraftig angreb fører til vægttab og anæmi. Påvisningen af æggene i afføringen med flotationsmetoden er usikker, da de næppe flyder. Derfor er der ingen systematiske undersøgelser af hyppigheden af forekomst. En pålidelig diagnose kan stilles ved hjælp af gastrisk skylleprøver eller en gastroskopi .
Spiserør orm angreb
Den esophageal orm ( Spirocerca Lupi ) er en lys rød orm, der fører til knuder i esophageal væg. Mandlige orme måler ca. 40 mm, hunorme er ca. 70 mm lange. Infektion forekommer peroralt via mellemliggende værter (forskellige møg biller ) eller via paratenic værter, såsom høns, krybdyr og gnavere, der er inficeret ved at spise billerne. Larven vandrer gennem aortavæggen , hvor den forbliver i cirka tre måneder og derfra ind i spiserøret, hvor den udvikler sig til en voksen orm. Forberedelsestiden er fem til seks måneder. Æggene har cylindrisk form, har afrundede hætter, en tynd, glat væg og måler 30–37 × 11–15 µm. På tidspunktet for udskillelsen er larven allerede i dem.
Infektionen er almindelig i det sydlige USA såvel som i tropiske lande. I Gabon blev parasitten fundet hos en fjerdedel af husdyrene.
Orme kan lejlighedsvis forårsage aortaaneurisme, når de migrerer , men de berørte hunde er ofte asymptomatiske. I selve spiserøret forårsager S. lupi en granulomatøs vævsreaktion, som, hvis den ikke behandles, ofte degenererer og derefter danner forskellige ondartede tumorer . Ud over pladecellecarcinom og fibrosarkom kan spiserørscellerne også degenerere til osteosarkomer . Den tumorrelaterede masse i brystet kan også føre til hypertrofisk osteopati .
En angreb diagnosticeres ved en endoskopi. Dette viser en masse i spiserøret med parasitter på de vorte-lignende åbninger. Diagnosen kan bekræftes ved påvisning af embryonerede æg i fæces.
Leverinfektion af hårorm
Leverormen Capillaria hepatica forekommer hovedsageligt hos gnavere og kaniner , infektioner hos hunde er sjældne. Infektionen opstår ved at spise en gnavers lever. Klinisk forekommer symptomer som ubehag i maven og leverforstørrelse , som er forårsaget af migrationen af larverne gennem leveren og æglægningen. En pålidelig diagnose er kun mulig gennem en leverbiopsi .
Parasitose i luftvejene
Infektion med lungehårorm (Capillariasis)
Den lunge hairworm ( Capillaria aerophila , Syn:. Eucoleus aerophilus ) er op til 25 mm lang og parasiterer i de nedre luftveje . Æggene produceret af de kvindelige orme har to stangbælg og en farveløs til grønlig, granulær skal. De kommer ind i mave-tarmkanalen ved at hoste op og synke og til sidst ud i miljøet via afføringen. Infektion opstår ved indtagelse af mad eller vand, der er kontamineret med æg. Larverne klækkes i tarmen og passerer gennem blodbanen til lungerne. Forberedelsestiden er ca. 40 dage.
I Tyskland blev en infektionsrate på 2,3% bestemt hos husdyr, i Østrig var den 0,2%, i Tjekkiet var den 0,6% og i Canada var den 0,3%. Hos røde ræve i det sydlige England viste C. aerophila sig at have en prævalens på 0,2% sammenlignet med 74% i Danmark, hvilket gjorde lungehårorm til en af de mest almindelige rundorme og ræve til et vigtigt naturligt reservoir til infektion hos hunde. Andre rovdyr som ulve, vaskebjørnehunde, marterlignende hunde, los og katte angribes også.
Infektion med lungehårorm forårsager sjældent kliniske symptomer som hoste, nysen og næsepræst. Med sekundær bakteriel infektion kan der dog også forekomme dødelig bronkopneumoni. Diagnosen kan stilles ved at undersøge fæces ved hjælp af en flotationsmetode til æg eller ved at udføre en lungebiopsi .
Lungworm angreb
Lungormen Crenosoma vulpis er op til 1,6 cm lang og overføres indirekte ved at spise fra mellemliggende værter såsom snegle . Det koloniserer luftrøret og bronkierne. Hovedværten er rødreven , men hunde, vaskebjørnehunde, ulve og prærieulve angribes også.
C. vulpis blev fundet hos omkring 1% af husdyrene i Tyskland og hos hunde med lungesymptomer hos 2,4 til 6% af dyrene. En angrebsprocent på 3,2% blev bestemt i Canada. En prævalens på 17% blev bestemt for røde ræve i Danmark, og angrebshastigheder mellem 25 og 50% i Nordamerika - rødreven kan derfor betragtes som den vigtigste naturlige vært.
Klinisk er infektion karakteriseret ved en kronisk hoste og svarer til allergisk bronkitis .
Påvisning af C. vulpis i fæcesprøver med standardflotationsmetoden er relativt usikker; kun 28,5% af fæcesprøverne, der var positive efter larveemigrationsmetoden , førte også til et positivt resultat med standardmetoden.
Filaroididae
Filaroididae er en gruppe af rundorm, der parasiterer lunger og luftrør . De mest almindelige arter er Oslerus osleri ( syn . Filaroides osleri ), der parasiterer (oslerose) i luftrøret - især i luftrørsgaffelens område (Bifurcatio tracheae) - og Filaroides hirthi , som angriber lungevævet (filaroidose) . Mandlige O. osleri vokser til ca. 6-7 mm, hunner 10 til 13 mm. Æggene måler 80-120 × 60-70 µm, larven L1 er ca. 250 µm lang. F. hirthi er 2-3 mm (hanner) eller 7-13 mm (hunner), larven L1 er 240-290 µm lang. Andersonstrongylus milksi (Syn. Filaroides milksi ) er en sjælden repræsentant for Filaroididae hos hunde og ligner stort set Filaroides hirthi i udseende, livscyklus og klinisk billede .
Parasitterne forårsager små knuder i området for forgrening af luftrøret eller i lungevævet; døde orme kan også forårsage større granulomer . De kvindelige orme lægger æg, hvorfra larverne udklækkes, og de udvikler sig til voksne orme over fem multer. Infektionen sker enten gennem æg eller den første larve, hovedsagelig gennem direkte kontakt med spyt, næsesekretioner eller gennem genoplivet maveindhold, når hvalpene fodres af moderen. Infektion ved at spise afføring er mulig, men sjælden. Inficerede dyr kan også selvinficere, fordi ormene ikke har brug for en mellemliggende vært. Når den er inficeret, migrerer larven fra tarmen via blod eller lymfekar ind i blodbanen, hvorfra den når lungerne eller luftrøret og udvikler sig til en voksen orm. Forberedelsen for O. osleri er ti uger, for F. hirthi fem uger.
Repræsentanterne for Filaroididae forekommer over hele verden. O. osleri er især udbredt i ræve og andre hunde, der lever i naturen, infektioner hos husdyr er sjældne. F. hirthi blev først observeret hos hunde af Beagle- racen i USA, men forekommer nu over hele verden og også i andre hunderacer, men frem for alt hos Beagles, der holdes som laboratoriehunde.
Infektionen med O. osleri forårsager kronisk betændelse i luftrøret og bronchi med en stærk tør hoste og unormal åndedrætsstøj ved indånding. Sygdommen manifesterer sig normalt kun i slutningen af det første leveår og reagerer ikke på antibiotikabehandling. Samtidig forekomst af lignende symptomer hos moderen og hendes hvalpe er en indikation af en sådan infektion. Lejlighedsvis kan der forekomme angrebsløs åndenød under træning . Feber forekommer normalt ikke.
Til diagnose kan detektering af knuder ved hjælp af en lungeprøve , muligvis også på røntgenbilleder af brystet , såvel som larverne i lungeskyllevæske eller luftrørspindler anvendes. Påvisning af larver i fæces ved hjælp af flotationsmetoden er usikker, især da larverne kun udskilles i fæces uregelmæssigt og slet ikke under den relativt lange forberedelse.
Parasitose i blodbanen
Heartworm angreb (dirofilariasis)
Sygdomspatogenet er Dirofilaria immitis , en nematode 1 mm tyk og 20-30 cm lang. Det har brug for en mellemliggende vært for sin udvikling, en del af udviklingscyklussen - fra larvestadiet L1 til L3 (mikrofilarier) - finder sted i myg . Overførslen til hunden finder sted under sugende handling. Larverne L4 udvikler sig i subcutis og trænger ind i blodbanen og kaster huden der for at blive voksne orme. De voksne hjerteorme koloniserer højre halvdel af hjertet , lungevaskestammen og delene af vena cava nær hjertet . Kun omkring seks måneder efter infektion danner hunnerne igen mikrofilarier (larve L1), som kommer ind i mindre blodkar med blodet og indtages igen af myg, når de suger.
Indtil videre er mere end 70 mygarter blevet identificeret som vektorer, men ingen af dem er hjemmehørende i Centraleuropa. I Tyrkiet har 26% af husdyrantistoffer mod D. immitis ( seroprevalens ). Seroprevalens er 4% i det sydlige USA og 1% i de nordlige stater. I den australske delstat Victoria blev der påvist antistoffer mod D. immitis hos 8% af hunde over to år, i Sydkorea er seroprevalensen omkring 40%.
Inficerede dyr viser nedsat ydeevne, når de modne orme udvikler sig, dvs. kun ca. seks måneder efter infektion, og træt hurtigt. Højre hjertesvigt udvikler sig med overbelastning og forstørrelse af højre side af hjertet ( cor pulmonale ), som manifesterer sig i åndenød, hoste og dannelse af ødem . Lever- og nyresvigt kan også forekomme som et resultat af hjertesvigt .
Den serologiske påvisning af D. immitis antigen , som er meget specifik og følsom , anvendes fortrinsvis til diagnose . Derudover kan mikrofilarier påvises mikroskopisk via en blodprøve med berigelse eller lejlighedsvis med en simpel blodudstrygning . Dette bevis er dog begrænset til de faser, hvor mikrofilarier virkelig er til stede i stort antal i blodet, hvorfor de betragtes som mindre følsomme på grund af mange falske negative fund.
Angiostrongylose
Den franske hjerteorm ( Angiostrongylus vasorum ) er en parasit i lungevaskulær stammen, lungearterierne og højre ventrikel . De meget tynde (170–360 µm) lyserøde orme er 1,4 til 2 cm lange. Forberedelsestiden varierer mellem 35 og 60 dage. Parasitens vigtigste endelige vært er ræve, men også hunde, ulve, prærieulve, grævlinger, pampasræve, brasilianske ræve, krabberæve og små pandaer er også angrebet. Oprindeligt blev parasitten hovedsageligt fundet i Frankrig, Danmark og Storbritannien. Hyppigheden af angreb er steget markant over hele verden i flere år, så der er også endemiske besætninger i USA, Sydamerika, Australien og i den asiatiske del af Rusland. De seneste tal i Tyskland viser en infektionsrate på 7,4% hos dyr med lungesygdom eller 0,5% af den samlede hundepopulation.
Kvindelige orme lægger udifferentierede æg, som kommer ind i lungekapillærerne via blodbanen, hvor larver L1 klækkes og migrerer til de nedre luftveje. Larverne hostes op, sluges og udskilles med afføringen. Eliminationsperioden (patent) er op til fem år. I mellemliggende værter (forskellige arter af snegle ) udvikler de sig til den infektiøse larve L3. Efter indtagelse trænger larverne ind i tarmvæggen og udvikler sig i lymfeknuder i bughulen. Derefter når de den højre ventrikel af hjertet og lungearterierne ved blodvej, hvor de smelter til de voksne orme.
Larverne når lungearterierne ti dage efter peroral infektion og forårsager alvorlige lungeforandringer og blodpropper . Lejlighedsvis migrerer orme og larver også til andre organer ( larve migrans ).
Klinisk viser de berørte hunde en langsomt progressiv svækkelse af hjerte- og / eller lungefunktionen. Kronisk hoste, åndenød, nægtelse af at spise og vægttab, diarré, centralnervesymptomer og vævsblødning er også almindelige symptomer. Diagnosen stilles ved at detektere larver L1 i fæces ved hjælp af larveemigrationsmetoden. Den tidskrævende larvevandringsproces kan erstattes af serologisk (sandwich ELISA) eller PCR-påvisning. En hurtig test ( IDEXX Angio Detect ) er tilgængelig til serologisk påvisning .
Parasitoser i urinorganerne
Kæmpe angreb med nyreorm
Den gigantiske nyre orm ( Dioctophyme renale ;. Syn Dioctophyma renale ) er den største kendte parasitisk nematode og kan angribe den nyre og lejlighedsvis bughulen hos hunde . Kvindelige orme når længder på over en meter med en diameter på op til 12 mm; mandlige orme måler 20 cm med 6-8 mm. Begge køn har blodrød farve. Parasitten er udbredt over hele verden, men er sjælden i Europa. Det er ikke begrænset til hunden som den ultimative vært, men kan angribe de fleste pattedyr (inklusive mennesker). Reproduktion og udskillelse af æg kan kun forekomme, hvis den samme nyre er inficeret af både en kvindelig og en mandlig orm, og ormene allerede har perforeret nyrebækkenet. Æg udskilles i urinen gennem nyrebækkenet . Disse æg er ovale til cylindriske, gulbrune, tykvæggede, med en ru, knoppet overflade og 71-84 × 45-52 µm i størrelse. Æggene embryoner inden for to uger til tre måneder afhængigt af den omgivende temperatur og er derefter smitsomme over for mellemliggende værter.
Infektion sker via forbrug af mellemliggende værter eller parateniske værter, der indeholder cyster med larver fra parasitten. Mellemliggende værter er regnorme og akvatiske små børster , hvor larve L1 luger og udvikler sig til larve L3; Paratenische værter er ferskvandsfisk eller frøer , hvor larven L3 indkapsler sig i muskelkødet. Larven frigøres fra cysten i den endelige værts fordøjelseskanal, trænger ind i tarmvæggen og migrerer til leveren i ca. 50 dage . Derefter trænger den direkte gennem bukhulen ind i nyren, hvor den udvikler sig til en voksen orm. Den højre nyre påvirkes oftere end den venstre. Hos hunde forbliver parasitten dog ofte i bughulen, hvilket har mindre alvorlige konsekvenser for hunden end en angreb i nyrerne. Den inficerede nyre ødelægges langsomt af parasitten, som normalt også perforerer nyrebækkenet . Da æg meget sjældent optræder i urinen, er detektion af dem uegnet til diagnose. En nyreormangreb kan påvises ved hjælp af sonografi .
Urinblære hårorm angreb
Urinblæren hairworm Capillaria plica er 13 til 60 mm lange og koloniserer urinblæren , lejlighedsvis også ureter og nyrebækkenet. Æggene er 63–68 × 24–27 µm i størrelse, dækket og har en let ru overflade. De udskilles i urinen. Regnorme, hvor den smitsomme larve L1 udvikler sig, tjener som mellemværter. Infektionen sker ved modtagelse af de mellemliggende værter eller indirekte via kollektive værter.
I tilfælde af husdyrhunde i større kenneler kan op til tre fjerdedele af dyrene blive inficeret. En prævalens på 80% blev fundet hos røde ræve i Danmark, hvilket gjorde urinblærehårorm til den mest almindelige nematode, og ræve var et vigtigt naturligt reservoir til infektion hos hunde.
C. plica forårsager sjældent symptomer. Hvis det er mere alvorligt, kan det føre til en betændelse i urinblæren med vandladning og urininkontinens . Diagnosen kan stilles ved påvisning i urinen, men på grund af den lange præpatens ikke hos dyr yngre end otte måneder.
Parasitose i huden
Peloderma
Pelodera strongyloides (Syn. Rhabditis strongyloides ) er en normalt fritlevende nematode, der forekommer over hele verden i fugtigt, rodet organisk materiale, og hvis larve L3 lejlighedsvis angriber hundens hud. Infektion opstår ved direkte kontakt med materiale, der indeholder larver i fugtige og beskidte køjer (f.eks. Når der bruges fugtigt halm som strøelse). Det er uklart, om larverne kan trænge ind i sund hud; Under alle omstændigheder favoriserer eksisterende hudsygdomme og fugtige tilstande, der blødgør huden, infektionen. Larverne parasiterer på hårsækkene og de øverste lag af dermis .
Læsionerne er normalt begrænset til de dele af huden, der var i direkte kontakt med det infektiøse materiale, normalt underlivet, underbusten og ekstremiteterne. Den berørte hud er rødlig, moderat til svær betændt og delvist til fuldstændig hårløs. Der er udtalt kløe , som kan føre til yderligere hudlæsioner (skorpedannelse) og sekundære bakterieinfektioner . Normalt er sygdommen selvbegrænsende, også fordi hunden er en falsk vært for ormene . Diagnosen stilles ved at skrabe huden , hvor larverne, der måler ca. 600 × 38 µm, let kan genkendes med mikroskopet.
Dracunculosis
Dracunculus insignis er en nematode, der hovedsagelig forekommer i Nordamerika, og hvis vigtigste vært er vaskebjørne . Den medina orm ( D. medinensis ) forekommer i Asien og Afrika og påvirker en lang række pattedyr, herunder mennesker. Begge parasitter findes lejlighedsvis hos husdyr i disse områder. Infektion forekommer peroralt ved indtagelse af vand med tragte , der tjener som mellemværter eller indirekte ved indtagelse af kollektive værter såsom frøer. Larverne frigøres under fordøjelsen og bar sig gennem tarmvæggen. Kvindelige orme migrerer til det subkutane væv efter parring. Danner her de smertefulde og delvis fistulous pseudo cyster som brud ved kontakt med vand og slip ca. 0,5 mm lange larver. Diagnosen kan stilles ved at detektere larverne eller hunnormene i sådanne cyster.
Kutan dirofilariasis
Dirofilaria repens er en subkutan vævsparasit hos hunde. Myg fungerer som mellemværter og bærere. Det forekommer hovedsageligt i det sydlige, sydlige, østlige og vestlige Europa såvel som store dele af Asien, men spredes længere og længere til Nordeuropa og detekteres også i stigende grad i Tyskland.
D. repens angreb forårsager lejlighedsvis hudklumper, hævelser, kløe, bylder og hårtab, men fortsætter ofte uden kliniske symptomer. Syre-phosphatase- reaktionen kan anvendes til diagnose .
Sjælden filariasis
Acanthocheilonema reconditum (Syn. Dipetalonema reconditum ) forekommer i USA og Sydeuropa. Angrebsgraden i det sydlige Italien er 16,5%, i Grækenland op til 8%. Katten og hundelopperne fungerer som bærere. Ormene parasiterer hovedsageligt i det subkutane væv, en lille del af parasitterne findes også i indre organer.
Cercopithifilaria grassi (Syn. Dipetalonema grassi , Acanthocheilonema grassi ) forekommer i Sydeuropa, i Grækenland er ca. 1% af hunde angrebet. Bæreren er det brune hundemærke . Larverne (microfilariae) parasiterer i huden.
Dipetalonema dracunculoides (Syn. Acanthocheilonema dracunculoides ) forekommer i Afrika og Spanien. I Afrika er lusefluer hovedbæreren i Spanien, hvor udbredelsen er 1,5%, den brune hund kryds. Forberedelsestiden er 2-3 måneder.
Parasitose i øjnene
Thelaciosis
Thelaziosis er forårsaget af repræsentanter for slægten Thelazia . De er hvidlige rundorm, der er ca. 1,5 cm lange. Thelazia callipeda er især udbredt i Fjernøsten (Japan, Kina, Korea, Indien og Rusland), men er også en almindelig årsag til øjensygdomme i nogle regioner i Italien med angreb på op til 60%. Der har for nylig været et stigende antal individuelle sager i Schweiz og Frankrig. Indtil videre er der dokumenteret fire sager i Tyskland, hvoraf tre efter et ophold i Italien. Thelazia californiensis er almindelig i Californien. Disse rundormers biologi er ikke endeligt afklaret. Fluer mistænkes for at være vektoren, der indtager larver L1, og hvor udvikling op til smitsomme larver L3 finder sted.
Thelacia parasiterer på øjeæblet under den niktende membran og i tårekanalerne og forårsager konjunktivitis og øget lakrimation . Hindring af tårekanaler eller hornhindebetændelse kan også forekomme. Hvis angrebet er alvorligt, er ormene allerede synlige for det blotte øje. En pålidelig diagnose kan stilles ved påvisning af de orme eller deres larver i øjet vask prøver eller en biopsi af den tårekirtlen .
Onchocerciasis
Det forårsagende middel til onchocerciasis hos hunde er Onchocerca lupi . Sygdommen forekommer i Nordamerika og nogle europæiske lande (Grækenland, Ungarn), men er sjælden - 64 tilfælde er hidtil beskrevet. Ormene forårsager granulomatøse knuder i ærter til bønner i sclera , omkring øjnene og bindehinden. Under visse omstændigheder kan der udvikles en lymfoplasmacytisk betændelse i øjenens midterste hud . Diagnosen kan stilles ved at detektere ormene i knuderne.
Andre parasitoser
Trichinella angreb (Trichinellosis)
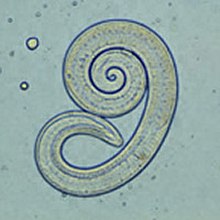
Trichinae ( Trichinella spp.) Er en slægt af rundorm, hvis larver vandrer ind i skeletmusklerne . Trichinae har ikke en verdensomspændende fase; infektionen opstår gennem indtagelse af rå muskelkød fra et inficeret dyr. I Europa er Trichinella spiralis mest udbredt hos husdyr, og Trichinella britovi og Trichinella nativa findes også hos hunde.
I tarmen fordøjes muskelkød og cyste kapsler, som frigiver larverne og invaderer foringen af duodenum og jejunum . Der udvikler de sig til voksne trikiner inden for cirka fire dage. Efter parring graver hunnormene dybere ned i slimhinden og lægger op til 1500 æg pr. Individ over fire til 16 uger. De udklækkede larver er ca. 100 mikrometer lange. De vandrer først ind i lymfekarene og derefter via portalvenen ind i det perifere blodkar system. Så snart de når musklerne, forlader de blodkaret og borer i en enkelt muskelfiber . Der vokser de hurtigt til en længde på 1 mm, indkapsler sig selv og begynder at tage den typiske krøllede form. Kapseldannelse i muskelvæv begynder omkring 15 dage efter infektion og afsluttes efter fire til otte uger - værtens kød er derefter smitsomt. Larverne kan forblive smitsomme i værtsmusklerne i årevis; de findes oftest i mellemgulvet , tungen , muskelmuskulaturen og interkostal muskler .
Der findes kun få data om hyppigheden af trichinae-infektion hos hunde. I Finland , som har en meget høj forekomst af trichinae hos vilde dyr, blev en infektionsfrekvens på mellem 4,9% og 8,6% fundet serologisk hos hunde . I den samme undersøgelse blev cyster i musklerne imidlertid kun fundet hos en ud af 102 hunde. I Kina, hvor hunde slagtes til konsum, blev trichinae fundet i gennemsnit 16,2% af slagtede hunde, hvor prævalensen varierede mellem 1,2 og 44,8% afhængigt af regionen.
Vaskebjørn rundorm angreb
Den vaskebjørn rundorm ( Baylisascaris procyonis ) er en relativ af hunden rundorm ( Toxocara canis , se ovenfor), som er specialiseret i vaskebjørne som den ultimative vært. I Tyskland er 70% af alle vaskebjørne inficeret med parasitten. Infektioner af hunden som endelig vært og ægstald er kendt fra USA, deres hyppighed har tendens til at stige og repræsenterer en betydelig risiko for zoonose , men angreb af hunden som en falsk vært ved indtagelse af æg er klinisk mere alvorlig . Larven fra vaskebjørnens rundorm vandrer ofte til den falske værts centralnervesystem , hvor den forårsager alvorlige neurologiske underskud, der kan være fatale.
Bekæmpe
De fleste infektioner er ret uskadelige for voksne hunde, da en patogen-vært-balance etableres, når immunsystemet er intakt . Men da nogle af dem kan forårsage sundhedsforstyrrelser, og nogle også udgør en potentiel fare for mennesker, er regelmæssige ormekurbehandlinger til hunde ret nyttige. Der er en højere risiko for infektion, især for hunde i større bedrifter, unge dyr, hunde i kontakt med andre dyr, jagthunde, omstrejfende og dyr, der fodres med rå kødprodukter. Den Europæiske Videnskabelige Counsel Companion Animal Parasitter (ESCCAP) - den europæiske sammenslutning af eksperter i parasitter hos hunde og katte - har derfor udstedt anbefalinger til bekæmpelse af infektioner med ormen. Disse er tilpasset regionale karakteristika af nationale veterinærspecialistforeninger. Sådanne retningslinjer findes også i USA og udstedes her af Companion Animal Parasite Council (CAPC).
Anbefalingerne, som sidst blev tilpasset i januar 2008 i overensstemmelse med ESCCAP-retningslinjerne for Tyskland, sigter mod at beskytte hunde " ... mod infektioner med orme og deres konsekvenser gennem professionel diagnostik, terapi og forebyggelse ". Målrettet kontrol anbefales til rundorm, krogorm og hjerteorm.
Hvalpe skal fra to uges alder hver 14. dag fravænning ormes profylaktisk. Ammende tæver skal også behandles første gang hvalpe bliver ormede. Sikker rundormsprofylakse kan kun opnås ved månedlig ormekur. ESCCAP anbefaler kun en månedlig cyklus til de ovennævnte risikogrupper og hunde med tæt kontakt med små børn. For de andre hunde tilrådes det at aforme ormen fire gange om året. En forøgelse eller reduktion i frekvensen af ormekur kan udføres gennem en individuel risikoanalyse og regelmæssige fæcesundersøgelser. Til behandling af rundorm er lægemidler baseret på emodepsid , fenbendazol , flubendazol , mebendazol , milbemycinoxim , moxidectin , pyrantel og selamectin godkendt til husdyrshunde i Tyskland . Disse lægemidler er bredspektrede anthelmintika og har også en virkning mod de fleste andre rundorm, der findes hos hunde. Derudover skal gødningen indsamles dagligt og bortskaffes sammen med husholdningsaffald. Regelmæssige rengørings- og desinfektionsforanstaltninger og flamming af kennelbunden sikrer, at de smitsomme æg og larver i umiddelbar nærhed elimineres eller i det mindste reduceres. Intet præparat er i øjeblikket godkendt til behandling af drægtige tæver, selvom eksperimentelle undersøgelser har vist, at brugen af selamectin eller emodepside under graviditet er effektiv til at forhindre infektion hos ufødte hvalpe.
Heartworm control spiller kun en rolle i Centraleuropa for hunde, der skal bringes til eller kommer fra Middelhavsområdet. Moxidectin, milbemycinoxim og selamectin er i øjeblikket godkendt til behandling og profylakse af hjerteormsygdom. Hertil kommer, når de rejser til hjerteorm endemiske områder, beskyttelse med insekt Myggemidler såsom permethrin eller deltamethrin er anbefales .
Fare for mennesker
Mennesker er falske værter for hundens rundorm Toxocara canis og hundens krogeorm ( Ancylostoma caninum ), dvs. larverne beskadiger inficerede organer, men de udvikler sig ikke til voksne orme. Begge er de vigtigste zoonotiske patogener blandt hundenematoder i Centraleuropa .
Infektionen med T. canis finder normalt sted via en smearinfektion ved peroral indtagelse af jord, der er forurenet med hundeavføring. Landmænd, gartnere, kloakarbejdere, dyrlæger og små børn (leger i sandkassen) er særligt udsatte. I Østrig blev der påvist antistoffer mod T. canis hos 3,7% af raske mennesker ( seroprevalens ) hos 44% af mennesker i udsatte erhverv. I Slovakiet havde sunde bloddonorer fra byområder en seroprevalens på 12% og dem fra landdistrikterne på 17%. I USA er 14% af befolkningen seropositive. En egyptisk undersøgelse fandt en seroprevalens på 18% hos raske voksne, og en tilsvarende høj infektionsrate blev fundet hos børn fra landdistrikter i Kina. I Jordan er seroprevalensen 11%, i Nigeria 30%, i det landlige Argentina 23%. Disse seroprevalenser indikerer imidlertid kun, hvor stor en procentdel af befolkningen der har oplevet en infektion. En sådan infektion behøver ikke nødvendigvis at føre til en sygdom, men kan afværges af immunsystemet uden symptomer. I sandkasser i store europæiske byer blev der fundet forurening med ormeæg i 10-100% af prøverne. Sygdomme forekommer primært hos børn og unge. Som viscerale larver ( Larva migrans visceralis ) kan hundens rundormorm angribe forskellige organer og forårsage alvorlig vævsskade der. Øjne , lunger , lever og centralnervesystemet påvirkes oftest .
Larverne af A. caninum kan trænge igennem huden, når de går barfodet over gulve, der er snavset med hundeavføring. Der forårsager de som vandrende larver ( Larva migrans cutanea , " hudmuld ") meget kløende rødme i huden. Passagerne boret af larverne er ofte synlige for det blotte øje. Sygdommen heler normalt spontant, men det kan tage måneder. Infektioner af denne art er sjældne i Centraleuropa, men en af de mest almindelige hudsygdomme i tropiske og subtropiske områder. Derudover kan A. caninum også udløse tarmbetændelse med tegn på en akut mave .
Af filariae er hjerteormen ( Dirofilaria immitis ) og Dirofilaria repens zoonotiske patogener. D. immitis forårsager sjældent sygdom hos mennesker, selvom ca. 20% af befolkningen i endemiske områder har antistoffer. Det meste af tiden er larverne indkapslet i lungerne. Mere end 400 sager er beskrevet for D. repens , hovedsageligt i Europa i Italien og Frankrig. Seroprevalensen hos mennesker er 68% i Italien og 22% i Frankrig. De voksne orme vandrer hovedsageligt ind i det subkutane væv, men de kan implantere sig selv i alle mulige organer.
Hunden spiller kun en rolle i spredningen af trichinella i nogle få regioner i verden. I Kina er forbrug af hundekød en vigtig infektionskilde for mennesker. Fire tilfælde af øjenormangreb (thelaciosis) er hidtil blevet beskrevet hos mennesker i Italien og Frankrig, men sygdommen er især udbredt blandt de fattigere befolkninger i Asien. Derudover kan hunde bidrage til spredning af ikke-værtsspecifikke parasitter såsom den kæmpe nyreorm eller medinaorm. Dog er den epidemiologiske betydning af hunde til infektioner hos mennesker endnu ikke undersøgt for disse parasitter.
litteratur
- Johannes Eckert et al. (Red.): Lærebog i parasitologi til veterinærmedicin. Enke-Verlag, 2. udgave 2008, ISBN 978-3-8304-1072-0 .
- Thomas Schnieder (red.): Veterinær parasitologi. Paul Parey, 6. udgave 2006, ISBN 3-8304-4135-5 .
- Peter F. Suter og Barbara Kohn (red.): Praktik på hundeklinikken. Paul Parey, 10. udgave 2006, ISBN 978-3-8304-4141-0 .
Individuelle beviser
- ↑ Barbara Hinney og Anja Joachim: Gastrointestinale parasitter hos hunde og katte. I: Kleintierpraxis 58 (2013), s. 256-278.
- ↑ a b c d Peter F. Suter og Reto Neiger : Ascarid angreb (rundorm). I: Peter F. Suter og Barbara Kohn (red.): Praktik på hundeklinikken. Paul Parey, 10. udgave. 2006, ISBN 978-3-8304-4141-0 , s. 718.
- ↑ a b c d e D. Barutzki og R. Schaper: Endoparasitter hos hunde og katte i Tyskland 1999-2002. I: Parasitol Res. 90 (2003), Suppl. 3, PMID 12928886 , s. 148-150.
- ↑ a b c d Heinrich Prosl: Hvor mange orme har hunden. Helminthologiske diskussioner 2006, Wien. ( PdF ( Memento fra 2. juni 2013 i internetarkivet ))
- ↑ a b c d S. Dubná et al.: Udbredelsen af tarmparasitter hos hunde fra Prag, landdistrikterne og krisecentre i Tjekkiet. I: Vet. Parasitol. 145 (2007), PMID 17169492 , s. 120-128.
- ^ E. Claerebout et al.: Giardia og andre tarmparasitter i forskellige hundepopulationer i det nordlige Belgien. Dyrlæge parasitol. 2008 (i pressen). PMID 19155136
- ↑ a b c A. Nikolić et al.: Høj forekomst af intestinale zoonotiske parasitter hos hunde fra Beograd, Serbien. I: Acta Vet Hung. 56 (2008), PMID 18828485 , s. 335-340.
- ↑ a b c d M. Papazahariadou et al.: Gastrointestinale parasitter hos hyrde- og jagthunde i Serres-præfekturet, Nordgrækenland. I: Vet Parasitol. 148 (2007), PMID 17573197 , s. 170-173.
- ↑ a b c d e f g T. Bihr og GA Conboy: Lungworm (Crenosoma vulpis) infektion hos hunde på Prince Edward Island. I: Can Vet J. 40 (1999), s. 555–559, PMC 1539780 (fri fuldtekst)
- ↑ a b c B.L. Blagburn et al.: Udbredelse af hundeparasitter baseret på fækale flotationer. I: Compend. Forts. Uddannelse. Øv. Vet. 18 (1996), s. 483-509.
- ↑ a b c d R.T. Blake og DJ Overend: Udbredelsen af Dirofilaria immitis og andre parasitter i hunde i byerne i det nordøstlige Victoria. I: Aust. Vet. J. 58 (1982) PMID 7115227 , s. 111-114.
- ↑ a b c S. Katagiri et al.: Udbredelse af hundens tarmparasitter og risikoopfattelse af zoonotisk infektion hos hundeejere i São Paulo State, Brasilien. I: Zoonoses Public Health 55 (2008), PMID 18811905 , s. 406-413.
- ↑ a b c d T. Inpankaew: Parasitiske zoonoser hos hunde i templer i Bangkok. I: Sydøstasiatiske J. Trop. Med. Public Health 38 (2007), PMID 17539273 , s. 247-255.
- ↑ a b c O.A. Sowemimo og SO Asaolu: Epidemiologi af intestinale parasitter hos hunde i Ibadan, Nigeria. I: J Helminthol. 82 (2008), PMID 18053301 , s. 89-93.
- ↑ a b c d B. Davoust et al.: Epidemiologisk undersøgelse af gastrointestinale og blodbårne helminter hos hunde i det nordøstlige Gabon. I: Onderstepoort J. Vet. Res. 75 (2008), PMID 19294992 , s. 359-364.
- ↑ a b H.L. Craig og PS Craig: Helminth-parasitter af ulve (Canis lupus): en artsliste og en analyse af offentliggjorte prævalensundersøgelser i befolkning i nærtisk og paleearktisk. I: J. Helminthol. 79 (2005), PMID 17169492 , s. 95-103.
- ↑ a b c d D.T. Richards et al.: Epidemiologiske undersøgelser af tarmhelminaparasitter hos røde ræve i landdistrikter og byer (Vulpes vulpes) i Det Forenede Kongerige. I: Vet Parasitol. 59 (1995), PMID 7571336 , s. 39-51.
- ↑ a b c d e f I. Saeed et al.: Helminths of red foxes (Vulpes vulpes) i Danmark. I: Vet. Parasitol. 139 (2006), PMID 16580775 , s. 168-179.
- ↑ a b c Peter F. Suter og Reto Neiger: Hookworm angreb, ankylostomyasis (Ancylostomum caninum, Uncinaria stenocephala). I: Peter F. Suter og Barbara Kohn (red.): Praktik på hundeklinikken. Paul Parey, 10. udgave, 2006, ISBN 978-3-8304-4141-0 , s. 718-719.
- ↑ a b U.S. Ugbomoiko et al.: Parasitter af betydning for menneskers sundhed hos nigerianske hunde: høj prævalens og begrænset kendskab til kæledyrsejere. I: BMC Vet. Res.4 (2008), PMID 19068110 , s.49 .
- ↑ a b Peter F. Suter og Reto Neiger: Trichuriasis, piskeormangreb (Trichuris vulpis, piskeorm). I: Peter F. Suter og Barbara Kohn (red.): Praktik på hundeklinikken. Paul Parey, 10. udgave, 2006, ISBN 978-3-8304-4141-0 , s. 718-719.
- ^ A b Larry P. Tilley og Francis WK Smith: Blackwells fem-minutters veterinærkonsulent, hunde og katte. J. Wiley, 4. udgave 2007, ISBN 978-0-7817-7360-7 ( online version ( Memento af 26. oktober 2009 i Internet Archive ))
- N TJ Nolan (2001): Canine Strongyloidiasis (PDF; 193 kB). International veterinærinformationstjeneste
- ↑ Merck Veterinary Manual: Physaloptera spp.
- ↑ James A. Clark: Physaloptera maveorm forbundet med kronisk vomition i en hund i det vestlige Canada. I: Kan. Vet. J. 31 (1990), s. 840. PMC 1480883 (fri fuldtekst)
- ↑ SK Theisen et al.: Physaloptera-infektion hos 18 hunde med intermitterende opkastning. I: Journal of the American Animal Hospital Association 34 (1998), PMID 9527433 , s. 74-78.
- ↑ The Merck Veterinary Manual: Spirocerca lupi
- ↑ Obduktion Show and Tell , Cornell Veterinary Medicine
- ↑ Barbara Kohn, Günter Schwarz, Peter F. Suter: Internship of the Dog Clinic , Georg Thieme Verlag, 2011 ISBN 978-3830411932 s. 678 (e- bog )
- ↑ P. Brander et al.: Capillaria hepatica i en hund og en pindsvin. I: Swiss Archive for Veterinary Medicine 132 (1990), PMID 2218471 , s. 365-370.
- ↑ a b Merck Veterinary Manual: Capillaria aerophila
- ↑ a b D. Barutzki: Nematodeinfektioner i luftvejene hos hunde i Tyskland. I: Tierärztl. Praxis Kleintiere 41 (2013), s. 326–336.
- ↑ a b c d e f D. Barutzki: Nematodeinfektioner i luftvejene hos hunde i Tyskland. I: Tierärztliche Praxis Kleintiere 41 (2013), s. 326-336.
- ↑ Dominique Grandjean et al.: Parasitisk rhinitis: Crenosoma angreb. I: Praktisk guide til hundeavlssygdomme. Aniwa Publications 2001, s. 111.
- ↑ a b c Josef Boch et al.: Filaroidosis og Oslerosis. I: Th. Schnieder (red.): Veterinær parasitologi. Georg Thieme Verlag, 2006, ISBN 9783830441359 , s. 491-492.
- ↑ Lesley G. King: Lærebog om luftvejssygdomme hos hunde og katte. Elsevier Health Sciences, 2004, ISBN 0721687067 , s. 551.
- ↑ RD Pinckney (2000): Canine Filaroides Infektion (PDF, 53 kB). International veterinærinformationstjeneste
- ↑ a b Dominique Grandjean et al.: Parasitisk rhinitis: Oslerus oslerus angreb. I: Praktisk guide til hundeavlssygdomme. Aniwa Publications 2001, s. 108-109.
- ↑ a b c Wendy A. Ware: Heartworm disease. I: Richard W. Nelson og C. Guillermo Couto (red.): Small Animal Internal Medicine. Mosby, 3. udgave 2003, ISBN 0-323-01724-X , s. 169-184.
- Yam M. Yaman et al.: Udbredelse af Dirofilaria immitis hos hunde fra Hatay-provinsen, Tyrkiet. I: J. Helminthol. 28 (2009), PMID 19173764 , s. 1-6.
- ^ D. Bowman et al.: Udbredelse og geografisk fordeling af Dirofilaria immitis, Borrelia burgdorferi, Ehrlichia canis og Anaplasma phagocytophilum hos hunde i USA: Resultater af en national klinikbaseret serologisk undersøgelse. I: Vet. Parasitol. 160 (2009), PMID 19150176 , s. 138-148.
- ↑ KH-sang: seroprevalens af hundedirofilariose i Sydkorea. Dyrlæge. Parasitol. 114 (2003), PMID 12788258 , s. 231-236.
- ↑ a b c Dieter Barutzki et al.: Angiostrongylus vasorum hos hunde: Aktuelle data om prævalensen i Tyskland og nye fund om profylakse og terapi. I: Parasiten Spezial 1/2010, s. 9-14.
- ↑ GA Conboy (2000): Canine Angiostrongylosis (fransk hjerteorm) (PDF; 36 kB). International veterinærinformationstjeneste
- ↑ Merck Veterinary Manual: Giant Kidney Worm ( Memento af 3. marts 2016 i internetarkivet )
- ↑ Nakagawa et al.: Giant Kidney Worm (Dioctophyma renale) infektioner hos hunde fra Northern Paraná, Brasilien. I: Veterinary Parasitology 145 (2006), s. 366-370. doi : 10.1016 / j.vetpar.2006.10.027 . PMID 17156927 .
- ↑ a b Dioctophyme renale . Animal Parasitology, Kansas State University
- ↑ The Merck Veterinary Manual: Capillaria plica
- ↑ a b D.F. Senior et al.: Capillaria plica infektion hos hunde. J. Am. Veterinærmed. Assoc. 176 (1980) PMID 7400020 , s. 901-905.
- ^ Merck Veterinary Manual: Pelodera Dermatitis
- S SAM Saari og SE Nikander: Pelodera (syn. Rhabditis) strongyloides som årsag til dermatitis - en rapport fra 11 hunde fra Finland. I: Acta Vet. Scand. 48 (2006): 18. PMID 16987397 , PMC 1569853 (fri fuldtekst)
- ↑ a b L. Langlais: Dracunculosis i en tysk hyrdehund. I: Kan. Vet. J. 44 (2003): 682. PMID 13677605
- ↑ B. Subrahmanyam et al:. Dracunculus medinesis (guinea orm) angreb i en hund og dens behandling med Flagyl. I: Indian Vet. J. 53 (1976), s. 637-639.
- ↑ Josef Boch et al.: Kutan Dirofilariosis. I: Thomas Schnieder (red.): Veterinær parasitologi. Paul Parey, 2006, ISBN 3-8304-4135-5 , s. 511.
- ↑ Bernhard Nocht Institute for Tropical Medicine: Hundens hudorm Dirofilaria repens påvist for første gang i tyske myg
- ↑ L. Keller et al:. Case rapport og gennemgang af litteraturen om kutan dirofilariasis. I: Tierärztliche Praxis Kleintiere 35 (2007), s. 31-34.
- ↑ a b c Josef Boch et al.: Sjælden filariasis hos hunde. I: Thomas Schnieder (red.): Veterinær parasitologi. Paul Parey, 2006, ISBN 3-8304-4135-5 , s. 511.
- ↑ a b c Dominique Grandjean et al.: Parasitisk konjunktivitis. I: Praktisk guide til hundeavlssygdomme. Aniwa Publications 2001, s. 144-145.
- ↑ a b Torsten Schottstedt: Okulær thelaciosis hos en hund. I: Kleintierpraxis 54 (2009), s. 160-163.
- ↑ D. Otranto et al.: Biology of Thelazia callipaeda (Spirurida, Thelaziidae) øjenorm i naturligt inficerede endelige værter. I: Parasitology (2004) 129 (5): 627-33, PMID 15552407
- ↑ G. og T. Binaciardi Otranto: Behandling af thelaziose hos hunde forårsaget af Thelazia callipaeda (Spirurida, Thelaziidae) ved anvendelse af en topisk formulering af imidacloprid 10% og moxidectin 2,5% . I: Veterinærparasitologi 129 (2005), PMID 15817208 , s. 89-93.
- ↑ Z. Egyed et al.: Morfologisk og genetisk karakterisering af Onchocerca lupi-inficerende hunde. I: Veterinærparasitologi 102 (2001), PMID 11731074 , s. 309-319.
- S T. Sréter og Z. Széll: Onchocercosis: En nyligt anerkendt sygdom hos hunde. I: Veterinary Parasitology 151 (2008), PMID 17951007 , s. 1-13.
- ↑ MK Zarfoss et al.: Okulær onchocerciasis hos hunde i USA: to nye tilfælde og en gennemgang af litteraturen. I: Vet. Ophthalmol. 8 (2005), PMID 15644101 , s. 51-57.
- ^ The Merck Veterinary Manual: Trichinellosis
- ↑ L. Oivanen et al.: Forekomsten af Trichinella-infektion hos husdyr i Finland. I: Veterinærparasitologi 132 (2005), PMID 15994010 , s. 125-129. PdF ( Memento fra 11. september 2011 i internetarkivet ). doi : 10.1016 / j.vetpar.2005.05.040 .
- ↑ ZQ Wang et al.: Epidemiologien for dyretrichinellose i Kina. I: Vet. J. 173. (2007), s. 243-244. doi : 10.1016 / j.tvjl.2005.08.002 . PMID 16162414 . (Anmeldelse).
- ↑ DD Bowman (2000): Baylisascaris procyonis hos hunde (PDF; 32 kB). International veterinærinformationstjeneste
- ↑ a b c d ESCCAP-anbefalinger til bekæmpelse af orme (helminter) hos hunde og katte. Tysk tilpasning af ESCCAP-henstillingen. ( pdf )
- ↑ a b Vetidata liste over ormeprodukter godkendt til hunde og katte i Tyskland ( pdf ( Memento fra 21. november 2008 i Internetarkivet ))
- ↑ Payne-Johnson M, Maitland TP, Sherington J, Shanks DJ, Clements PJM et al.: Effektivitet af selamectin administreret topisk til gravide og ammende hundehunde til behandling og forebyggelse af voksne rundorm (Toxocara canis) infektioner og loppe (Ctenocephalides felis felis) angreb i dæmningerne og deres hvalpe. I: Vet. Parasitol. 91 (2000), s. 347-358
- ↑ J. Tänzler: Forebyggelse af nyfødtinfektion hos hvalpe med Toxocara canis WERNER 1782 (Anisakidae) ved behandling af tæven under graviditet. Vet Med Diss, Hannover 2004
- ↑ H. Auer og H. Aspöck: nosology og epidemiologi af menneskelig toxocarosis - den aktuelle situation i Østrig. I: Wiener Klin. Wochenschr. 116 (2004), Suppl. 4, PMID 15683037 , s. 7-18.
- ↑ a b K. Havasiová et al.: En seroepidemiologisk undersøgelse af human Toxocara-infektion i Den Slovakiske Republik. J. Helminthol. 67 (1993) PMID 8132974 , s. 291-296.
- ↑ a b CDC: Toxocara Infection Roundworm Infection (Zoonotic). ( PdF )
- ↑ SN Antonios et al.: Seroprevalensundersøgelse af Toxocara canis hos udvalgte egyptiske patienter. I: J. Egypten. Soc. Parasitol. 38 (2008), PMID 19143141 , s. 313-318.
- ↑ ZJ Luo et al.: Påvisning af cirkulerende antigener og antistoffer i Toxocara canis-infektion blandt børn i Chengdu, Kina. J. Parasitol. 85 (1999), PMID 10219304 , s. 252-256.
- ^ MN Abo-Shehada et al.: Seroprevalens af Toxocara canis-antistoffer hos mennesker i det nordlige Jordan. I: J. Helminthol. 66: 75-78 (1992).
- ^ OO Ajayi et al.: Hyppighed af human toxocariasis i Jos, Plateau State, Nigeria. I: Mem. Inst. Oswaldo Cruz. 95 (2000), PMID 10733730 , s. 147-149.
- ↑ P. Chiodo et al.: Relaterede faktorer til human toxocariasis i et landdistriktssamfund i Argentina. Mem Inst Oswaldo Cruz. 101 (2006), PMID 16951810 , s. 397-400.
- Schn Thomas Schnieder: Bekæmpelse af rundormangreb hos hunde effektivt - beskytter mennesker. I: Veterinärspiegel 2/2009, s. 76-79.
- ^ MA Brenner og MB Patel: Kutan larvevandring: det krybende udbrud. Cutis. 72 (2003), PMID 12953933 , s. 111-115.
- ↑ MA Bahgat et al.: Evaluering af Ancylostoma caninums rolle hos mennesker som årsag til akut og tilbagevendende mavesmerter. I: J. Egypten. Soc. Parasitol. 29 (1999), PMID 12561926 , s. 873-882.
- ↑ J. Croese et al.: Human enterisk infektion med hunde krogeorme. I: Ann. Praktikant. Med. 120 (1994) PMID 8304653 , s. 434-435.
- ↑ S. Pampiglione et al:. Humant Dirofilariosis grund Dirofilaria (Nochtiella) repens: En gennemgang af verdens litteratur. I: Parasitologia 37 (1995), PMID 8778658 , s. 149-193.
- ↑ J. Cui og Wang ZQ: Udbrud af human trichinellose Forårsaget af forbrug af hundekød i Kina. I: Parasite 8 (2001), Suppl. 2, PMID 11484389 , s. 74-77.
- ↑ D. Otranto og M. Dutto: Human thelaziasis, Europa. I: Emerg. Inficere. Dis. 14 (2008), PMID 18394285 , s. 647-649.
- ↑ J. Shen et al.: Human thelaziosis - en forsømt parasitisk sygdom i øjet. I: J. Parasitol. 92 (2006), PMID 16995411 , s. 872-875.