Hund mast celle tumor
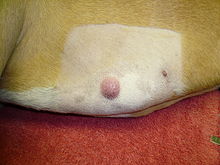

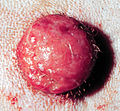
Den mastcelletumor i hunde er en nydannelse ( neoplasi ) oprindelse fra mastceller i hunde , som forekommer hovedsageligt i huden og subkutant væv. Mastcelletumorer er ikke kun ekstremt almindelige hos hunde, men har også tendens til at udvikle ondartede forløb meget oftere end hos andre dyrearter. Den gennemsnitlige overlevelsestid for maligne tumorer er kun fire måneder, mens det for godartede tumorer er mere end to år.
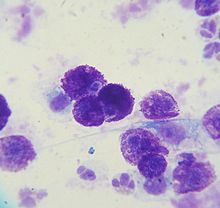
Mastceller er celler i immunsystemet, der spiller en rolle i det medfødte immunrespons . De producerer et antal biologisk aktive stoffer, især histamin . Mastcelletumorer udgør cirka en femtedel af alle hudtumorer hos hunde. De vises som klumper eller hævede pletter, og sår og blødning i mave og tolvfingertarm forekommer hos omkring en femtedel af de berørte dyr . Dattertumorer i ondartede mastcelletumorer forekommer primært i lymfeknuder , lever , milt og knoglemarv . Enhver klump i huden eller subkutant væv kan være en mastcelletumor. Detektion er kun mulig ved at tage væv med en fin kanyle ( fin nålebiopsi ) med efterfølgende farvning og mikroskopisk undersøgelse ( cytodiagnostics ).
Selvom kategoriseringen efter de kliniske symptomer og cellestrukturen i cytodiagnostik giver indikationer for den biologiske adfærd (godartet eller ondartet) og dermed udsigten til en kur, er denne tumorsygdom uforudsigelig og bør behandles på et tidligt stadium. Den valgte metode er komplet kirurgisk fjernelse , som også kan kombineres med stråling eller kemoterapi . Tumorer, der ikke kan fjernes kirurgisk eller kun ufuldstændigt, kan også behandles med tyrosinkinasehæmmere .
Mastcelletumorer er også mere almindelige hos husdyrheste , fritter og huskatte , men de opfører sig normalt godartede i disse dyrearter. Mastcelletumorer er meget sjældne hos andre dyrearter og hos mennesker.
Mastcelle

Mastceller ( mastceller ) er celler fra den immunsystemet og udgør et vigtigt led mellem medfødte og adaptive immunrespons . De stammer fra precursorceller i knoglemarven og vandrer som umodne celler i mange væv , især i dem med tæt kontakt med uden for verden, hvor de differentierer .
Modne mastceller er afrundede celler i bindevævet , hvis cytoplasma indeholder granuler med en anden farvningsadfærd ( metakromasi ). Granulerne opbevares histamin , heparin og cytokiner, såsom tumornekrosefaktor-a . På celleoverfladen, har mastceller bindingssteder ( receptorer ), hvoraf to er funktionelt vigtigst: Den stamcellefaktor receptor ( tyrosinkinase KIT ) regulerer den differentiering , reproduktion , aktivering og levetid af mastceller ved at binde stamcellefaktoren . Den immunglobulin receptor FcsRI ( høj affinitet IgE-receptoren ) binder immunglobulin E (IgE) med høj bindingsstyrke ( affinitet ). Ikke kun stamcellefaktoren, men også et antal interleukiner og ultraviolet stråling fører til aktivering og multiplikation af mastceller. Når mastceller aktiveres, frigives inflammatoriske mediatorer , cytokiner og proteaser enten fra granulerne eller er nydannede og frigives på kort tid.
Funktionen af mastceller i allergier er blevet undersøgt bedst , de er også involveret i autoimmune sygdomme og i intensiveringen af de inflammatoriske reaktioner i bakterielle infektioner . På den anden side kan mastceller også have antiinflammatoriske virkninger, da de beskytter mod skadelige faktorer som bakterier og parasitter . Derudover kan mastceller takket være deres store repertoire af biologisk aktive stoffer bidrage til udvikling og vækst af andre hudtumorer.
Forekomst og oprindelse
Mastcelletumorer hos hunde forekommer hovedsageligt i huden og subkutant væv. De findes meget sjældent i indre organer som tyndtarmen , mundslimhinden , næseslimhinden eller bindehinden . Ca. 20% af alle hudtumorer og 6% af alle tumorer hos hunde er mastcelletumorer. De forekommer oftere i nogle racer: tyske boksere og beslægtede korthårede racer , golden retrievere , beagles , irske settere , gravhunde og Berner bjerghunde . Der er ingen afhængighed af dyrets køn. Gennemsnitsalderen for berørte hunde er otte år, men mastcelletumorer kan udvikles hos hunde så tidligt som fire måneder eller i en meget gammel alder.
Hos mennesker kendes et antal mutationer og kromosomændringer, der fører til den patologiske multiplikation af mastceller ( mastocytoser ). Mutationer i genet for stamcellefaktorreceptor (c-KIT) fører til en forlænget cellelevetid og et øget antal nye mastceller. Den D816V- mutationen er den mest almindelige af disse c-kit mutationer og forekommer i 80% af patienter med mastocytose. Men der er også mastocytosepatienter uden ændringer i stamcellefaktorreceptoren. I alt kendes mere end 20 kromosomændringer hos mennesker, der kan føre til mastocytose, hvor kromosomer 2 , 7 , 12 , 13 , 14 og X hyppigst påvirkes.
Ændringer i c-KIT synes også at spille en rolle hos hunde. Både øget genekspression og en mutation med phosphorylering af stamcellefaktorreceptoren, som fører til aktivering uden binding af stamcellefaktoren ( liganduafhængig ), kan forekomme. I mellemtiden er sådanne mutationer kendt mere end 30, hvoraf den mest almindelige en dobbelt ( tandem mutation ) af exon 11 er, at retten på indersiden af cellemembranen fraktionen liggende (juxtamembran domæne ) af stamcellefaktor receptor kodet . Mastcelletumorer uden c-KIT-mutation forekommer også hos hunde; i modsætning til amerikanske undersøgelser blev der næsten ikke påvist nogen relevante c-KIT-mutationer i mastcelletumorer hos tyske hunde. Hvorvidt dette var utilsigtet eller metodisk, eller om det afspejler genetiske forskelle i avlslinjerne, skal afklares gennem yderligere undersøgelser. Årsagerne til den øgede forekomst af mastcelletumorer hos hunde er stadig uforklarlige, formodentlig er der flere årsager (multifaktoriel forekomst).
Klinisk billede

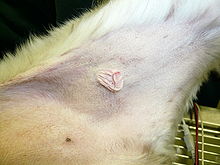
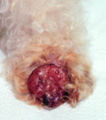
Mastcelletumorer i huden fremstår som knuder ( papler ), hævede pletter ( plak ) eller knuder ( nodus ), som kan gå i opløsning på overfladen og mavesår . Deres konsistens spænder fra blød til grovknude. Rødme og kløe kan forekomme lokalt ( Dariers tegn ). Lejlighedsvis forekommer satellitknuder , det vil sige, at tumoren spredes via lymfekar i nærliggende hudområder; i omkring 10% af tilfældene dannes flere mastcelletumorer fra starten ( primær mangfoldighed ).
Mastcelletumorer kan danne dattertumorer ( metastaser ) i de (regionale) lymfeknuder, der er ansvarlige for området såvel som i andre organer såsom lever , milt og knoglemarv ; andre steder er meget sjældne. I godartede mastcelletumorer er metastasehastigheden under 10%, hos ondartede er den over 50%.
Selv uden dannelsen af dattertumorer kan en mastcelletumor udløse alvorlige generelle lidelser ( paraneoplastisk syndrom ). Disse udløses af frigivelsen af inflammatoriske mediatorer og cytokiner. Dannelsen af heparin af mastcellerne kan føre til en øget tendens til blødning som et resultat af produktionen af fibroblasthæmmende cytokiner (især FGF-2 ), der interfererer med sårhelingsprocesser . Cirka en femtedel af hunde med en mastcelletumor udvikler modvilje mod at spise, kaste op , tarry afføring og anæmi som et resultat af mavesår eller tolvfingertarmsår ; sådanne mavesår opdages endda hos over 80% af patienter i obduktion . Cirka 80% af hunde med sådanne sår aflives på grund af deres dårlige generelle tilstand . I alvorlige tilfælde kan disse sår føre til en livstruende mave- eller tarmperforationsledning . Derudover kan det også føre til et klinisk billede, der minder om en ondartet sygdom i det bloddannende system. Denne systemiske mastocytose observeres hovedsageligt hos dyr, hvorfra en mastcelletumor tidligere er blevet fjernet. Træthed, uvillighed til at spise, opkastning, vægttab, bleghed og forstørrelse af lever og milt forekommer.
Ifølge det kliniske billede klassificeres mastcelletumorer i fire faser i henhold til kriterierne fra Verdenssundhedsorganisationen :
| Scene 1 | en tumor begrænset til huden uden lymfeknudeinddragelse a) uden generelle |
| Trin 2 | en tumor begrænset til huden med lymfeknude -metastase a) uden generelle |
| Trin 3 | Flere tumorer eller store enkelttumorer, der vokser infiltrativt med eller uden lymfeknudeinddragelse a) uden generelle |
| Trin 4 | Tumor med fjern metastase eller tilbagefald med metastase |
Diagnose
Et blik eller en berøringsdiagnose er ikke mulig, da hverken udseende eller konsistens tillader en forskel fra andre hudtumorer.
Det valgte diagnostiske middel er fin nålebiopsi , da tilstrækkelige celler kan opnås fra mastcelletumorer. I det cytologiske præparat kan mastceller differentieres relativt let fra andre celletyper på basis af deres granuler , skønt det skal bemærkes, at visse hurtige farvningsopløsninger kun pletter mastcellegranuler upålideligt, og celler af dårligt differentierede mastcelletumorer kan indeholde meget få granuler.
I blodtal tælles ændringer kun sjældent, lejlighedsvis forekommer der en stigning i en undertype af hvide blodlegemer ( eosinofili ). Ved systemisk mastocytose er et fald i antallet af hvide blodlegemer ( leukopeni ) almindeligt. Mastceller, der cirkulerer i blodet, observeres for det meste ikke.
Ifølge det histopatologiske cellebillede er mastcelletumorer hos hunde opdelt i forskellige kvaliteter. Den mest udbredte klassificering af mastcelletumorer er baseret på ordningen fra Patnaik og kolleger fra 1984:
| Tumor klasse 1 (godt differentieret) |
|
| Tumor klasse 2 (moderat differentieret) |
|
| Tumor klasse 3 ( anaplastisk ) |
|
En undersøgelse fra 2011 sætter dog spørgsmålstegn ved denne klassificering. Identiske præparater fra 95 mastcelletumorer, hvoraf sygdommens resultat var kendt, blev sendt til 28 patologer i 16 forskellige institutioner. Mens aftalen mellem de forskellige efterforskere var 75% for grad 3-tumorer, var den mindre end 63% for grad 1 og 2, og de prognoser, der blev afledt af dette, viste ringe overensstemmelse med udfaldet af sygdommen. Kiupel og kolleger foreslog derfor et nyt system, der kun indeholder to karakterer: lav og høj grad . Tumorer vurderes som høj kvalitet, hvis et eller flere af følgende kriterier er opfyldt i ti synsfelter med høj forstørrelse (40x mål ):
- mindst syv mitoser
- mindst tre flerkernede celler (tre eller flere cellekerner)
- mindst tre unormale kerner (fordybninger, segmentering, uregelmæssig form)
- Kerneudvidelse ( karyomegali , kernediameterne på 10% af mastcellerne varierer mindst to gange).
Den gennemsnitlige overlevelsestid hos dyr med højgradig mastcelletumor var fire måneder sammenlignet med to år hos dyr med lavgradig mastcelletumor. Derudover var gentagelser og metastaser signifikant mere almindelige i mastcelletumorer af høj kvalitet . Derudover synes der at være en forbindelse mellem typen af c-KIT-mutation på den ene side og den biologiske adfærd eller graden af tumor på den anden. Den immunhistokemiske påvisning af celledelingsmarkører såsom Ki-67 eller den argyrofile nucleolus- organisatorregion (AgNOR) viser også korrelationer med mastcelletumorers biologiske opførsel. Mere end 23 Ki-67-positive celler pr cm 2 eller mere end fire AGNOR pr cellekerne betragtes som prognostisk ugunstige.
Den biologiske opførsel af mastcelletumorer er meget variabel så hos hunde og kun delvis forudsigelig, så hos hunde er udtrykket mastcelletumor udtrykkene mastocytom (godartet) og Mastosarkom at foretrække (ondartet). Det kliniske stadium, histopatologisk kvalitet, c-KIT-ekspressionsmønster og celledeling markører giver spor, men tillader ikke nøjagtige udsagn. Tilsyneladende er mastcelletumorer hos hunde molekylært heterogene neoplasmer. Mastcelletumorer i den tyske bokser, en af de racer, der oftest er ramt, viser normalt et godartet forløb. Tumorens placering synes også at spille en rolle. Mastcelletumorer i tæer, perineum , lyske og slimhinder er mere tilbøjelige til metastaser end i andre regioner. I modsætning hertil har mastcelletumorer i bindehinden ringe tendens til at gentage sig eller metastaser, uanset grad. Naturligvis kan epigenetiske faktorer , de umiddelbare miljøforhold ( mikromiljø ), dannelsen af nye blodkar og vækstfaktorer påvirke biologisk adfærd.
Enhver anden hudtumor hos hunden kan anvendes til differentiel diagnose: i huden især histiocytomer , basaliomer , melanomer og T-celle lymfomer , i det subkutane væv, især lipomer , hæmangiopericytomer og hæmangiosarkomer . Afgrænsningen af disse tumorer udgør imidlertid næppe nogen problemer i cytodiagnostika.
behandling
Selvom kategoriseringen efter de kliniske symptomer og cellestrukturen i cytodiagnostik giver indikationer for den biologiske adfærd, forbliver en mastcelletumor uforudsigelig og kan klassificeres som potentielt ondartet. Den behandling fremgangsmåde til første valg er den tidligst mulige kirurgisk fjernelse af tumoren. Ledsagende kemoterapi og stråling kan være nødvendigt, især hvis fuldstændig fjernelse ikke er mulig eller usikker af anatomiske årsager. I tilfælde af inoperable tumorer kan et behandlingsforsøg med tyrosinkinasehæmmere foretages. Generelt er udsigten til en kur bedst i veldifferentierede mastcelletumorer ( lav kvalitet eller grad 1) og hos dyr uden generelle symptomer (underfaser a). Hos unge hunde (<1 år) er prognosen også bedre end hos ældre hunde.
kirurgi
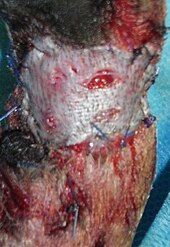
Kirurgisk fjernelse ( resektion ) skal udføres så tidligt som muligt, dvs. før lymfeknuder eller endda andre organer påvirkes (trin 1). Mastcelletumorer har en pseudokapsel lavet af komprimerede tumorceller og normalt fine forlængelser i det omgivende væv, der strækker sig ud over det håndgribelige tumorvæv. Af denne grund anbefales en sikkerhedsafstand på ca. 3 cm over den berørbare kant. Fjernelsen finder sted, selv med mastcelletumorer i det subkutane væv , med hele huden og i dybden inklusive den subkutane fascia . Det kan være svært at lukke den resulterende hudfejl på lemmerne, så en hudtransplantation også kan være nødvendig. Biopsier bør tages fra margenen og det resterende dybe væv (tumorbed) for at kontrollere for tilstedeværelsen af resterende tumorvæv .
Disse grundlæggende tumorkirurgiske regler kan ikke altid implementeres fuldt ud, især på lemmerne, fordi dette ville resultere i tab af nerver , kar og sener , så amputation også skal overvejes. Under visse omstændigheder forsøg kan fremstilles ved hjælp af Hl og H₂ receptorantagonister før operationen for at reducere tumorstørrelsen. Selvom fjernelsen af tumorcellerne er ufuldstændig for at reducere antallet af tumorceller ( cytoreduktiv resektion ), er indgivelsen af disse aktive stoffer indikeret, da interventionen kan føre til degranulering af mastcellerne og dermed frigivelse af inflammatoriske faktorer.
I tilfælde af veldifferentierede mastcelletumorer, der er mindre end 5 cm, er udsigten til heling ( prognose ) meget god med korrekt kirurgisk fjernelse, men dårlig i tilfælde af gentagelser . Planlægning af den kirurgiske tilgang under den indledende procedure er derfor af afgørende betydning. Med tumorer mindre end 2,5 cm er overlevelsestiden meget høj, selv med højgradige tumorer.
strålebehandling
Den strålebehandling anvendes hovedsageligt ikke helt aftagelige mastcelletumorer som tillægsbehandling og betragtes som et stof valg. Mastceller er meget følsomme over for ioniserende stråling . I grad 2 mastcelletumorer viser forskellige undersøgelser sygdomsfri sygdom hos ca. 95% af patienterne efter et år og hos ca. 90% af patienterne mellem andet og femte år efter behandling. I en undersøgelse var et års overlevelsesrate for grad 3-tumorer uden lymfeknudeinddragelse 71%. Strålebehandling kan også bruges som en palliativ behandling , da det normalt fører til en betydelig krympning af tumoren. En undersøgelse af kortdistance strålebehandling for grad 2 og 3 tumorer efter kirurgisk fjernelse viste også god succes og god tolerance.
kemoterapi
Til kemoterapi anvendes forskellige aktive ingredienser. Glukokortikoider har en direkte hæmmende virkning på multiplikationen af mastceller. Direkte injektion i tumoren anbefales ikke længere; systemisk administration er på den anden side ofte kombineret med administration af cytostatika . Vinca-alkaloider såsom vinblastin , cyclophosphamid , hydroxycarbamid , doxorubicin , mitoxantron og L-asparaginase anvendes som cytostatika , selvom kombinationer af forskellige aktive ingredienser er mere lovende. Ifølge det europæiske konsensuspapir fra 2012 er kemoterapi altid indiceret, hvis tumoren allerede har spredt sig i kroppen, eller hvis hverken reoperation eller stråling er mulig i tilfælde af ufuldstændig kirurgisk fjernelse.
Hydroxycarbamid reagerede i en undersøgelse hos 28% af de behandlede hunde, 4% (to dyr) viste en fuldstændig heling ( fuldstændig remission ). Bivirkninger var hovedsageligt ændringer i blodtalet, såsom anæmi og neutropeni . Kombinationen af hydroxycarbamid med prednisolon i ufuldstændigt fjernede grad 2-tumorer resulterede i to tilfælde i dødsfald fra leversvigt ; af de resterende hunde overlevede alle det første og 77% det andet år. Med kombinationen af hydroxycarbamid, vinblastin og prednisolon blev der opnået en responsrate på 65% for mastcelletumorer, der ikke kunne fjernes eller ikke kunne fjernes fuldstændigt; den gennemsnitlige overlevelsestid var signifikant højere for grad 2-tumorer end for grad 3 tumorer (954 versus 190 dage). Bivirkningerne (neutropeni, stigning i leverværdier ) var moderate.
Tyrosinkinasehæmmere

I mellemtiden er der med tyrosinkinasehæmmere aktive ingredienser, der specifikt arbejder på stamcellereceptoren i mastcellerne. Siden 2009 er to tyrosinkinasehæmmere - masitinib (handelsnavn Masivet ) og toceranib (handelsnavn Palladia ) - blevet godkendt i EU til behandling af mastcelletumorer hos hunde .
Masitinib er godkendt til behandling af inoperable mastcelletumorer i klasse 2 og 3 (eller high-grade) med c-KIT-mutation. De vigtigste bivirkninger er opkastning, diarré, neutropeni , anæmi og proteinuri , men disse er normalt milde. I en undersøgelse af hunde med grad 2 og 3 tumorer uden metastaser steg den gennemsnitlige overlevelsestid fra 75 til 118 dage, da den aktive ingrediens blev brugt til indledende behandling til 253 dage.
Toceranib har flere angrebspunkter ( multitarget lægemiddel ): Det virker ikke kun på stamcellereceptoren, men også på receptorer for den vaskulære vækstfaktor (VEGF) og blodpladevækstfaktoren (PDGF) og kan derfor også bruges i mast celletumorer uden c-KIT-mutation. Bivirkningerne svarer til masitinibs bivirkninger, men er meget almindelige og er alvorlige hos over en tredjedel af dyrene.
Der har også været positive erfaringer med tyrosinkinasehæmmeren imatinib, som er godkendt til brug i humanmedicin .
Tigilanoltiglat
Siden 2019 har der været en ny behandlingsmulighed ved at injicere tigilanoltiglat (EBC-46), en aktiv ingrediens fra rødtræfrugten , direkte i tumoren. En undersøgelse var i stand til at opnå en fuldstændig tumorremission hos 75% af dyrene med en enkelt injektion, som i 93% forblev uden gentagelse. Med en to-gang injektion steg succesraten til 88%. Et lægemiddel (handelsnavn Stelvonta , Virbac ) til behandling af mastcelletumorer er i mellemtiden blevet godkendt i EU .
Mastcelletumorer af andre arter
Mastcelletumorer hos mennesker
| Klassificering i henhold til ICD-10 | |
|---|---|
| C94.3 | Mastcelle leukæmi |
| C96.2 | Ondartet mastcelletumor Ondartet mastocytose |
| Q82.2 | medfødt mastocytose urticaria pigmentosa |
| ICD-10 online (WHO version 2019) | |
En patologisk spredning af mastceller kaldes mastocytose i humanmedicin . Den øgede opbevaring af mastceller i huden ( kutan mastocytose ) er en sjælden sygdom med en forekomst på mindre end ti nye tilfælde pr. 1 million indbyggere. Den mest almindelige form for disse hudmastocytoser er godartet urticaria pigmentosa ("pigmentnældeafhængighed"). Andre organer er også påvirket hos omkring 20% af de små børn, mens tallene for voksne varierer mellem 40 og 90%.
Isolerede mastcelletumorer som hos hunde er meget sjældne hos mennesker. Godartede mastcelletumorer ( mastocytom , mastcelle nevus ) udvikler sig normalt hos små børn under to år og fremstår som enkelt eller flere, rødlige eller rødbrune hævede pletter eller knuder på huden. Som reaktion på mekaniske stimuli eller spontant kan de svulme op som nældefeber ( Dariers tegn ) og forårsage kløe . Der er ingen tendens til degeneration eller involvering af andre organer. Mastocytomer går normalt tilbage uden behandling, men det kan tage flere år. Malign mastcelletumorer ( mastcelle sarkomer ) er ekstremt sjældne i mennesker og er kontroversielle som selvstændig kliniske billede.
Mastcelletumorer i andre dyrearter
Mastcelletumorer er også relativt almindelige hos heste, katte og fritter, omend sjældnere end hos hunde. Hos tamme heste forekommer de hovedsageligt hos ældre dyr i hoved- og nakkeområdet såvel som på underbenene. Gentagelsesfrekvensen er lav med korrekt kirurgisk fjernelse. Hos huskatte er mastcelletumorer i huden for det meste godartede. En histologisk klassificering som hos hunden har ikke vist sig at være nyttig. Kirurgisk fjernelse er også den valgte behandlingsmetode for katte, og hvis resektionen er ufuldstændig, kan den også kombineres med stråling. Hvis mastcelletumorer er talrige, kan palliativ behandling med glukokortikoider også forsøges. En speciel form for mastcelletumor forekommer hos siamesiske katte . Her ligner mastcellerne histiocytter, og samlinger af lymfocytter og eosinofile granulocytter er spredt i tumoren . Hos ældre katte udvikler mastcelletumorer lejlighedsvis også i tyndtarmen, hvilket kan føre til intestinal invagination eller perforering og udviser aggressiv biologisk adfærd. I fritter udgør mastcelletumorer omkring 16% af hudtumorer, men de er også for det meste godartede.
Mastcelletumorer er meget sjældne hos andre pattedyr. Der er individuelle rapporter om tamkvæg , husæsler , tamsvin , lamaer , Richardson jorden egern , hamstere og afrikanske pindsvin . I mus spontane mastcelletumorer er meget sjældne, i forskning, musen er Masttumor- cellelinie P 815, men meget almindeligt anvendt.
Mastcelletumorer er meget sjældne hos fugle og krybdyr; individuelle tilfælde er blevet beskrevet i tamhøns , kædeslange og en Galápagos kæmpe skildpadde .
Weblinks
- Martin Kessler: Mastcelletumoren hos hunde: en tumor med mange ansigter.
- Mastcelletumor - information fra universitetet i München
litteratur
- Martin Kessler : Onkologi til små dyr: diagnose og terapi af tumorsygdomme hos hunde og katte . 2. udgave, Parey Verlag, Stuttgart 2005, ISBN 978-3-8304-4103-8 , s. 210-215.
- Martin Kessler: Mastcelletumorer, mastocytom (mastcellsarkom). I: Hans Georg Ingen, Peter F. Suter (red.): Praktik på hundeklinikken. 10. udgave, Parey Verlag, Stuttgart 2006, ISBN 978-3-8304-4141-0 , s. 1135-1136.
- Anthony S. Stannard og L. Thoma Remskive: Mastocytoma hos hunden . I: Jack E. Moulton (red.): Tumorer hos husdyr . 2. udgave, University of California Press, Berkeley [et al.] 1978, ISBN 0-520-02386-2 , s. 26-31.
- C. Guillermo Couto: Mastcelletumorer hos hunde og katte. I: Richard W. Nelson og C. Guillermo Couto (red.): Små dyrs indre medicin. 3. udgave, Mosby, St. Louis 2003, ISBN 0-323-01724-X , s. 1146-1149.
- 55. Österreichische Apotheker-Verlagsgesellschaft mbH: Austria-Codex Schnellhilfe 2016/17. Druckerei Berger, Horn 2016, s. 1015, ISBN 978-3-85200-244-6
Individuelle beviser
- ↑ a b R. J. Mayoral et al.: MiR-221 påvirker effektorfunktioner og actin-cytoskelet i mastceller. I: PloS en. Bind 6, nummer 10, 2011, s. E26133, ISSN 1932-6203 . doi: 10.1371 / journal.pone.0026133 . PMID 22022537 . PMC 3192147 (fri fuld tekst).
- ^ CP Shelburne og JJ Ryan: Th2-cytokiners rolle i mastcellehomeostase. I: Immunologiske anmeldelser . Bind 179, februar 2001, s. 82-93, ISSN 0105-2896 . PMID 11292031 . (Anmeldelse).
- ↑ a b S. Ch'ng et al.: Mastceller og kutane maligniteter. I: Moderne patologi . Bind 19, nummer 1, januar 2006, s. 149-159, ISSN 0893-3952 . doi: 10.1038 / modpathol.3800474 . PMID 16258517 . (Anmeldelse).
- ^ SJ Galli, M. Tsai: Mastceller i allergi og infektion: alsidig effektor og regulerende celler i medfødt og adaptiv immunitet. I: European Journal of Immunology. Bind 40, nummer 7, juli 2010, s. 1843-1851, ISSN 1521-4141 . doi: 10.1002 / eji.201040559 . PMID 20583030 . (Anmeldelse).
- ↑ Erwin Dahme og Eugen Weiss: Oversigt over husdyrens specielle patologiske anatomi. 6. udgave, Parey Verlag, Stuttgart 2007, ISBN 978-3-8304-1048-5 , s. 143.
- ↑ LA Hillman et al:. Biologisk adfærd orale og perioral mastcelletumorer hos hunde: 44 tilfælde (1996-2006). I: Journal of the American Veterinary Medical Association. Bind 237, nummer 8, oktober 2010, s.936-942, ISSN 0003-1488 . doi: 10.2460 / javma.237.8.936 . PMID 20946081 .
- ^ AK Patnaik et al.: Ekstrakutan mastcelletumor hos hunden. I: Veterinær patologi. Bind 19, nummer 6, november 1982, s. 608-615, ISSN 0300-9858 . PMID 6815869 .
- ↑ M. Fife et al.: Canine conjunctival mast cell tumors: a retrospective study. I: Veterinær oftalmologi. Bind 14, nummer 3, maj 2011, s. 153-160, ISSN 1463-5224 . doi: 10.1111 / j.1463-5224.2010.00857.x . PMID 21521438 .
- ↑ a b c d e Martin Kessler: Mastcelletumorer, mastocytom (mastcellsarkom). I: Hans Georg Ingen, Peter F. Suter (red.): Praktik på hundeklinikken. 10. udgave, Parey Verlag, Stuttgart 2006, ISBN 978-3-8304-4141-0 , s. 1135-1136.
- ↑ a b c Anthony S. Stannard and L. Thoma Pulley: Mastocytoma of the dog . I: Jack E. Moulton (red.): Tumorer hos husdyr . 2. udgave, University of California Press, Berkeley [et al.] 1978, ISBN 0-520-02386-2 , s. 26-31.
- ↑ a b c d F. Riva et al.: En undersøgelse af mutationer i c-kit genet hos 32 hunde med mastocytom. I: Tidsskrift for veterinær diagnostisk undersøgelse. Bind 17, nummer 4, juli 2005, s. 385-388, ISSN 1040-6387 . PMID 16131001 .
- ↑ H. Sadrzadeh, O. Abdel-Wahab, AT Fathi: Molekylære ændringer underliggende eosinofile og mast cellemaligniteter. I: Discovery medicin. Bind 12, nummer 67, december 2011, s. 481-493, ISSN 1944-7930 . PMID 22204765 .
- ^ Y. Takeuchi et al.: Afvigende autofosforylering af c-Kit-receptor i hunde-mastcelletumorcellelinjer. I: Veterinær immunologi og immunopatologi. Bind 137, nummer 3-4, oktober 2010, s. 208-216, ISSN 1873-2534 . doi: 10.1016 / j.vetimm.2010.05.009 . PMID 20591500 .
- ↑ K. Ohmori et al.: Identifikation af c-kit-mutationsuafhængig neoplastisk celleproliferation af hundemastceller. I: Veterinær immunologi og immunopatologi. Bind 126, nummer 1-2, november 2008, s. 43-53, ISSN 0165-2427 . doi: 10.1016 / j.vetimm.2008.06.014 . PMID 18687474 .
- ↑ a b Heike Aupperle et al.: Nye diagnostiske aspekter i hunde mastcelletumorer - en oversigt over den aktuelle undersøgelsessituation. I: specifikt lille dyr. S1 (2011), s. 44-48. ( Fuld tekst ( minde af 13. august 2012 i internetarkivet ); PDF; 1,3 MB)
- W MM Welle et al.: Hundemastcelletumorer: en gennemgang af patogenesen, kliniske træk, patologi og behandling. I: Veterinær dermatologi. Bind 19, nummer 6, december 2008, s. 321-339, ISSN 1365-3164 . doi: 10.1111 / j.1365-3164.2008.00694.x . PMID 18980632 . (Anmeldelse).
- ↑ a b c d e f James Warland og Jane Dobson: Hudtumorer hos hunde og katte. I: Veterinærfokus. Bind 21, 2011, s. 34-41.
- ↑ a b c d e Martin Kessler: Hundens mastcelletumor: en tumor med mange ansigter.
- ↑ a b c d e C. Guillermo Couto: Mastcelletumorer hos hunde og katte. I: Richard W. Nelson og C. Guillermo Couto (red.): Små dyrs indre medicin. 3. udgave, Mosby, St. Louis 2003, ISBN 0-323-01724-X , s. 1146-1149.
- ↑ a b c d e f Martin Kessler: Onkologi til små dyr: diagnose og terapi af tumorsygdomme hos hunde og katte . 2. udgave, Parey Verlag, Stuttgart 2005, ISBN 978-3-8304-4103-8 , s. 210-215.
- Hard Reinhard Mischke: Cytologisk praktik inden for veterinærmedicin . Schlütersche, Hannover 2005, ISBN 978-3-89993-013-9 , s.135 .
- ^ AK Patnaik, WJ Ehler, EG MacEwen: Hundes kutane mastcelletumor: morfologisk klassificering og overlevelsestid hos 83 hunde. I: Veterinær patologi. Bind 21, nummer 5, september 1984, s. 469-474, ISSN 0300-9858 . PMID 6435301 .
- ↑ a b M. Kiupel et al.: Forslag om et 2-trins histologisk klassificeringssystem for hunde-kutane mastcelletumorer for mere præcist at forudsige biologisk adfærd. I: Veterinær patologi. Bind 48, nummer 1, januar 2011, s. 147-155, ISSN 1544-2217 . doi: 10.1177 / 0300985810386469 . PMID 21062911 .
- ↑ RM Gil da Costa et al.: CD117 immunoexpression i hunde mastcelletumorer: korrelationer med patologiske variabler og proliferationsmarkører. I: BMC veterinærforskning. Bind 3, 2007, s. 19, ISSN 1746-6148 . doi: 10.1186 / 1746-6148-3-19 . PMID 17711582 . PMC 2077863 (fri fuld tekst).
- ↑ D. Zemke, B. Yamini, V. Yuzbasiyan-Gurkan: Mutationer i juxtamembrandomænet af c-KIT er forbundet med højere kvalitet mastcelletumorer hos hunde. I: Veterinær patologi. Bind 39, nummer 5, september 2002, s. 529-535, ISSN 0300-9858 . PMID 12243462 .
- ↑ a b J. J. Thompson et al.: Canine subkutane mastcelletumorer: cellulær proliferation og KIT-ekspression som prognostiske indekser. I: Veterinær patologi. Bind 48, nummer 1, januar 2011, s. 169-181, ISSN 1544-2217 . doi: 10.1177 / 0300985810390716 . PMID 21160022 .
- ↑ a b M. N. Mayer: Strålebehandling for hunde mastcelletumorer. I: Den canadiske veterinærdagbog. La revue vétérinaire canadienne. Bind 47, nummer 3, marts 2006, s. 263-265, ISSN 0008-5286 . PMID 16604985 . PMC 2823470 (fri fuldtekst). (Anmeldelse).
- ↑ M. Fife et al.: Canine conjunctival mast cell tumors: a retrospective study. I: Veterinær oftalmologi. Bind 14, nummer 3, maj 2011, s. 153-160, doi: 10.1111 / j.1463-5224.2010.00857.x , PMID 21521438 .
- ↑ K. Rigas et al.: Mastcelletumorer hos hunde under 12 måneder: en multi-institutionel retrospektiv undersøgelse. I: J. Small Anim. Øv. Bind 61, 2020, udgave 7, s. 449–457.
- ↑ AS Moore et al.: Retrospektiv resultatevaluering for hunde med kirurgisk udskåret, ensom Kiupel højgradig, kutan mastcelletumor. I: Vet. Comp. Oncol. 2020. doi: 10.1111 / vco.12565
- ^ NC Northrup, RE Roberts, TW Harrell, KL Allen, EW Howerth, TL Gieger: Iridium-192 interstitiel brachyterapi som supplerende behandling for hunde kutane mastcelletumorer. I: Journal of the American Animal Hospital Association. Bind 40, nummer 4, 2004 jul-aug, s. 309-315, ISSN 1547-3317 . PMID 15238561 .
- G SM Govier: Principper for behandling af mastcelletumorer. I: Kliniske teknikker i praksis med små dyr. Bind 18, nummer 2, maj 2003, s. 103-106, ISSN 1096-2867 . doi: 10.1053 / svms.2003.36624 . PMID 12831070 . (Anmeldelse).
- ↑ L. Blackwood et al:. Europæisk konsensus dokument på mastcelletumorer hos hunde og katte. I: Veterinær og komparativ onkologi. Bind 10, nummer 3, september 2012, s. E1 - e29, doi: 10.1111 / j.1476-5829.2012.00341.x , PMID 22882486 (anmeldelse)
- ↑ KM Rassnick et al.: Fase II open-label undersøgelse af hydroxyurinstof med enkelt middel til behandling af mastcelletumorer hos hunde. I: Veterinær og komparativ onkologi. Bind 8, nummer 2, juni 2010, s. 103-111, ISSN 1476-5829 . doi: 10.1111 / j.1476-5829.2010.00211.x . PMID 20579323 .
- ↑ K. Hosoya et al.: Adjuvans CCNU (lomustin) og prednison kemoterapi til hunde med ufuldstændigt udskåret mast celle tumorer. I: Journal of the American Animal Hospital Association. Bind 45, nummer 1, 2009 jan-feb, s. 14-18, ISSN 1547-3317 . PMID 19122059 .
- ↑ KM Rassnick et al.: En fase II-undersøgelse til evaluering af toksiciteten og effekten af skiftevis CCNU og højdosis vinblastin og prednison (CVP) til behandling af hunde med højgradige, metastatiske eller ikke-resekterbare mastcelletumorer. I: Veterinær og komparativ onkologi. Bind 8, nummer 2, juni 2010, s. 138-152, ISSN 1476-5829 . doi: 10.1111 / j.1476-5829.2010.00217.x . PMID 20579327 .
- ↑ Österreichische Apotheker-Verlagsgesellschaft mbH: Austria-Codex Schnellhilfe 2016/17 . Red.: Österreichische Apotheker-Verlagsgesellschaft mbH Wien 2016, ISBN 978-3-85200-244-6 , s. 1015 .
- ↑ Produktinformation for Palladia filmovertrukne tabletter til hunde. (PDF) Hentet 2. januar 2017 .
- ^ KA Hahn et al.: Masitinib er sikker og effektiv til behandling af hundemastcelletumorer. I: Journal of veterinary internal medicine bind 22, nummer 6, 2008 nov-dec, s. 1301-1309, ISSN 0891-6640 . doi: 10.1111 / j.1939-1676.2008.0190.x . PMID 18823406 .
- ↑ adgang til Toceranib på Vetpharm, der blev fundet den 29. juli 2012 fundet.
- ↑ O. Yamada et al.: Imatinib fremkaldte et gunstigt svar hos en hund med en mastcelletumor, der bar et c-kit c.1523A> T-mutation via undertrykkelse af konstitutiv KIT-aktivering. I: Veterinær immunologi og immunopatologi. Bind 142, nummer 1-2, juli 2011, s. 101-106, ISSN 1873-2534 . doi: 10.1016 / j.vetimm.2011.04.002 . PMID 21561667 .
- ↑ TT De Ridder et al.: Randomiseret kontrolleret klinisk undersøgelse, der evaluerer effektiviteten og sikkerheden ved intratumoral behandling af canina-mastcelletumorer med Tigilanol-tiglat (EBC-46). I: J. Vet. Intern. Med. 2020, doi: 10.1111 / jvim.15806 .
- ↑ Guideline Mastocytosis (PDF; 313 kB) fra det tyske dermatologiske samfund
- ↑ Heiko Traupe, Henning Hamm: Pædiatrisk dermatologi . 2. udgave, Springer, Heidelberg 2005, ISBN 978-3-540-25646-5 , s. 215-223.
- ↑ a b Gerd Plewig, P. Thomas: Fremskridt inden for praktisk dermatologi og venereologi 2006 . Bind 20 af fremskridt inden for praktisk dermatologi og venereologi . Springer, Heidelberg 2007, ISBN 3-540-30514-9 , s. 391.
- ↑ Otto Braun-Falco et al.: Dermatology and Venereology . 5. udgave, Springer, Heidelberg 2005, ISBN 978-3-540-40525-2 , s. 1396.
- ↑ Wolfgang Remmele: Patologi. 1. Juridiske spørgsmål inden for patologi; Introduktion til biopsidiagnostik; Hjerte- og vaskulær system; Hæmatologi; Milt; Thymus . 2. udgave, Springer, Berlin 1999, ISBN 3-540-61095-2 , s. 507-508.
- ↑ Hanns-Jürgen Wintzer: Hestesygdomme : en guide til studier og praksis. 3. udgave, Parey, Berlin 1999, ISBN 3-8263-3280-6 , s. 483.
- ↑ Laura Marconato og Giuliano Bettini: Tarmtumorer hos katte. I: Veterinærfokus 23 (2013), s. 39-45.
- ↑ GA Parker, CA Picut: Histopatologisk funktioner og post-kirurgisk følgetilstande af 57 kutane neoplasmer hos fritter (Mustela putorius furo L.). I: Veterinær patologi. Bind 30, nummer 6, november 1993, s. 499-504, ISSN 0300-9858 . PMID 8116142 . (Anmeldelse).
- ^ BI Smith og LA Phillips: Medfødte mastocytomer i en Holstein-kalv. I: Den canadiske veterinærdagbog. Bind 42, nummer 8, august 2001, s. 635-637, ISSN 0008-5286 . PMID 11519274 . PMC 1476568 (fri fuld tekst).
- ^ G. Kay et al.: Grad III mastocytom i et æsel. I: Veterinærjournalen. Bind 152, nummer 9, marts 2003, s. 266-267, ISSN 0042-4900 . PMID 12638914 .
- ↑ G. Migaki, KA Langheinrich: mastocytoma i en gris. I: Pathologia veterinaria. Bind 7, nummer 4, 1970, s. 353-355, ISSN 0031-2975 . PMID 4998946 .
- ↑ TY Lin et al.: Mastcelletumorer i en lama (Lama glama). I: Tidsskrift for veterinær diagnostisk undersøgelse. Bind 22, nummer 5, september 2010, s. 808-811, ISSN 1040-6387 . PMID 20807950 .
- ^ XJ He et al.: Spontan kutan mastcelletumor med lymfeknudemetastase i en Richardsons jordekorn (Spermophilus richardsonii). I: Tidsskrift for veterinær diagnostisk undersøgelse. Bind 21, nummer 1, januar 2009, s. 156-159, ISSN 1040-6387 . PMID 19139521 .
- ↑ K. Nishizumi, K. Fujiwara, A. Hasegawa: Kutane mastocytomer i djungariske hamstere. I: Forsøgsdyr. Bind 49, nummer 2, april 2000, s. 127-130, ISSN 1341-1357 . PMID 10889951 .
- ↑ JT Raymond, MR White, EB Janovitz: Ondartet mastcelletumor i en afrikansk pindsvin (Atelerix albiventris). I: Journal of wildlife sygdomme. Bind 33, nummer 1, januar 1997, s. 140-142, ISSN 0090-3558 . PMID 9027702 .
- ^ DJ Lewis, JM-tilbud: Malignt mastocytom hos mus. I: Journal of comparative pathology. Bind 94, nummer 4, oktober 1984, s. 615-620, ISSN 0021-9975 . PMID 6439762 .
- ↑ GM Patnaik, D. Mohanty: Et tilfælde af aviær mastocytomer. I: Den indiske veterinærjournal. Bind 47, nummer 4, april 1970, s. 298-300, ISSN 0019-6479 . PMID 4987390 .
- ↑ J. Schumacher, RA Bennett, LE Fox, SL Deem, L. Neuwirth, JH Fox: Mastcelletumor i en østlig kingsnake (Lampropeltis getulus getulus). I: Tidsskrift for veterinær diagnostisk undersøgelse. Bind 10, nummer 1, januar 1998, s. 101-104, ISSN 1040-6387 . PMID 9526872 .
- ↑ M. Santoro et al.: Mastcelletumor i en kæmpe Galapagos-skildpadde (Geochelone nigra vicina). I: Journal of comparative pathology. Bind 138, nummer 2-3, 2008 feb-apr, s. 156-159, ISSN 0021-9975 . doi: 10.1016 / j.jcpa.2007.11.004 . PMID 18308330 .