Ribose
| Strukturel formel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||
| Fischer projektion , åben kæde repræsentation | ||||||||||
| Generel | ||||||||||
| Efternavn | Ribose | |||||||||
| andre navne |
|
|||||||||
| Molekylær formel | C 5 H 10 O 5 | |||||||||
| Kort beskrivelse |
farveløst fast stof |
|||||||||
| Eksterne identifikatorer / databaser | ||||||||||
| ||||||||||
| ejendomme | ||||||||||
| Molar masse | 150,13 g mol −1 | |||||||||
| Fysisk tilstand |
fast |
|||||||||
| massefylde |
0,80 g cm −3 (20 ° C) |
|||||||||
| Smeltepunkt |
90-95 ° C |
|||||||||
| opløselighed |
opløseligt i vand |
|||||||||
| Sikkerhedsinstruktioner | ||||||||||
| ||||||||||
| Så vidt muligt og sædvanligt anvendes SI-enheder . Medmindre andet er angivet, gælder de givne data for standardbetingelser . | ||||||||||
Ribose er en sukker med fem carbon -atomer, en pentose , og forekommer hyppigt i naturen som D- ribose, mens den enantiomere L- ribose er af ringe betydning.
D- ribose er en del af byggestenene til ribonukleinsyre (RNA). I nukleosiderne er ribosen bundet til en nukleobase via C1-atomet , for eksempel i adenosin , cytidin , guanosin , uridin og ribothymidin . De tilsvarende nukleotider dannes ved yderligere phosphorylering af den hydroxylgruppen (-OH) på C5-atomet . Rygraden ( rygraden ) i et RNA- makromolekyle, der danner de via organofosfatbindinger , der er sammenkoblet riboseenheder.
"Ribose" betyder normalt D- ribose. D - deoxyribose i deoxyribonukleinsyre (DNA) adskiller sig kun fra dette ved C2-atomet på grund af et manglende iltatom . Ribose kan også syntetiseres fra andre monosaccharider i den menneskelige organisme via pentose-phosphat-cyklussen .
Etymologi og isolation
Den fremtrædende kemiker Emil Fischer erkendte, at der ud over kulhydraterne xylose og arabinose , som består af fem carbonatomer, skal være en anden isomer ( epimer ), som han kaldte ribose. Dette er et kunstigt navn kombineret med omvendte bogstaver med navnet Arabinose. Forskeren Phoebus Levene , der kom fra USA til Fischers Berlin-institut, satte kursen mod en vej, der førte ind i fremtiden, som han ikke kunne forudse på det tidspunkt: han hydrolyserede "gærnukleinsyre" fra bagegær og fik en ribose med en D- , D- , D- konfiguration. Resultatet blev beskrevet i rapporterne fra det tyske kemiske selskab i 1909 .
Yderligere undersøgelser af Levene og WA Jacobs viste, at sukkerribosen er bundet til heterocykliske baser, f.eks. B. adenin, var bundet, d. H. var til stede som et nukleosid. Som beskrevet ovenfor er phosphatgrupper (nukleotider) bundet til nukleosiderne.
Imidlertid var Levenes proces for dyr til at producere store mængder ribose. Hellmut Bredereck udviklede forbedrede metoder ved at bruge et enzym fra søde mandler til hydrolyse. På denne måde kunne reaktionstemperaturen sænkes.
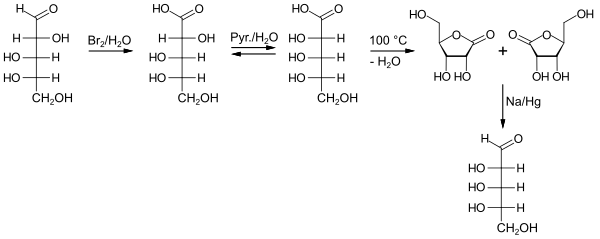
Synteser
Midlertidigt før D- ribosen var af Oskar Piloty ved delvis syntese , startende fra gruppen bestående af arabisk tyggegummi, der kunne opnås ved hydrolyse af L- arabinose først (1891), opnåede L- ribose. Til dette formål blev aldehydgruppen i aldosen oxideret til carboxylsyren ( L- arabonsyre, L- arabinsyre) med bromvand . Efter opvarmning med den svage base pyridin i vandig opløsning fandt epimerisering sted ved C2-atomet, dvs. H. i ligevægt med L- arboxylsyre blev L- ribonsyre dannet. Dette blev adskilt og cykliseret til lactonen , som i det sidste trin blev reduceret til L- ribose under anvendelse af natriumamalgam . Willem Alberda van Ekenstein og Jan Johannes Blanksma forbedrede oprensningen af L- ribose efter reduktion med natriumamalgam. Efter at D- arabinose også var blevet tilgængelig gennem nedbrydning af billig D- glucose, producerede van Ekenstein og Blanksma også D- ribose ved hjælp af Fischer-Piloty-metoden.
Fischer-projektionsformlerne anvendt på tidspunktet for belysning af disse kulhydrater giver ikke noget indtryk af den rumlige struktur. Derfor er perspektiviske skeletformler af lactoner inkluderet.
I 1898 udgav Otto Ruff en anden metode til omdannelse af D - gluconsyre til D - arabinose ( Ruff nedbrydning ). Calciumsaltet af carboxylsyren (calcium D- gluconat) blev oxidativt decarboxyleret med hydrogenperoxid i nærvær af jernsalte.
En vigtig forbedring i syntesen af D- epimeren var den elektrokemiske oxidation af D arabinosen ved anoden, hvor calciumcarbonat blev tilsat. The D -arboxylic syre kunne isoleres som calciumsaltet og behandles yderligere.
Paul Karrer og kolleger brugte disse reaktionstrin til en syntese af lactoflavin .
For nylig er den "unaturlige" L- ribose også kommet tilbage i fokus; Derivater med denne pentose kan være af interesse for udviklingen af aktive farmaceutiske ingredienser. For eksempel kan L- ribose produceres fra L- arabinose gennem bioteknologi (sammenlign med Pilotys syntese, se ovenfor).
ejendomme
Ribose er et farveløst fast stof med et smeltepunkt på 90–95 ° C og er opløseligt i vand.
D- riboses forfatning og strukturer var blevet arbejdet omhyggeligt. En krystalstrukturanalyse af forbindelsen blev kun rapporteret i 2010. Røntgendiffraktion og NMR-spektroskopiske eksperimenter kom til det resultat, at molekylerne i krystallinsk D-ribose danner en hemiacetal og er til stede som en seksleddet ring i en pyranoseform . Der er to isomere former, α- D- ribopyranose og β- D- ribopyranose, som er indeholdt i krystallen i forskellige proportioner.
Når ribosen er opløst i vand, bevarer den pyranosestrukturen delvist; derudover, som det længe har været kendt, dannes fem ringe i en kemisk ligevægt, dvs. H. Furanoser dannet. I begge tilfælde er α- og β- anomere former mulige.
Ved 31 ° C, 58,5% af den D- ribosemolekylet er i p- D -pyranoids, 21,5% i α- D -pyranoids, og 13,5% i β- D -furanoids, 6,5% i α- D furanoid og 0,05% i åben kæde. Β-pyranose-formen er derfor mest almindelig i vandig opløsning, da tre af de fire hydroxylgrupper er placeret i ækvatorialplanet.
| D -Ribose stavemåder | ||
|---|---|---|
| Kileformel | Haworth notation | |

|
 α- D- ribofuranose |
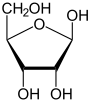 β- D- ribofuranose |
 α- D- ribopyranose |
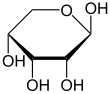 β- D- ribopyranose |
|
Biologisk betydning og biosyntese

D- ribose, esterificeret med phosphorsyre ved C5-OH, er et medlem af kulhydratmetabolismen som ribose-5-phosphat . Dens biosyntese forekommer på flere måder. En precursor er ribulose-5-phosphat , en anden er glyceraldehyd-3-phosphat , som ekspanderes med en C 2 -fragment i en transketolase reaktion til dannelse C 5 sukker phosphat.
Ribose er en byggesten af nukleosider og nukleotider . Ribosylnukleosidphosphater spiller en vigtig rolle i metabolismen af celler, for eksempel som biologiske energibærere, såsom adenosindiphosphat (ADP) og adenosintrifosfat (ATP). Effekten af hormonelle og nervøse signaler i cellen kan forbedres med cyklisk adenosinmonophosphat (cAMP), der tjener som et sekundært messenger-stof .
Interstellar forekomst
Ribose blev påvist i meteoritter i 2019. Da dette kulhydrat er essentielt for livet på jorden, rejser dette fund igen spørgsmålet om kemisk udvikling , dvs. H. hvordan det præbiotiske "liv" udviklede sig på vores planet.
bevis
Ribose kan påvises med Bial-reagenset (en opløsning af orcin og jern (III) chlorid i koncentreret saltsyre ). Testen er positiv, hvis en grønblå farve ændres efter tilsætning af Bial-reagens til kulhydratet og efter opvarmning.
Weblinks
Individuelle beviser
- ↑ a b c d e f Indtastning til CAS-nr. 50-69-1 i GESTIS stof database over den IFA , adgang den 11. september 2014. (JavaScript krævet)
- ^ PA Levene, WA Jacobs. Rapporter fra det tyske kemiske samfund, bind 1909, bind 42, 1201.
- ↑ Hellmut Bredereck: Repræsentation af nukleosider ved enzymatisk hydrolyse af gærnukleinsyre; på samme tid et bidrag til repræsentationen af d-ribose. I: Rapporter fra det tyske kemiske selskab. Født 1938, bind 71, 408. https://doi.org/10.1002/cber.19380710237
- ↑ Hellmut Bredereck, Martin Köthnig, Eva Berger: Om d-Ribose (repræsentation af en krystalliseret anhydroribose) , I: Rapporter fra det tyske kemiske samfund. 1940, bind 73, 956. https://doi.org/10.1002/cber.19400730906
- ^ W. Alberda van Ekenstein, J. Blanksma: Om krystalliseret l-ribose. I: Chemisch Weekblad Vol. 6, s. 373-375. Baseret på præsentationen af Henle i Chemisches Zentralblatt Jg. 1908, bind 2, s. 1584. https://delibra.bg.polsl.pl/dlibra/publication/38191/edition/34381/content?ref=struct , tilgængelig den 19. oktober 2020.
- ^ W. Alberda van Ekenstein, J. Blanksma: Om d-Ribose. I: Chemisch Weekblad bind 10, s. 664. Baseret på rapporten fra Schönfeld i Chemisches Zentralblatt Jg. 1913, bind 2, s. 1562. https://delibra.bg.polsl.pl/dlibra/publication/18297 / udgave / 17223 / content? ref = struct , adgang 19. oktober 2020.
- ↑ Otto Ruff: Om transformation af d-gluconsyre til d-arabinose , I: Reports of the German Chemical Society, Jg. 1898, bind 31, s. 1573. https://doi.org/10.1002/cber. 18980310250
- ^ Marguerite Steiger, Helvetica chimica Acta. Vol. 19, s. 189. I hendes digitaliserede afhandling, der er tilgængelig på Internettet, er eksperimentelle detaljer beskrevet detaljeret. https://www.research-collection.ethz.ch/bitstream/handle/20.500.11850/133644/1/eth-20781-01.pdf
- ↑ Paul Karrer, B. Becker, F. Benz, P. Frei, H. Salomon, K. Schopp, om syntesen af lactoflaviner . I: Helvetica Chimica Acta. Født 1935, bind 18, s. 1435-1448. DOI: 10.1002 / hlca.193501801196
- ↑ M. Helanto, K. Kiviharju, T. Granström, M. Leisola, A. Nyyssölä: bioteknologisk produktion af l-ribose fra L-arabinose . I: Anvendt mikrobiologi og bioteknologi bind 2009, bind 83, s. 77-83.
- ↑ Dubravka Sisak, LB McCusker, G. Zandomeneghi, BH Meier, D. Blaser, R. Boese, WB Schweizer, R. Gylmour, JD Dunitz. Bedre sent end aldrig! Furanoseformen af D- ribose, som forekommer i utallige biomolekyler, forekommer ikke i den krystallinske forbindelse . I: Angewandte Chemie, bind 2010, bind 122, 4605; Angewandte Chemie International Edition, bind 2010, bind 49, 4503. https://doi.org/10.1002/anie.201001266
- ↑ Stephen J. Angyal: Sammensætningen af at reducere sukker i opløsning. I: Fremskridt inden for kulhydratkemi og biokemi . 1984, bind 42, s. 15-68, doi : 10.1016 / S0065-2318 (08) 60122-5 .
- ↑ Peter Karlson et al., Kort lærebog om biokemi for medicinske og naturvidenskabelige forskere, 13. udgave, 1988, s. 218-230, Thieme, Stuttgart, New York.
- ↑ Yoshihiro Furukawa, Yoshito Chikaraishi, Naohiko Ohkouchi, O. Ogawa, Daniel P. Glavin, Jason P. Dworkin, Chiaki Abe, Tomoki Nakamura: Extraterrestrial ribose og andet sukker i primitive meteoritter, In:.. PNAS Vol 2019 Vol 116, Pp. 24440-24445; https://www.pnas.org/content/116/49/24440