L- gulonolactonoxidase
| L-gulonolactonoxidase | ||
|---|---|---|
| Egenskaber ved humant protein | ||
| Masse / længde primær struktur | hos mennesker uden oversættelse | |
| Identifikator | ||
| Eksterne ID'er |
|
|
| Enzymklassificering | ||
| EF, kategori | 1.1.3.8 , oxidoreduktaser | |
| Svarstype | oxidation | |
| Substrat | L - gulonolacton + O 2 | |
| Produkter | Askorbinsyre + hydrogenperoxid | |
| Hændelse | ||
| Forældre taxon | Hvirveldyr | |
| Undtagelser | Tørre-næse primater , marsvin , real benfisk , nogle spurvefugle og bat familier | |
| Ortolog | ||
| person | mus | |
| Entrez | 2989 | 268756 |
| Ensemble | ENSG00000234770 | ENSMUST00000059970 |
| UniProt | P58710 | P58710 |
| Refseq (mRNA) | NG_001136.2 | NM_178747.3 |
| Refseq (protein) | NP_848862.1 | |
| Gen locus | Chr 8: 27,42 - 27,45 Mb | Chr 14: 65,99 - 66,01 Mb |
| PubMed søgning | 2989 |
268756
|
L -Gulonolactonoxidase ( GULO , gulo eller GLO ), også kendt som L -Gulono -γ -lactonoxidase, der refereres til, er et enzym fra gruppen af oxidaser , hvilket for produktionen af ascorbinsyre er meget vigtigt (C -vitamin) i højere organismer . Det katalyserer det sidste trin i biosyntesen af ascorbinsyremed den selektive oxidation af L- gulonolacton (også kaldet L- gulono-1,4-lacton eller L- gulono-γ-lacton). Den L -Gulonolactonoxidase findes i næsten alle hvirveldyr (hvirveldyr), og - ifølge den nuværende viden (2013) - selv med meget mange hvirvelløse dyr (hvirvelløse dyr).
The L -Gulonolactonoxidase er ved ekspression af et gen , den Gulo producerede genet. En genetisk defekt udløst af en mutation betyder, at den berørte organisme ikke længere er i stand til at producere ascorbinsyre. Uden tilstrækkeligt C -vitaminindtag gennem mad udvikler sådanne organismer hypovitaminose C - kaldet skørbug hos mennesker . Hos mennesker såvel som mange andre hvirveldyrsgrupper, herunder I alle real benfisk (Teleostei), mest systematiske enheder af de flagermus (CHIROPTERA) og nogle systematiske enheder af spurvefuglene (Passeriformes) samt alle marsvin (Caviidae) den genetisk bestemt manglende evne til at kunne producere ascorbinsyre svarer imidlertid til en normal tilstand erhvervet i løbet af evolutionen. C -vitamin mangelsymptomer forekommer kun i ekstraordinære situationer hos dem på grund af en mad, der generelt er rig på C -vitamin. Mens i mennesker og de andre berørte amniotes Gulo er til stede som en pseudogen og kaldes derfor også GULOP eller GuloP ( P står for 'pseudo'), er det ikke længere kan påvises i det virkelige benfisk.
Kun tabet af funktion af L- gulonolactonoxidase gør ascorbinsyre pr. Definition til et ' vitamin ' for den pågældende art . For alle andre arter med funktionel L- gulonolactonoxidase er ascorbinsyre bare en metabolit .
Funktion og beskrivelse
Askorbinsyre er afgørende for alle planter og dyr . Som autotrofe organismer har planter ingen eksogene kilder til at opfylde deres askorbinsyrebehov. De er derfor alle afhængige af selvsyntesen af ascorbinsyre. På den anden side kan dyr, der er fundamentalt heterotrofe, i princippet opfylde deres krav til ascorbinsyre ved f.eks. At spise planter. Langt de fleste hvirveldyr er imidlertid i stand til selv at syntetisere ascorbinsyre. Med det meget store antal hvirvelløse dyr er viden om, hvilke arter der er i stand til at syntetisere ascorbinsyre, stadig meget skitseret og i nogle tilfælde modstridende. Biosyntesen af ascorbinsyre i planter er fundamentalt anderledes end hos dyr. For eksempel i det sidste syntesetrin af højere planter er L - galactono-1,4-lacton substratet for enzymet L- galactono-1,4-y-lactone dehydrogenase (GLDH). L- gulonolactonoxidase spiller ingen rolle i biosyntesen af ascorbinsyre i planter.
Hos dyr begynder biosyntese med D - glucose (druesukker). Det enzymatisk omdannes til ascorbinsyre i fire trin via mellemprodukter D - glucuronsyre , L - gulonsyre og L- gulono-1,4-lacton. Enzymet L- gulonolactonoxidase er påkrævet til det sidste trin i biosyntese hos dyr . Det katalyserer oxidationen af L- gulono-1,4-lacton til ascorbinsyre. Denne reaktion kræver også ilt, som tilføres de ascorbinsyreproducerende celler via blodkarrene . Sammen med to hydrogenatomer, som fjernes fra ringsystemet af L- gulonolacton i 3,4-stillingen under reaktionen, dannes der således hydrogenperoxid som et biprodukt af reaktionen .
Organismer, der mangler enzymet L- gulonolactonoxidase, eller som ikke fungerer korrekt på grund af en mutation, kan ikke selv producere ascorbinsyre. Disse organismer afhænger af indtagelse af tilstrækkelige mængder ascorbinsyre fra mad. Ellers bliver de syge med en C -vitaminmangel.

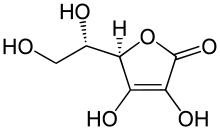
L- gulonsyre ( 1 ) omdannes til L- gulonolacton ( L- gulono-1,4-lacton) ( 2 ) under katalytisk påvirkning af en glucono -lactonase ( A ) . I det sidste trin, L- gulonolactone oxidase ( B ) katalyserer selektiv oxidation af L- gulonolactone til 2-keto- L- gulonlactone ( 3a ), som tautomeriseres spontant til ascorbinsyre ( 3b ) . Hydrogenperoxid (H 2 O 2 ) er udformet som et biprodukt af oxidationen . Hvis en organisme mangler enzymet L- gulonolactonoxidase, kan den ikke selv producere ascorbinsyre. Så afhænger det af det eksogene indtag af ascorbinsyre for overlevelse . Ellers bliver han syg på grund af C -vitaminmangel, som vil føre til døden efter flere måneder.
L- gulonolactonoxidase er et mikrosomalt enzym. Hos rotter og andre gulo-positive pattedyr findes det i mikrosomerne i hepatocytterne (leverceller). Det er et membranbundet enzym, hvis aktive side stikker ind i lumen af mikrosomet. I modsætning hertil frigives det oxiderede substrat - ascorbinsyre - ekstraluminalt i retningen af det endoplasmatiske retikulum . Hydrogenperoxidet, der også produceres under reaktionen, reduceres med ækvivalente mængder glutathion . Det foretrukne substrat for L - gulonolactonoxidase er L- gulono-1,4-lacton. Derudover er det også i stand til at katalysere oxidationen af L - galactonolacton , D - mannonolacton og D - altronolacton . I modsætning hertil katalyseres ikke oxidationen af andre y-lactoner , såsom L - idonolacton eller D- gluconolacton . Det er klart, at de egnede substrater skal have en hydroxygruppe på det andet carbonatom . The Michaelis konstant (K m værdi) af L- gulonolactone oxidase er i området fra 0,007 til 0,15 mM. I princippet er elektronoverførslen fra L- gulonolactonoxidase ikke begrænset til oxygen som elektronacceptor . Andre oxidationsmidler, såsom phenazinmethosulfat eller kaliumhexacyanidoferrat (III), kan også oxidere L- gulono-1,4-lacton til ascorbinsyre ved hjælp af L- gulonolactonoxidase . L- gulonolactonoxidase isoleret fra rottelever består af 440 aminosyrer og har en molmasse på 50.605 g / mol. Genet, der koder for dette enzym, har en åben læseramme på 1320 nukleotider .
Forekomst og bevis

Gulo- genet, der koder for enzymet L- gulonolactonoxidase, findes i næsten alle hvirveldyr. Det bruges primært af celler i leveren eller nyrerne udtrykt . Disse to organer er hovedproducenterne af ascorbinsyre hos hvirveldyr. I udviklingsforløbet fandt en ændring i ascorbinsyresyntese fra nyrerne til leveren sted uafhængigt af hinanden i forskellige udviklingslinjer hos hvirveldyr. Således producerede fisk , padder , krybdyr og evolutionært ældre fugle - ordener samt æglæggende pattedyr ( monotremes , monotremes) ascorbinsyre i nyrerne. Derimod finder produktionen af ascorbinsyre sted i de evolutionære yngre fugleordner og hos de højere pattedyr (placentalia) i leveren. Pungdyr (Marsupialia) producerer ascorbinsyre i både nyrerne og leveren. Overgangen til større lever kan være et resultat af et højere selektionstryk til under stressbetingelser , homeostasen til bedre vedligeholdt.
Gulo udtrykkes kun af mange organismer i en senere fase af deres individuelle udvikling. For eksempel rotte fostre er kun i stand til at producere ascorbinsyre fra den 16. dag og fremefter. Udtrykket af gulo kan øges med forskellige stimuli. Dette omfatter f.eks. Glykogenolyse (nedbrydning af glykogen ). Forskellige lægemidler, såsom barbiturater , phenazon eller aminophenazon , samt kræftfremkaldende stoffer, såsom methylcholanthren eller benzo [ a ] pyren , øger gulo -ekspressionen i forsøgsdyr. Årsagen til dette er sandsynligvis det øgede behov for glucuronsyre for at afgifte disse xenobiotika . Det er klart, at alle enzymer i glucuronsyrebanen er opreguleret.
Nogle arter er ikke i stand til selv at syntetisere ascorbinsyre. Ifølge den nuværende status er årsagen til dette altid en defekt i gulo -genet eller dets sletning .
Indtil 1970'erne bestod den klassiske detektionsmetode for et defekt eller manglende gulo -gen i at fodre forsøgsdyr så frit som muligt fra ascorbinsyre og derefter undersøge dem for symptomer på C -vitaminmangel. Derefter udviklede in vitro teknikker, hvor man, for eksempel fra lever eller nyre af den art, der skal testes med vævshomogenater L -Gulono -1,4 -lacton, -forstadiemolekylet for ascorbinsyren i biosyntesen -offset og katalytisk under påvirkning af L- gulonolactonoxidase bestemte mængden af dannet ascorbinsyre. Begge er indirekte detektionsmetoder for tilstedeværelsen af L- gulonolactonoxidase. Moderne metoder til genekspressionsanalyse fra Gulo er f.eks. Baseret på Gulo-specifikke antistoffer og Western blotting samt på fluorescens in situ hybridisering .
Hvirvelløse dyr og basale hvirveldyr
I løbet af tilfældige test på hvirvelløse dyr ("Invertebrata") og fisk blev der i første omgang ikke fundet tegn på aktivitet af L- gulonolactonoxidase eller generelt om disse dyrs evne til at kunne syntetisere ascorbinsyre. En af disse arter er for eksempel den ørkengræshoppe ( Schistocerca gregaria ). I 1970'erne førte disse resultater til den opfattelse, at fisk, insekter og andre hvirvelløse dyr grundlæggende ikke var i stand til at producere ascorbinsyre. Da det var kendt, at L- gulonolactone oxidase er til stede i aktiv form i moderne padder , blev hypotesen suppleret med postulat, L- gulonolactone oxidase kun var til stede i løbet af vertebraten jord skift , der forekom i perioden inden ca.. For 416 til 359 Millioner af år siden menes det at være en nyerhvervet egenskab. Behovet for ascorbinsyre, lyder argumentet, er betydeligt højere på grund af det øgede oxidative stress forbundet med at gå i land.
Ved fastlæggelsen af denne hypotese blev ældre undersøgelser, der var i direkte modstrid med den, imidlertid ikke taget i betragtning. Allerede i 1922 viste det sig for eksempel, at "modelorganismen" Drosophila melanogaster (sortbuget frugtflue) fungerede uden ascorbinsyre i kosten. Det samme gælder den røde bomuldspindorm ( Pectinophora gossypiella ) og møllen Argyrotaenia velutinana . Derudover blev der begået systematiske fejl . Den undersøgte fisk hele tilhørte den virkelige benfisk (Teleostei), der er dog et relativt stærkt afledt gruppe af ray finner (Actinopterygii). Efter at evnen til at syntetisere ascorbinsyre kunne påvises i de mere primitive strålingsfinner, lungefisk (Dipnoi), hajer (Selachii) og stråler (Batoidea), var antagelsen om, at denne evne kun blev erhvervet evolutionært hos hvirveldyr ved at gå i land ikke længere holdbar. Efter aktiv L- gulonolactone oxidase blev påvist i 1998 i havet lampret ( Petromyzon marinus ), en meget original hvirveldyr, det kan også antages, at ascorbinsyre syntese er en original træk ved alle hvirveldyr, der kun fik tabt i et par linjer af udvikling. Hos hvirvelløse dyr er kendskabet til ascorbinsyresyntesens evne imidlertid stadig for ufuldstændigt til på nuværende tidspunkt (2013) at kunne bestemme, hvornår denne evne, der blev muliggjort af L- gulonolactonoxidase, første gang dukkede op under udviklingen.
"Højere" hvirveldyr uden L- gulonolactonoxidase
Hos alle hvirveldyr, der ikke er i stand til selv at syntetisere ascorbinsyre, er årsagen altid gulo -genet, hvis genprodukt katalyserer det sidste trin i biosyntesen til ascorbinsyre. I ingen af disse dyr er en genetisk defekt i et af de tre andre enzymer involveret i ascorbinsyrebiosyntese årsagen. Forklaringen på dette er, at en defekt i Gulo kun påvirker syntesen af ascorbinsyre, mens en genetisk defekt med hensyn til andre enzymer ville afbryde biosyntesen af andre stoffer. For eksempel en genetisk defekt, der forhindrede produktion af glucono-laktonase ville ikke kun afbryder syntesen af L- gulonolactone, men også blandt andet, den pentosephosphatvejen og nedbrydningen af caprolactam . Den Gulo gen emne, sammenlignet med de andre gener i Ascorbinsäurebiosynthese, en meget mindre selektionstryk. Et tab af funktion har mindre fatale konsekvenser og er åbenbart selv uden negative virkninger i nogle organismer. Flere hvirveldyrslinjer er negative for L- gulonolactonoxidase. Disse er alle ægte benede fisk (Teleostei), nogle familier af passerine fugle (Passeriformes) og flagermus (Chiroptera), alle arter fra marsvinfamilien (Caviidae) og alle arter, der tilhører underordnelsen af de tørre næser (Haplorhini) ), herunder menneskers. Hos de ægte benede fisk, marsvin og primater med tør næse er den genetiske defekt så alvorlig, at den kan klassificeres som irreversibel i evolutionære termer. I modsætning hertil er det originale gulo -pseudogen tilsyneladende blevet reaktiveret i nogle flagermus- og passerine -fuglearter i løbet af udviklingen. Ifølge den nuværende videnstilstand spillede fødevaren fra de berørte arter naturligvis ingen rolle i denne "genreaktivering". Det menes derfor, at tabet af evnen til at syntetisere ascorbinsyre er en neutral egenskab .
Ægte benfisk (Teleostei)

De terrestriske hvirveldyr (Tetrapoda) er hovedsageligt en gulopositiv stor gruppe, men indeholder nogle taxa - især blandt pattedyr - som heller ikke har nogen funktionel L -gulonolactonoxidase. Disse er angivet separat nedenfor.

Oprindeligt blev det antaget, at fisk generelt ikke er i stand til at syntetisere ascorbinsyre, og at denne evne først udviklede sig hos de tidlige terrestriske hvirveldyr i udviklingsforløbet. Baseret på omfattende forskning ved vi nu, at alle fisk, med undtagelse af den ægte benede fisk (Teleostei), producerer ascorbinsyre i deres krop. De gør dette ved hjælp af L- gulonolactonoxidase, som produceres i nyrerne på alle gulo-positive fisk. Askorbinsyresyntese er et forfædreegenskab, der findes hos hvirveldyr, og som blev tabt for den almindelige forfader til teleostdyret for omkring 200 til 210 millioner år siden. Det gentab, der forårsager denne egenskab, er tilsyneladende fuldstændigt. Ved hjælp af BLAST -algoritmen kunne Gulo -sekvensen eller resterne af den ikke findes i nogen af de fuldstændigt sekventerede genomer af et teleostdyr . I sammenligning, en fund, baseret på proteinsekvensen af L -Gulonolactonoxidase af indenlandske kylling ( Gallus domesticus ), en 74% match til den hvide stør ( Acipenser transmontanus ) og endda til Ciona intestinalis ( Ciona intestinalis ) eller en 48% aftale. Den Gulo genet, som koder for L- gulonolactone oxidase, er således særdeles konserveret på tværs mange taxa . Grunden til, at der ikke findes rester af gulo -genet i teleostiergenomet, er enten, at pseudogenet muterede til ukendelighed i løbet af de 200 millioner år, eller at genet blev slettet .
Passerines (Passeriformes)


Passerinefuglenes rækkefølge (Passeriformes) er en forholdsvis ung taxon fra et evolutionært synspunkt . Nogle arter er ikke i stand til selv at syntetisere ascorbinsyre. Andre syntetiserer ascorbinsyre i leveren og ikke som i mange andre fuglearter i nyrerne. Overgangen til syntese i leveren og tab af funktion hos nogle arter af passerine fugle betragtes af nogle forfattere som "evolutionære fremskridt".
En nærmere undersøgelse af stammens historie gør det klart, at de passeriner, der ikke er i stand til at syntetisere ascorbinsyre, ikke er monofyletiske . Forudsat at manglende evne til at syntetisere ascorbinsyre er passerine -fugles forfædre, blev evnen genvundet fire gange i forskellige slægter og gik tabt igen en gang (i terpsifoner ). På den anden side, hvis man antager, at evnen til at syntetisere ascorbinsyre er forfædretilstanden, så tabtes denne evne tre gange i forskellige slægter og blev genvundet tre gange.
Flagermus (chiroptera)
Efter undersøgelser af flagermusarter Vesperugo abramus og flyver fox slægten Pteroptus fundet, at de ikke kan syntetisere ascorbinsyre, i alt 34 bat arter fra 6 forskellige blev familier undersøgt i detaljer for denne evne i 1976 . Efter at der ikke blev fundet nogen gulo -aktivitet hos disse dyr, blev den for tidlige konklusion i 1976, at dette generelt var tilfældet med flagermus. Denne antagelse skulle revideres i 2011: For flyvende rævart Rousettus leschenaultii og flagermusarten Himalaya rundbladet næse ( Hipposideros armiger ) fandt man overraskende, at gulo- genet ikke er et pseudogen hos disse dyr . Med et flagermus-specifikt polyklonalt gulo- antistof blev L -gulonolactonoxidase endelig påvist i disse to flagermusarter- de er derfor i stand til at producere ascorbinsyre. Sammenlignet med en mus reduceres produktionen af L- gulonolactonoxidase med en faktor seks eller fire. Baseret på flagermusens fylogeni , som er almindeligt accepteret i dag, kan det konkluderes, at det oprindeligt inaktive gulo -gen blev reaktiveret evolutionært i disse to arter . I modsætning til teleosts er dette for eksempel muligt, fordi sekvensen af gulo- genet er meget godt bevaret i begge arter og kun adskiller sig en smule fra gulopositive pattedyr. Genaktiveringen af genet krævede sandsynligvis kun mutationer i områder, der er involveret i regulering af genets ekspression. Det faktum, at aktiviteten er signifikant lavere end musens, tyder på, at yderligere mutationer ville være nødvendige for at øge ekspressionshastigheden. På den anden side kan den videre evolutionære udvikling af gulo -genet i disse to arter også forløbe i præcis den modsatte retning, nemlig at det er på vej til et ikke længere aktivt pseudogen. Når Kalong -Flughund ( Pteropus vampyrus ), som er gulo -negativ, var i exons genom 3 til 8 samt 11 og 12 fundet. Sekvensen er fri for indeler og stopkodoner , så genstrukturen stadig stort set er intakt. Den associerede aminosyresekvens har imidlertid otte mutationer på positioner, der er fuldt konserveret i elleve andre pattedyrarter. Det antages derfor, at selvom dette gen muligvis udtrykkes, er genproduktet - L -gulonolactonoxidase - ikke funktionelt. Gulo -genets tilstand i Kalong flyvende ræv er muligvis et eksempel på et gen, der ikke længere kan genaktiveres i løbet af udviklingen, fordi for mange omvendte mutationer ville være nødvendige. Ændringerne i flagermusernes gulo -gen er relativt nyere i evolutionære termer. For eksempel fandt funktionstabsmutationen i slægten Pteropus kun sted for omkring 3 millioner år siden.
Marsvin (Caviidae)
Marsvin er gulo-negative, og denne egenskab er forbundet med en særlig episode i sygehistorien: Allerede i 1907 opdagede de to norske læger Axel Holst og Theodor Frølich, at marsvin udvikler et klinisk billede med en bestemt kost, der udelukkende bestod af korn eller brød svarer til skørbug hos mennesker. For første gang lykkedes det dem specifikt at overføre C -vitamin -mangelsygdommen til et forsøgsdyr . Derudover kunne de vise, at forsøgsdyrene ikke blev syge med en ensidig kost med hvidkål , gulerødder eller mælkebøtter . Hvis de lod foderhavre eller byg spire på forhånd, blev marsvinene heller ikke syge. Hvis de tørrede det spirede korn før fodring eller opvarmede det til 37 ° C, tabte skørbugsegenskaberne igen. Med deres forsøg lykkedes det Holst og Frølich at bevise, at skørbugt er en mangelsygdom . 19 år efter Holst og Frølichs forsøg blev ascorbinsyre opdaget af Albert von Szent-Györgyi Nagyrápolt .
Ved sammenlignende sekvens analyser af Gulo genet af rotter, mus og marsvin, begyndende fra et punkt i tid af separation ( divergens tid ) af marsvine linje (svarer til den store gruppe af porcupine slægtninge ) fra rotte-muse linje (svarer til den store gruppe bever-slægtninge , musefamilier og flyvende egern ) ved cirka 72 mya er tidspunktet for funktionstabsmutationen af gulo- genet i marsvin dateret til cirka 14 mya. Den forholdsvis unge alder og typen af andre mutationer i gulo- pseudogenet viser klart, at dette tab af funktion må være opstået uafhængigt af det hos andre pattedyr, for eksempel tørnæsede primater. I marsvin gulo pseudogen, exons 1 og 5 var fuldstændig tabt og exon 6 delvist tabt, mens i de tørre næser primater gik syv af de oprindelige tolv exons tabt. Den type første mutation, der førte til tab af funktion af L- gulonolactonoxidase, er stadig helt uklar hos både marsvin og primater med tør næse.
ODS -rotter og sfx -mus
ODS-rotter ( Osteogenic Disorder Shionogi ) er en muteret stamme af albino-rotter ( Wistar-rotter ), hvor funktionen af L- gulonolactonoxidase er gået helt i stå på grund af en punktmutation . En enkelt GA-mutation ( guanin versus adenin ) i nukleotid 182 i genproduktet fører til, at aminosyren cystein i position 61 i L- gulonolactonoxidase erstattes af tyrosin , hvilket fører til fuldstændigt tab af funktion (mutation af funktion) ) af oxidasekonsekvensen.
I 2000 blev en musestamme først rapporteret at være tilbøjelig til spontane brud. Hos disse dyr, kendt som sfx -mus ( spontane knoglebrud ), blev en genetisk defekt på kromosom 14 oprindeligt fundet årsagen. I 2005 blev det opdaget, at det var en sletning af gulo -genet på dette kromosom. Hvis sfx -mus modtager en tilstrækkelig mængde C -vitamin i deres kost, går tendensen til spontane knoglebrud tabt.
Ud over marsvin bruges ODS -rotter og sfx -mus som modelorganismer , især til forsøg med C -vitaminmetabolisme.
Primater med tør næse (Haplorhini)
Generelt

I øjeblikket (2013) antages det, at tabet af gulos funktion i tørnæse -primaterne (Haplorhini) fandt sted for omkring 74 til 61 millioner år siden, relativt kort tid efter linjen af tørnæsede primater (gamle aber, nye verdens aber og nisser lemurer) adskilt fra lemurlinjen (77,5 mya).
Da funktionsløse pseudogener ikke er udsat for selektionstryk, og mutationer i disse gener ikke har nogen evolutionær fordel eller ulempe for den pågældende organisme, viser de typisk en høj mutationshastighed. Ved at sammenligne identiske gensegmenter kan relationer mellem individuelle udviklingslinjer for tørnæsede primater derfor analyseres. I 1999 sammenlignede en japansk forskningsgruppe et gensegment med 164 basepar på exon 10 af GuloP i flere primater. Jo færre basepar i dette afsnit er forskellige, når man sammenligner to arter, jo tættere er de i familie med hinanden. For chimpanser, menneskers nærmeste slægtninge, er forskellene i GuloP -genet hos mennesker faktisk de mindste.
For den amerikanske biolog Jerry Coyne er GuloP et af de vigtigste beviser for evolution og et argument mod såkaldt " intelligent design ". Tabet af Gulos funktion og mutationsforskellene mellem primaterne, som korrelerer med deres grad af forhold, kan efter hans mening kun forklares af denne arts udvikling og fælles forfædre. Coyne spørger blandt andet, hvorfor en "designer" ville inkorporere en mekanisme til ascorbinsyresyntese hos mennesker, men derefter slukke den igen ved at ændre et af de gener, der er ansvarlige for det.
"Hvorfor ville en skaber lægge en vej til fremstilling af C -vitamin i alle disse arter og derefter deaktivere det?"
Mennesker ( homo sapiens )
GuloP er en af omkring 80 pseudogener, der hidtil er fundet og karakteriseret hos mennesker. Det er placeret på kromosom 8 gen locus 21.1. GuloP består af omkring seks exoner , hvoraf ingen kode. Det betyder, at dette gen ikke fungerer som en skabelon for biosyntesen af et protein, der svarer til den genetiske kode - enzymet L -gulonolactonoxidase - hvorfor det kaldes et pseudogen. Til sammenligning består det fuldt funktionelle gulo -gen hos rotter af tolv exoner. Afskriftens længde hos mennesker er 748 basepar. Af de tolv exoner i rotte -gulo -genet findes kun eksoner 7, 9, 10 og 12. Hos mennesker findes eksoner 8 og 11 sandsynligvis deletion . Det høje antal mutationer, der generelt er typisk for pseudogener, findes i de opnåede exoner.
Indtil 1970'erne var der spekulationer om, at visse befolkninger - især eskimoer - måske kunne syntetisere ascorbinsyre i deres kroppe. Af den daglige kost, som dengang næsten udelukkende bestod af fisk og kød, så det ud til, at det daglige behov for C -vitamin ikke kunne dækkes. I dag ved vi, at eskimoer - som alle andre mennesker - ikke har nogen L -gulonolactonoxidase i deres organisme og derfor ikke kan syntetisere ascorbinsyre. Tilberedningen af kød, ofte rå, men højst kun mildt kogt, sikrer, at C -vitaminet i det stort set bevares. I dag antages det, at omkring 15 til 20 mg C -vitamin absorberes gennem den daglige kost. En mængde, der er høj nok til at forhindre skørbug. Derudover er der reelle C -vitaminforøgelser ved at spise rå sæl eller rensdyrlever . Forbrug af mængder omkring 100 gram er tilstrækkeligt til at dække det daglige behov for C -vitamin. Af eskimoer er muktuk ( hvalskind ) meget værdsat, og dette længe før du kunne demonstrere et højt indhold af C -vitamin ved analyse. Maktaaq indeholder omkring 35 mg C -vitamin pr. 100 gram - en højere koncentration af C -vitamin end nogle citrusfrugter har. Alt i alt antages det, at en eskimo med traditionel kost indtager omkring 40 mg C -vitamin om dagen.
Årsager til tab af funktion
Fra et evolutionært synspunkt kunne kun disse arter miste funktionen af L- gulonolactonoxidase, hvis de permanent indtager tilstrækkelige mængder ascorbinsyre gennem deres kost. Ellers ville en funktionstabsmutation i Gulo være en betydelig selektionsulempe. Alle dyrearter, der ikke er i stand til selv at producere ascorbinsyre, spiser naturligvis rige på C -vitamin. Dette viser undersøgelser af forskellige arter, der er gulo -negative. Mens den anbefalede daglige dosis C -vitamin til voksne i USA er 1 mg pr. Kg legemsvægt pr. Dag, i naturen, for eksempel gorillaer 20 til 30, indtager pelshyleaber 88 og Geoffroys edderkoppeaber 106 mg C -vitamin kg kropsvægt pr. dag. Den jamaicanske frugtflagermus ( Artibeus jamaicensis ) når endda en værdi på 258 mg / kg / dag. En anden indikation på den manglende selektionstryk hos Gulo-negative arter er, at disse dyr har meget forskellige, men altid C-vitaminrige kostvaner. Omvendt er der endnu ikke fundet nogen gulo-negative arter, der har en lavt vitamin C-diæt, for eksempel gennem det eksklusive forbrug af plantefrø. Et overskud af ascorbinsyre gennem kroppens egen syntese, ud over ascorbinsyre, der indtages gennem mad, synes ikke at tilbyde nogen selektionsfordel. At supplere den normale C-vitaminrige kost med C-vitamin har ingen positive virkninger på marsvin. Udvælgelsestrykket hos mange hvirveldyr er naturligvis meget lille for både tab og genopretning af gulo -aktivitet.
Den to gange Nobelprisvinder Linus Pauling behandlede intensivt spørgsmålet om, hvorfor nogle arter kunne miste evnen til at syntetisere ascorbinsyre, selvom dette potentielt er så vigtigt. Han fremsatte tesen for mennesker om, at en direkte, tidlig forfader til mennesker levede for omkring 25 millioner år siden i et område, hvor kosten af denne dyreart var rig på ascorbinsyre. På grund af en mutation er kroppens evne til at syntetisere ascorbinsyre gået tabt. Muligvis skete dette på grund af tab af funktion af et enzym. Da der var tilstrækkeligt C -vitamin tilgængeligt gennem kosten, havde denne mutation ikke kun ingen negative virkninger, men betød tværtimod en udvælgelsesfordel. Dette skyldtes, at disse mutanter ikke længere behøvede at investere ressourcer i konstruktionen og driften af ascorbinsyrebiosyntesen.
"Disse mutantdyr ville i det miljø, der gav en rigelig forsyning af ascorbinsyre, have en fordel i forhold til de ascorbinsyreproducerende dyr, idet de var blevet befriet for byrden ved at konstruere og betjene maskineriet til produktion af ascorbinsyre."
Energien frigivet ved tabet af ascorbinsyresyntese var nu tilgængelig for de berørte organismer til andre formål, hvilket gav dem en fordel i forhold til ikke-mutanterne. Med denne tilgang fulgte Pauling stort set livshistorisk teori og mindre-er-mere hypotesen. Sidstnævnte siger, at genetiske tab spiller en vigtig rolle i evolutionen og kan betyde en evolutionær fordel.
Askorbinsyre regulerer hypoxi-induceret faktor 1α (HIF-1α) i højere organismer . Med øgede ascorbinsyreniveauer reduceres produktionen og aktiviteten af HIF-1α betydeligt. Når den aktiveres, opregulerer HIF-1α ekspressionen af hundredvis af stressgener . Fra disse eksperimentelle observationer blev hypotesen udviklet om, at organismer, der har mistet evnen til at syntetisere ascorbinsyre, har en evolutionær fordel, fordi de kan regulere HIF-1α-aktivitet via den eksogene optagelse af ascorbinsyre. Hvis tilførslen af ascorbinsyre er tilstrækkelig, er transkriptionsfaktoren HIF-1α mindre aktiv end i tilfælde af et ascorbinsyreunderskud. På denne måde er organismen naturligvis i stand til at genkende forsyningsstatus for ascorbinsyre. Fra undersøgelser af andre pseudogener vides det, at selvom de ikke leverer genprodukter (= proteiner), har de vigtige epigenetiske funktioner i ekspressionen af andre gener. Hvilken rolle GuloP spiller i dette, og om det giver en evolutionær fordel, er stadig stort set ukendt.
En anden hypotese antager, at fordelen ved ascorbinsyre selvforsyning ikke opvejer ulemperne ved ascorbinsyresyntese. Ved oxidation af L- gulonolacton katalyseret af L- gulonolactonoxidase dannes hydrogenperoxid som et biprodukt. For et molekyle af den producerede antioxidant ascorbinsyre produceres ét molekyle af oxidationsmidlet hydrogenperoxid. Dette øger igen oxidativ stress og behovet for glutathion i cellerne, der producerer ascorbinsyre. Sammen med ascorbinsyre er glutathion den vigtigste intracellulære antioxidant. Efter denne hypotese, med en tilstrækkelig tilførsel af eksogen ascorbinsyre, var tabet af L- gulonolactonoxidase-aktivitet en evolutionær fordel. Imod denne hypotese taler imidlertid det faktum, at Gulo -genet er muteret tilbage i nogle arter . Ifølge den nuværende status (2013) er det mere sandsynligt, at mangfoldigt tab og genopretning af ascorbinsyresyntesen er utilsigtet, som det kan forventes for en neutral egenskab. Denne egenskab er imidlertid kun neutral, så længe der er tilstrækkeligt C -vitamin i kosten.
Tab af funktion af L- gulonolactonoxidase fører til en begrænsning af kosten. Især for tørnæberne antages det, at funktionstabet førte til yderligere udvikling af sensoriske evner, ændringer i adfærd og ændringer i stofskifte for bedre at kunne tilpasse sig den nødvendige kost. Dette kan have ført til udviklingen af trikromatisk syn hos aber , hvilket giver en evolutionær fordel til fodring efter mad, blandt andet til farvedifferentiering af frugter.
Individuelle beviser
- ↑ a b c d Gerald F. Combs: Vitaminerne. 4. udgave, Academic Press, 2012, ISBN 0-12-381981-4 , s. 236. Begrænset forhåndsvisning i Google bogsøgning .
- ^ PL Conklin: Nylige fremskridt inden for rolle og biosyntese af ascorbinsyre i planter. I: Anlæg, celle og miljø. Bind 24, 2001, s. 383-394, doi: 10.1046 / j.1365-3040.2001.00686.x .
- ^ RD Hancock, D. McRae et al.: Syntese af L-ascorbinsyre i floemet. I: BMC plantebiologi. Bind 3, november 2003, s. 7, doi: 10.1186 / 1471-2229-3-7 , PMID 14633288 , PMC 317296 (fri fuld tekst).
- ↑ a b c d e IB Chatterjee: Evolution og biosyntese af ascorbinsyre. I: Videnskab. Bind 182, nummer 4118, december 1973, s. 1271-1272, PMID 4752221 .
- ↑ a b c d e D. Glaubitz: Ascorbinsyre og ascorbinsyresyntese hos hvirvelløse dyr - en sammenlignende analyse. Afhandling, Free University of Berlin, 2004, s. 1–20.
- ↑ N. Smirnoff, PL Conklin, FA Loewus: Biosyntese af ascorbinsyre i planter: en renæssance. I: Årlig gennemgang af plantefysiologi og plantemolekylærbiologi. Bind 52, juni 2001, s. 437-467, doi: 10.1146 / annurev.arplant.52.1.437 , PMID 11337405 .
- ^ GL Wheeler, MA Jones, N. Smirnoff: Den biosyntetiske vej for C -vitamin i højere planter. I: Naturen. Bind 393, nummer 6683, maj 1998, s. 365-369, doi: 10.1038 / 30728 , PMID 9620799 .
- ^ CL Linster, TA Gomez et al.: Arabidopsis VTC2 koder for en GDP-L-galactosefosforylase, det sidste ukendte enzym i Smirnoff-Wheeler-vejen til ascorbinsyre i planter. I: Journal of biologisk kemi. Bind 282, nummer 26, juni 2007, s. 18879-18885, doi: 10.1074 / jbc.M702094200 , PMID 17462988 , PMC 2556065 (fri fuld tekst).
- ↑ V. Locato, S. Cimini, LD Gara: Strategier for at øge C -vitamin i planter: fra planteforsvarsperspektiv til fødevarebiofortifikation. I: Grænser i plantevidenskab. Bind 4, 2013, s. 152, doi: 10.3389 / fpls.2013.00152 , PMID 23734160 , PMC 3660703 (fri fuld tekst).
- ^ IB Chatterjee, GC Chatterjee et al.: Biologisk syntese af L-ascorbinsyre i dyrevæv: omdannelse af D-glucuronolacton og L-gulonolacton til L-ascorbinsyre. I: The Biochemical journal. Bind 76, august 1960, s. 279-292, PMID 13692610 , PMC 1204705 (fri fuld tekst).
- ^ John MC Gutteridge, Naoyuki Taniguchi: Eksperimentelle protokoller for reaktivt ilt og nitrogenarter , 2000, Oxford University Press, ISBN 0-19-850668-6 .
- ^ N. Smirnoff: L-ascorbinsyre biosyntese. I: Vitaminer og hormoner. Bind 61, 2001, s. 241-266, PMID 11153268 (anmeldelse).
- ^ F. Puskás, L. Braun et al.: Gulonolactonoxidase-aktivitetsafhængig intravesikulær glutathionoxidation i rotterlevermikrosomer. I: FEBS breve. Bind 430, nummer 3, juli 1998, s. 293-296, PMID 9688558 .
- ↑ a b G. Bánhegyi, M. Csala og andre: Ascorbatsynteseafhængigt glutathionforbrug i muselever. I: FEBS breve. Bind 381, nummer 1-2, februar 1996, s. 39-41, PMID 8641435 .
- ↑ a b K. Kiuchi, M. Nishikimi, K. Yagi: Oprensning og karakterisering af L-gulonolactonoxidase fra hønsenyremikrosomer. I: Biokemi. Bind 21, nummer 20, september 1982, s. 5076-5082, PMID 7138847 .
- ↑ M. Nishikimi, BM Tolbert, S. Udenfriend: Oprensning og karakterisering af L-gulono-gamma-lacton oxidase fra rotte og gedelever. I: Arkiver for biokemi og biofysik. Bind 175, nummer 2, august 1976, s. 427-435, PMID 822334 .
- ↑ GL Eliceiri, EK Lai, PB McCay: Gulonolactone oxidase. Solubilisering, egenskaber og delvis oprensning. I: J Biol Chem. Bind 244, nummer 10, 1969, s. 2641-2645, PMID 5769996 .
- ^ A b CL Linster, E. Van Schaftingen: Vitamin C. Biosyntese, genbrug og nedbrydning hos pattedyr. I: FEBS journal. Bind 274, nummer 1, januar 2007, s. 1-22, doi: 10.1111 / j.1742-4658.2006.05607.x , PMID 17222174 (anmeldelse).
- ↑ T. Koshizaka, M. Nishikimi et al:. Isolering og sekvensanalyse af en komplementær DNA, der koder rottelever L-gulono-gamma-lacton oxidase, et nøgleenzym for L-ascorbinsyre-biosyntese. I: J Biol Chem. Bind 263, nummer 4, 1988, s. 1619-1621, PMID 3338984 .
- ↑ SZ Wong, B. Ching et al.: Ascorbinsyre-biosyntese og brakvandsklimatisering i Euryhaline ferskvand hvid-kantet stingray, Himantura signifer. I: PloS en. Bind 8, nummer 6, 2013, s. E66691, doi: 10.1371 / journal.pone.0066691 , PMID 23825042 , PMC 3688944 (fri fuld tekst).
- ^ SD Gupta, C. Sen Gupta et al.: Enzymisk syntese af L-ascorbinsyre fra syntetiske og biologiske D-glucurono-1,4-lactonkonjugater. I: Analytisk biokemi. Bind 38, nummer 1, november 1970, s. 46-55, PMID 5478251 .
- ^ EC Birney, R. Jenness, HD Hume: Evolution af et enzymsystem: ascorbinsyrebiosyntese i monotremer og pungdyr. I: evolution. Nummer 34, 1980, s. 230-239.
- ↑ a b c d e f g h i j k l m n o p q r G. Drouin, JR Godin, B. Pagé: Genetikken ved tab af C -vitamin hos hvirveldyr. I: Nuværende genomik. Bind 12, nummer 5, august 2011, s. 371-378, doi: 10.2174 / 138920211796429736 , PMID 22294879 , PMC 3145266 (fri fuld tekst).
- ↑ a b IB Chatterjee, AK Majumder et al.: Syntese og nogle hovedfunktioner af C -vitamin hos dyr. I: Annaler fra New York Academy of Sciences. Bind 258, september 1975, s. 24-47, PMID 1106297 (anmeldelse).
- ↑ a b J. Cui, YH Pan et al.: Progressiv pseudogenisering: C -vitamin syntese og dets tab hos flagermus. I: Molekylær biologi og evolution. Bind 28, nummer 2, februar 2011, s. 1025-1031, doi: 10.1093 / molbev / msq286 , PMID 21037206 .
- ↑ L. Hasan, P. Vögeli et al.: L-gulono-gamma-lactonoxidase-genet (GULO), som er en kandidat til C-vitaminmangel hos grise, der kortlægger til kromosom 14. I: Animal genetics. Bind 30, nummer 4, august 1999, s. 309-312, PMID 10467707 .
- ^ RH Dadd: Ascorbinsyre og caroten i ernæringen af ørkenhoppe, Schistocera gregaria Forsk. I: Nature Volume 179, 1957, s. 427, doi: 10.1038 / 179427a0 .
- ↑ G. Niedźwiedzki, P. Szrek et al:. Tetrapod trackways fra den tidlige Mellemøsten Devon periode Polen. I: Naturen. Bind 463, nummer 7277, januar 2010, s. 43-48, doi: 10.1038 / nature08623 , PMID 20054388 .
- ↑ a b A. Nandi, CK Mukhopadhyay et al.: Evolutionær betydning af C -vitamin biosyntese i terrestriske hvirveldyr. I: Fri radikal biologi og medicin. Bind 22, nummer 6, 1997, s. 1047-1054, PMID 9034244 .
- ^ AW Bacot, A. Harden: Vitaminkrav til Drosophila. I vitamin B og C. I: The Biochemical journal. Bind 16, nummer 1, 1922, s. 148-152, PMID 16743060 , PMC 1259065 (fri fuld tekst).
- ↑ ES Vanderzant, R. Reiser: Aseptisk opdræt af den lyserøde frøkapselorm på syntetiske medier. I: Journal of Economic Entomology. Bind 49, 1956, s. 7-10.
- ↑ GC Rock: Aseptisk opdræt af codling møl på syntetiske kostvaner: krav til ascorbinsyre og fedtsyrer. I: Journal of Economic Entomology. Bind 60, 1967, s. 1002-1005.
- ↑ DE Dykhuizen, KM Harrison, BJ Richardson: Evolutionary virkninger af ascorbinsyre produktion i den australske lungefisk. I: Experientia. Bind 36, nummer 8, august 1980, s. 945-946, PMID 7439328 .
- ^ YK Nam, YS Cho et al.: Isolering og forbigående ekspression af et cDNA, der koder for L-gulono-gamma-lactonoxidase, et centralt enzym for L-ascorbinsyrebiosyntese, fra tigerhajen Scyliorhinus torazame. I: Akvakultur. Bind 209, 2002, s. 271-284, doi: 10.1016 / s0044-8486 (01) 00731-1 .
- ↑ DM Fracalassi, ME Allen et al:. Ascorbinsyre biosyntese i Amazonas fisk. I: Akvakultur. Bind 192, 2001, s. 321-332, doi: 10.1016 / S0044-8486 (00) 00455-5 .
- ^ R. Moreau, K. Dabrowski: Fisk erhvervet ascorbinsyresyntese før fremkomsten af terrestriske hvirveldyr. I: Fri radikal biologi og medicin. Bind 25, nummer 8, november 1998, s. 989-990, PMID 9840745 .
- ^ R. Moreau, K. Dabrowski: Kropspulje og syntese af ascorbinsyre i voksen havlampe (Petromyzon marinus): en agnathanfisk med gulonolactonoxidaseaktivitet. I: PNAS. Bind 95, nummer 17, august 1998, s. 10279-10282, PMID 9707638 , PMC 21499 (fri fuld tekst).
- ^ YS Cho, SE Douglas et al.: Isolering og karakterisering af cDNA-sekvenser af L-gulono-gamma-lactonoxidase, et centralt enzym for biosyntese af ascorbinsyre, fra eksisterende primitive fiskegrupper. I: Sammenlignende biokemi og fysiologi. Del B, biokemi og molekylærbiologi. Bind 147, nummer 2, juni 2007, s. 178-190, doi: 10.1016 / j.cbpb.2007.01.001 , PMID 17317254 .
- ^ A b R. Moreau, K. Dabrowski: Biosyntese af ascorbinsyre af eksisterende actinopterygians. I: J Fish Biol. Bind 57, 2000, s. 733-745, doi: 10.1111 / j.1095-8649.2000.tb00271.x .
- ^ K. Dabrowski: Primitive aktinopterigiske fisk kan syntetisere ascorbinsyre. I: Experientia. Bind 50, nummer 8, 1994, s. 745-748, doi: 10.1007 / BF01919376 .
- ↑ a b c MY Lachapelle, G. Drouin: Inaktiveringsdatoer for humane og marsvin C -vitamin -gener. I: Genetica. Bind 139, nummer 2, februar 2011, s. 199-207, doi: 10.1007 / s10709-010-9537-x , PMID 21140195 .
- ↑ a b C. Martinez del Rio: Kan Passerines syntetisere C -vitamin? I: The Auk. Bind 114, nummer 3, s. 513-516, doi: 10.2307 / 4089257 .
- ^ CR Chaudhuri, IB Chatterjee: L-ascorbinsyresyntese hos fugle: fylogenetisk tendens. I: Videnskab. Bind 164, nummer 3878, april 1969, s. 435-436, PMID 5777214 .
- ^ EC Teeling, MS Springer et al.: En molekylær fylogeni for flagermus belyser biogeografi og fossilrekorden. I: Videnskab. Bind 307, nummer 5709, januar 2005, s. 580-584, doi: 10.1126 / science.1105113 , PMID 15681385 .
- ^ S. Dutta Gupta, PK Choudhury, IB Chatterjee: Syntese af l-ascorbinsyre fra d-glucurono-1,4-lacton-konjugater af forskellige dyrearter. I: International Journal of Biochemistry. Bind 4, nummer 21, 1973, s. 309-314, doi: 10.1016 / 0020-711X (73) 90053-0 .
- ↑ RN ROY, BC Guha: Arter forskel med hensyn til biosyntesen af ascorbinsyre. I: Naturen. Bind 182, nummer 4631, august 1958, s. 319-320, PMID 13577829 .
- ↑ a b EC Birney, R. Jenness, KM Ayaz: Flagermusers manglende evne til at syntetisere L-ascorbinsyre. I: Naturen. Bind 260, nummer 5552, april 1976, s. 626-628, PMID 1264230 .
- ^ J. Cui, X. Yuan et al.: Seneste tab af C -vitamin biosyntese evne hos flagermus. I: PloS en. Bind 6, nummer 11, 2011, s. E27114, doi: 10.1371 / journal.pone.0027114 , PMID 22069493 , PMC 3206078 (fri fuld tekst).
- ↑ A. Holst, T. Frölich: Eksperimentelle undersøgelser vedrørende skib beri-beri til skørbugt. II. Om skørbugs ætiologi. I: Journal of Hygiene. Bind 7, 1907, s. 634-671, PMID 4606855 .
- ↑ Adolphe-Auguste Lesage, Rudolf Fischl: Lærebog om spædbarns sygdomme. Georg Thieme, 1912, s. 375.
- ↑ H. Schaumann : Etiologien i Beriberi II. Kapitel 3: Utilstrækkelig mad. Arkiv for skibe og tropisk hygiejne, 1914, s. 125. Begrænset forhåndsvisning i Google bogsøgning.
- ↑ Tina König: Udvikling af ernæringsforskning hos grise (indtil 1930). (PDF; 3,6 MB) Afhandling, University of Veterinary Medicine Hannover, 2004, s.165.
- ↑ Wolfgang Schaumann: Charles Darwin-Life and Work John Wiley & Sons, 2012, ISBN 3-527-66072-0 , s. 51. Begrænset forhåndsvisning i Google bogsøgning .
- ↑ a b PH Fabre, L. Hautier et al.: Et glimt af mønsteret for diversificering af gnavere: en fylogenetisk tilgang. I: BMC Evolutionær Biologi. Bind 12, 2012, s. 88, doi: 10.1186 / 1471-2148-12-88 , PMID 22697210 , PMC 3532383 (fri fuld tekst).
- ↑ a b T. Kawai, M. Nishikimi et al.: En missense-mutation af L-gulono-gamma-lactonoxidase bevirker, at skørbøjs-tilbøjelige osteogene lidelser rotter ikke kan syntetisere L-ascorbinsyre. I: Journal of biologisk kemi. Bind 267, nummer 30, oktober 1992, s. 21973-21976, PMID 1400508 .
- ↑ en b M. Nishikimi, R. Fukuyama et al:. Kloning og kromosomal kortlægning af det humane ikke-funktionelle gen for L-gulono-gamma-lacton oxidase, enzymet for L-ascorbinsyre biosyntese mangler i mennesket. I: Journal of biologisk kemi. Bind 269, nummer 18, maj 1994, s. 13685-13688, PMID 8175804 .
- ^ F. Horio, K. Ozaki et al.: Krav til ascorbinsyre i en rotte mutant ude af stand til at syntetisere ascorbinsyre. I: Journal of Nutrition. Bind 115, nummer 12, december 1985, s. 1630-1640, PMID 4067654 .
- ^ F. Horio, K. Ozaki et al.: Krav til askorbinsyre til induktion af mikrosomale lægemiddelmetaboliserende enzymer i en rotte mutant ude af stand til at syntetisere ascorbinsyre. I: Journal of Nutrition. Bind 116, nummer 11, november 1986, s. 2278-2289, PMID 3098936 .
- ^ WG Beamer, CJ Rosen et al.: Spontan fraktur (sfx): en mus genetisk model for defekt peripubertal knogledannelse. I: Ben. Bind 27, nummer 5, november 2000, s. 619-626, PMID 11062347 .
- ^ Y. Jiao, X. Li et al.: En sletning, der forårsager spontan fraktur identificeret fra en kandidatregion af musekromosom 14. I: Pattedyrs genom. Bind 16, nummer 1, januar 2005, s. 20-31, doi: 10.1007 / s00335-004-2414-0 , PMID 15674730 .
- ^ A b Y. Jiao, J. Zhang et al.: Differentiel genekspression mellem vildtype- og Gulo-mangelfulde mus forsynet med vitamin C. I: Genetik og molekylærbiologi. Bind 34, nummer 3, juli 2011, s. 386-395, doi: 10.1590 / S1415-47572011005000031 , PMID 21931508 , PMC 3168176 (fri fuld tekst).
- ↑ C. VERGELY, F. Goirand et al:. C-vitaminmangel udøver paradoksale cardiovaskulære virkninger i osteogen disorder Shionogi (ODS) rotter. I: Journal of Nutrition. Bind 134, nummer 4, april 2004, s. 729-735, PMID 15051818 .
- ↑ D. Smith, G. Asmundsson et al:. Det osteogene lidelse Shionogi (ODS) rotte: en ny model for studiet af C-vitamin metabolisme. I: United States Department of Agriculture - Agricultural Research Service juni 1995.
- ↑ Y. Ohta, M. Nishikimi: Random nukleotidsubstitutioner i primat-funktionelt gen for L-gulono-gamma-lacton oxidase, de manglende enzym i L-ascorbinsyre-biosyntese. I: Biochimica et Biophysica Acta . Bind 1472, nummer 1-2, oktober 1999, s. 408-411, PMID 10572964 .
- ↑ a b Jerry A. Coyne : Hvorfor Evolution er sand. Oxford University Press, 2009, ISBN 0-19-923084-6 , s. 72-73. begrænset forhåndsvisning i Google Bogsøgning.
- ^ A b X. Wang, WE Grus, J. Zhang: Gentab under menneskelig oprindelse. I: PLoS biologi. Bind 4, nummer 3, marts 2006, s. E52, doi: 10.1371 / journal.pbio.0040052 , PMID 16464126 , PMC 1361800 (fri fuld tekst).
- ^ ZD Zhang, A. Frankish et al.: Identifikation og analyse af unitære pseudogener: historiske og nutidige gentab hos mennesker og andre primater. I: Genombiologi. Bind 11, nummer 3, 2010, s. R26, doi: 10.1186 / gb-2010-11-3-r26 , PMID 20210993 , PMC 2864566 (fri fuld tekst).
- ↑ GULOP .
- ↑ Gene database for National Center for Biotechnology Information (NCBI): GULOP gulonolactone (L-) oxidase, pseudogen (Homo sapiens (menneske)) . Tilgænglig september 1, 2013.
- ↑ Ensembl : Udskrift: GULOP-001 ENST00000454030 Adgang til 1. september 2013.
- ^ L-gulonolactonoxidase. I: Online Mendelsk arv i mennesket . (Engelsk).
- ^ RA Gibson, AJ Sinclair: Er eskimoer obligatoriske kødædere? I: Lancet. Bind 1, nummer 8229, maj 1981, s. 1100, PMID 6112464 .
- ↑ a b Kenneth J. Carpenter: The History of Scurvy and Vitamin C. Cambridge University Press, 1988, ISBN 0-521-34773-4 , s. 231. Begrænset forhåndsvisning i Google bogsøgning .
- ^ JR Geraci, TG Smith: C -vitamin i kosten af inuitjægere fra Holman, nordvestlige territorier. (PDF; 288 kB) I: Arctic. Bind 32, nummer 2, 1979, s. 135-139.
- ↑ K. Fediuk, N. Hidiroglou et al:. C-vitamin i Inuit traditionelle fødevarer og kvinders kostvaner. I: Journal of Food Composition and Analysis. Bind 15, nummer 3, 2002, s. 221-235, doi: 10.1006 / jfca.2002.1053 .
- ^ K. Milton, R. Jenness: Ascorbinsyreindhold i neotropiske plantedele til rådighed for vilde aber og flagermus. I: Experientia. Bind 43, nummer 3, marts 1987, s. 339-342, PMID 3104078 .
- ^ JI Pollock, RJ Mullin: C -vitamin biosyntese hos prosimians: bevis for Tarsius 'antropoide affinitet. I: Amerikansk tidsskrift for fysisk antropologi. Bind 73, nummer 1, maj 1987, s. 65-70, doi: 10.1002 / ajpa.1330730106 , PMID 3113259 .
- ^ M. Levine: Nye begreber inden for ascorbinsyres biologi og biokemi. I: The New England Journal of Medicine . Bind 314, nummer 14, april 1986, s. 892-902, doi: 10.1056 / NEJM198604033141407 , PMID 3513016 (anmeldelse).
- ^ A b Tom Hager: Linus Pauling: Og livets kemi. Oxford University Press, 2000, ISBN 0-19-513972-0 , s. 122. Begrænset forhåndsvisning i Google Bogsøgning.
- ^ DA Roff: Genomics bidrag til livshistorisk teori. I: Nat Rev Genet 8, 2007, s. 116-125, PMID 17230198 (anmeldelse).
- ↑ NPO: Inkarnation: Fordel ved tab af gener? På: scinexx den 14. januar 2006.
- ^ MV Olson: When less is more: gentab som en motor for evolutionær forandring. I: American Journal of Human Genetics . Bind 64, nummer 1, januar 1999, s. 18-23, doi: 10.1086 / 302219 , PMID 9915938 , PMC 1377697 (gratis fuld tekst) (anmeldelse).
- ^ HJ Knowles, RR Raval et al.: Virkning af ascorbat på aktiviteten af hypoxi-inducerbar faktor i kræftceller. I: Kræftforskning . Bind 63, nummer 8, april 2003, s. 1764-1768, PMID 12702559 .
- ^ A. Grano, MC De Tullio: Ascorbinsyre som en sensor for oxidativt stress og en regulator for genekspression: Yin og Yang af vitamin C. I: Medicinske hypoteser . Bind 69, nummer 4, 2007, s. 953-954, doi: 10.1016 / j.mehy.2007.02.008 , PMID 17376607 .
- ^ A b MC De Tullio: Mysteriet om vitamin C. I: Naturundervisning. Bind 3, nummer 9, 2010, 48.
- ↑ L. Poliseno, L. Salmena et al:. A-kodende-uafhængig funktion af gen og pseudogendonorer mRNA'er regulerer tumorbiologi. I: Naturen. Bind 465, nummer 7301, juni 2010, s. 1033-1038, doi: 10.1038 / nature09144 , PMID 20577206 , PMC 3206313 (fri fuld tekst).
- ^ B. Halliwell: C -vitamin og genomisk stabilitet. I: Mutationsforskning. Bind 475, nummer 1-2, april 2001, s. 29-35, PMID 11295151 (anmeldelse).
- ^ Terrence W. Deacon : En rolle for afslappet valg i udviklingen af sprogkapaciteten. I: John C. Avise , Francisco J. Ayala (red.): I lyset af evolution IV: The Human Condition. Bind 4, National Academy of Sciences , National Academies Press, 2010, ISBN 0-309-18528-9 , s. 287 begrænset forhåndsvisning i Google bogsøgning .