Cyste nyre
| Klassificering i henhold til ICD-10 | |
|---|---|
| Q61.1 | Polycystisk nyre, autosomal recessiv infantil type |
| Q61.2 | Polycystisk nyre, autosomal dominerende voksen type |
| Q61.3 | Uspecificeret polycystisk nyre |
| ICD-10 online (WHO version 2019) | |

Polycystisk nyresygdom , også kendt som polycystisk nyre betegnes ( engelsk nyresygdom polycystisk , PCD er en gruppe af alvorlige, hovedsagelig) arvelige -relaterede sygdomme i nyrerne . På grund af dannelsen af et stort antal væskefyldte kamre eller vesikler (de antikke græske πολύς polys 'meget'), de såkaldte cyster , er nyrerne betydeligt begrænset i deres filtreringsfunktion . En nyrecyste er derimod en enkelt cyste, der normalt nævnes som en uskadelig chance for at finde i løbet af en undersøgelse .
Genetisk bestemte nyrecyster er den mest almindelige livstruende arvelige sygdom hos mennesker og en af hovedårsagerne til kronisk nyresvigt . En kur er kun mulig med en nyretransplantation .
Symptomer
De første symptomer, der kan indikere cystiske nyrer, er forhøjet blodtryk , blodig urin ( hæmaturi ), gentagne urinvejsinfektioner , en stigning i størrelsen på maven og smerter i maven. Så længe nyrerne kan kompensere for eventuelle funktionsnedsættelser, er der ofte ingen symptomer. Cirka en tredjedel af patienterne forbliver symptomfrie , selv indtil det er nyresvigt (ESRF) i slutstadiet . Dette gør en tidlig diagnose meget vanskeligere. Den stigende ødelæggelse af nyrevævet fører til flere og flere klager i forskellige organer på grund af de tilbageholdte affaldsprodukter og vandet. Disse inkluderer nedsat ydeevne og utilpashed, gulfarvning og kløe i huden på grund af de lagrede urintoksiner, søvn- og koncentrationsforstyrrelser, hovedpine, lægkramper, kvalme, opkastning, diarré og smagsforstyrrelser. Højt blodtryk, hjertearytmier eller betændelse og vejrtrækningsproblemer forekommer også. Derudover er der anæmi (på grund af reduktionen af erythropoietin produceret af nyren, som bruges til bloddannelse), koagulationsforstyrrelser, øget modtagelighed for infektioner, cerebral blødning og blødgøring af knoglerne (da nyren også er involveret i D-vitamin stofskifte).
Patienter med polycystisk nyre klager ofte over smerter i den side flanke af deres ryg eller mave . Smerten kan være midlertidig eller permanent, kedelig og ulidelig. Smerten skyldes sandsynligvis den omfattende cyste vækst. Derudover fortrænges de omgivende organer ved ekstrem strækning af nyrekapslen (Capsula fibrosa renalis) .
Smerten kan lindres kortvarigt ved punktering af cyster, for eksempel perkutant , dvs. gennem huden eller minimalt invasivt ved laparoskopisk afkortering af cyster. På grund af dannelsen af nye cyster er disse foranstaltninger ikke bæredygtige, så de tilsvarende interventioner skal gentages. Derudover ændrer behandlingen ikke sygdomsforløbet.
Hos omkring 30 til 50% af patienterne er den indledende diagnose af "polycystiske nyrer" lavet af blodig urin ( hæmaturi ). Årsagen til blødningen er normalt revner i cyster. Selve blødningen er stort set harmløs og stopper af sig selv. På grund af den nedsat nyrefunktion, udskiller patienter med cystisk nyrer øgede mængder af endogene proteiner i den urinen . Hvis kroppen udskiller 30 til 300 milligram albumin om dagen , kaldes det mikroalbuminuri . Hvis endnu større mængder albumin udskilles, kaldes dette makroalbuminuri . Hvis der kan påvises proteiner større end albumin i urinen, er proteinuri til stede. Sidstnævnte kan let detekteres med teststrimler , der holdes i urinen. Mikroalbuminuri er meget sværere at opdage. Protein og mikroalbuminuri er en indikation af nedsat nyrefunktion. Polycystiske nyrer er blot en af flere mulige tilstande, der kan føre til denne dysfunktion.
En arteriel hypertension ("hypertension") er placeret foran patienter med polycystisk nyre med 50 til 75%. Blodtrykket hos de berørte er ofte allerede markant øget før et fald i nyrefunktionen ( glomerulær filtreringshastighed , GFR).
Diagnose

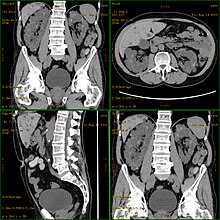
Diagnosen stilles normalt ved sonografi ("ultralyd") eller ved andre billeddannelsesmetoder , såsom magnetisk resonanstomografi . Med ultralyd kan cyster ned til en størrelse på 5 mm diagnosticeres med moderne enheder. Den tidlige påvisningshastighed hos 20-årige patienter er omkring 90%. Selvom computertomografi tilbyder en højere opløsning med bedre billedkvalitet, er det ikke bruges til patientens screeninger , primært på grund af stråling , men kun til særlige diagnostiske spørgsmål.
Den biopsi , hvor en lille mængde af nyre og lever væv fjernes, anvendes i barndommen til skelne mellem ARPKD og ADPKD ( tidligt indtrædende ) . Dette betyder, at morfologiske ændringer i basalmembranen kan påvises på et meget tidligt tidspunkt. ARPKD diagnosticeres ved bestemmelse af medfødt leverfibrose .
Ifølge Osathanondh og Potter er cyste nyrerne patologisk og anatomisk opdelt i følgende typer:
| Type | Infestation | Nyrestørrelse | Cyste størrelse | Glomeruli | Gallekanalcyster | Overlevelsestid |
|---|---|---|---|---|---|---|
| JEG. | begge sider | forstørret til stærkt forstørret | jævnt bred (12 mm) | normal | ledig | Neonatal periode |
| II | dobbeltsidet, ensidet eller delvist | forstørret eller reduceret | forskellige størrelser | formindsket og unormalt | utilgængelig | Voksen alder |
| III | mest bilaterale | forstørret | forskellige størrelser, nogle gange meget langt | glomerulære cyster | lejlighedsvis, men derefter kun i afgrænsede områder | Voksen alder |
| IV | begge sider | Nedskaleret | lille, placeret subcapsularly | Glomeruli formindsket, glomular cyster | utilgængelig | Voksen alder |
I praksis tillader de typer, der er defineret på denne måde, ofte ikke en klar klassificering . Ud over den patoanatomiske beskrivelse af nyrerne og leveren spiller familiens historie ( anamnese ) derfor en vigtig rolle. I arvelige tilfælde af nyrecyster anvendes de genetisk baserede udtryk autosomal - dominerende og autosomal recessiv .
Ved at identificere potentielt berørte gener er en ikke-invasiv demonstrativ molekylær genetisk diagnose mulig. I mange tilfælde kan denne procedure erstatte invasiv biopsidiagnostik og muliggøre etiologisk klassificering. Denne klassificering åbner igen måder for forskellige terapeutiske muligheder for behandling af sygdommen. Den følsomhed for en virkelig positivt resultat er omkring 95%. En sammenhæng mellem genotype og fænotype er kun mulig i begrænset omfang. Mutationsanalyse er vanskelig med PKD1-genet på grund af dets størrelse (46 kodende exoner og 14,2 kb af transkriptet ). Derudover er de første 33 eksoner af PKD1 i tre homologe kopier af det berørte kromosom 16 på gen locus p13.1 (HG-A ~ 21 kb, HG-B ~ 17 kb og HG-C ~ 8,5 kb; HG = homologt gen ) er til stede. Dette gør specifik multiplikation ved hjælp af polymerasekædereaktion (PCR) betydeligt vanskeligere .
Fra den molekylære genetiske diagnose opstår der et særligt problem. Den tidlige diagnose af patientens genetiske disposition muliggør profylaktiske tiltag og tidlig understøttende terapi på den ene side . På den anden side kan pårørende og patienter blive konfronteret med sandsynligheden for, at en livstruende sygdom bryder ud i flere årtier allerede i barndommen. Risici og fordele skal derfor nøje afvejes inden en diagnose.
Hos patienter med en familiær disposition ( disposition ) kan diagnosen stilles ved hjælp af sonografi fra 20 år, hvis der kan påvises mindst to nyrecyster pr. Nyre. Manglende cyster udelukker på den anden side sygdommen hos personer over 30 år.
Patogenese
Oprindelsen og udviklingen af cyste nyrer , patogenesen , er baseret på en cystisk degeneration af de såkaldte tubuli (nyretubuli, også: urinrør) i nyrerne. I tilfælde af autosomal dominant arvet PKD fører dette til en stigende udvidelse af nyrerne i løbet af årtier. Dette kan føre til funktionsnedsættelse eller endda fuldstændigt tab af nyrens filtreringsfunktion. Begge nyrer er lige påvirket. Flere hundrede cyster, som er omfangsrige i deres udseende, kan udvikle sig pr. Organ. Nyrernes masse og volumen kan stige markant som et resultat. Mens en sund nyre har en gennemsnitlig masse på 160 g , kan polycystiske nyrer nå op til 8 kg med et volumen på op til 40 × 25 × 20 cm³ (= 20 liter) (sund nyre: 12 × 6 × 3 cm³ = 0,216 liter ). På trods af det betydeligt øgede pladsbehov for organet opstår funktionelle lidelser i de omkringliggende organer kun relativt sjældent.
Cysterne findes både på renal medulla (medulla renis) og på renal cortex (cortex renalis) . I princippet kan ethvert område af en nefron udvikle en cyste. Imidlertid er glomeruli og Henles sløjfe primært påvirket . Cysterne er fyldt med såkaldt rørformet urin . Diameteren på en enkelt cyste kan variere meget fra nogle få millimeter til over 100 mm. Store cyster kan indeholde flere hundrede milliliter rørformet urin. Indersiden af cysten består af et enkeltlags pladeepitel eller isoprismatisk (kubisk) epitel fra et lag . Efterhånden som sygdommen skrider frem, kan både antallet og størrelsen af de nuværende cyster øges.
etiologi
Polycystiske ændringer i nyrerne er en tilstand, der forekommer i en række sygdomme. De kan opstå sporadisk som en afvigelse fra den normale udvikling af nyrerne eller kan erhverves i voksenlivet (erhvervede cystiske nyrer ) . Den langt mere almindelige årsag ( etiologi ) for denne sygdom er arvelige defekter i visse gener ( arvelige cystiske nyrer ) . Langt den største andel tages af den autosomale dominerende polycystiske nyresygdom ( engelsk autosomal dominerende polycystisk nyresygdom , ADPKD ). Denne sygdom er den mest almindelige arvelige årsag til kronisk nyresvigt : omkring 7% af alle dialysepatienter lider af den.
Derudover forårsager forskellige andre - meget sjældnere - arvelige sygdomme cystiske nyrer. Erhvervede cystiske nyrer kan også udvikle sig, især hos dialysepatienter. Da langt størstedelen af cyste nyrer er forårsaget af ADPKD, bruges udtrykket "cyste nyre" ofte synonymt for ADPKD.
Arvelige cystiske nyrer
Størstedelen af polycystiske nyresygdomme er arvelige ( arvelige ). Et stort antal forskellige gener kan påvirkes og dermed udløse sygdommen. Syndromerne, der er anført nedenfor, repræsenterer et udvalg af de vigtigste arvelige polycystiske nyresygdomme, og nogle af sygdommene er inkluderet i det såkaldte NPH-MCKD-kompleks .
| gen | Kromosomgen locus |
protein | sygdom | Forekomst | Alder ∗) |
|---|---|---|---|---|---|
| Autosomal dominerende | |||||
| PKD1 | 16 s13.3 | Polycystin-1 | ADPKD | 1: 500-1000 | ca. 50 |
| PKD2 | 4 q21-q23 | Polycystin-2 | ADPKD | 1: 3500-7000 | ca. 70 |
| VHL | 3 p26-p25 | VHL30 | Von-Hippel-Lindau | 1: 35.000 | 20-30 |
| TSC1 | 9 q34 | Hamartin | Knoldsklerose | 1: 10.000 (begge sammen) | 30-40 |
| TSC2 | 16 s13.3 | Tuberine | Knoldsklerose | ||
| ? | 1 q21 | Medullær cystisk nyresygdom type 1 | 1 til 9: 1.000.000 (type 1 + 2) | 62 | |
| UMOD | 16 s12.3 | Uromodulin | Medullær cystisk nyresygdom type 2 | 32 | |
| Autosomal recessiv | |||||
| PKHD1 | 6 p21.2-p12 | Fibrocystin | ARPKD | 1: 20.000 | <20 |
| NPHP1 | 2 q13 | Nephrocystine-1 | Nephronophthisis (ung) | ca. 1: 100.000 (alle NPHP) | 13. |
| NPHP2 | 9 q22-q31 | Omvendt | Nephronophthisis (infantil) | <1 | |
| NPHP3 | 3 q22.1 | Nephrocystine-3 | Nephronophthisis (teenager) | 19. | |
| NPHP4 | 1 s36.22 | Nefroretinin | Nephronophthisis | 21 | |
| NPHP5 | Nephrocystine 5 | Nephronophthisis | 13. | ||
| NPHP6 | Nephrocystine 6 | Nephronophthisis | |||
| GLIS2 | 16 s13.3 | GLI-lignende protein 2 | Nephronophthisis | ||
| BBS1 | 11 q13.1 | BBS1 protein | Bardet-Biedl syndrom | 1: 140.000 (alle BBS) | |
| BBS2 | 16 q21 | BBS2 protein | Bardet-Biedl syndrom | ||
| ARL6 | 3 p13-p12 |
BBS3 protein ADP-ribosyleringsfaktor-lignende protein 6 |
Bardet-Biedl syndrom | ||
| BBS4 | 15 q22.3-q23 | BBS4 protein | Bardet-Biedl syndrom | ||
| BBS5 | 2 q31.1 | BBS5 protein | Bardet-Biedl syndrom | ||
| MKKS | 20 p12 | BBS6 protein | McKusick-Kaufman syndrom | ||
| BBS7 | 4 q27 | BBS7 protein | Bardet-Biedl syndrom | ||
| TTC8 | 14 q31.3 | BBS8 protein | Tetratricopeptid Gentag domæne 8 | ||
| BBS9 | 7 p14 | PTHB1 | Bardet-Biedl syndrom | ||
| BBS10 | 12 q21.2 | BBS10 protein | Bardet-Biedl syndrom | ||
| TRIM32 | 9 q33.1 | Zinkfingerprotein HT2A | Trepartsmotiv indeholdende 32 | ||
| BBS12 | 4 q27 | BBS12 protein | Bardet-Biedl syndrom | ||
| X-bundet dominerende | |||||
| CXORF5 | X p22.3-p22.2 | OFD1 | Oro-facio-digitalt syndrom type 1 | 1: 250.000 | |
| Ukendt arv | |||||
| ? | ? | Medullær cyste nyre | 1: 5000 | 40-50 | |
| ? | ? | Multicystisk nyredysplasi | <10 og 50-60 |
Autosomal dominerende polycystisk nyresygdom
Autosomal dominant polycystisk nyresygdom (ADPKD), også kendt som Potter type III cystisk nyredegeneration , er den mest almindelige livstruende arvelige sygdom hos mennesker. Der er cirka 5 millioner mennesker, der er ramt af ADPKD over hele verden. Den Forekomsten er 1: 500 til 1: 1000. For eksempel er det i USA to gange mere almindeligt end multipel sklerose og ti gange mere almindeligt end seglcelleanæmi . Mænd og kvinder er lige så berørt. Race og oprindelse er også irrelevant. De symptomer er normalt kun observeret i voksenalderen. Arven af ADPKD er autosomal dominant ( monogen ) med komplet gennemtrængning . På grund af den autosomale dominerende arv arver halvdelen af børnene det muterede gen fra deres forældre på et statistisk gennemsnit og udvikler selv ADPKD. Cirka 50% af alle mutationsbærere lider af progressiv nyreinsufficiens. I en gennemsnitlig alder på 58 år er nyreerstatningsbehandling indiceret hos halvdelen af ADPKD-patienter .
Som en systemisk sygdom i ADPKD er andre organer - i de fleste tilfælde leveren - ofte påvirket af cyste dannelse. Afhængigt af forfatteren har op til 75% af dem, der er ramt af ADPKD, levercyster.
genetik
Indtil videre er mutationer i to forskellige gener blevet identificeret som årsagen til sygdommen hos ADPKD-patienter: generne PKD1 og PKD2 . Hos mennesker er PKD1 placeret på kromosom 16 gen locus 16p13.3-p13.12. Det koder for proteinet polycystin-1 . Hos patienter med signifikante mutationer i PKD1 når nyreinsufficiens slutstadiet i en gennemsnitlig alder på 50 år, hvilket betyder, at nyreerstatningsbehandling er indiceret. Patienter med mutationer i PKD2, som er placeret på kromosom 4- gen-locus q21-q23 og koder for polycystin-2, når dette stadium betydeligt senere i en gennemsnitsalder på 70 år ( sen debut ) . Ca. 85% af patienterne med ADPKD bærer en eller flere mutationer i PKD1. De resterende 15% skyldes mutationer i PKD2.
På mobilniveau er ADPKD en recessiv mekanisme. Den første betingelse for sygdommen er en kimlinjemutation i en af PKD1- eller PKD2- allelerne . For det andet skal en somatisk mutation , et såkaldt andet hit, finde sted, så cyste-dannelsen initieres. Dette tab af heterozygositet ( tab af heterocygositet , LOH) fundet i ADPKD tager tydeligvis evigt. Den indledende somatiske mutation kan være på det andet gen. I dette tilfælde kaldet transheterozygositet er kimlinjemutationen PKD1, og den somatiske mutation er PKD2 eller omvendt. I dyremodeller blev det fundet, at kimlinjemutationer, der påvirker begge alleler af et PKD-gen, er perinalt dødelige. Med det andet hit mister den berørte celle sin evne til at hæmme spredning og bliver således udgangspunktet for dannelsen af en ny cyste. En vigtig indikator for rigtigheden af den anden hitteori er eksperimenter med knockout-mus , hvor PKD1 eller PKD2 blev slået fra ( gendeletion ). Kun homozygote dyr bliver syge , mens heterozygote dyr udvikler sig næsten normalt. Den anden hitteori forklarer også, hvorfor kun ca. 1% af alle nefroner i ADPKD danner cyster, selvom alle celler bærer den arvede mutation.
Fra 1995 blev et tredje gen, kaldet PKD3, mistænkt for at være en anden mulig årsag til ADPKD. Mutationer, der ikke var forårsaget af hverken PKD1 eller PKD2, blev senere observeret i fire andre familier med cystiske nyrer fra forskellige lande. Eksistensen af dette gen er nu i tvivl.
| gen | Loci | Eksoner | Mutationstype | Frekvens (%) |
| PKD1 | 16p13.3 | 46 (14,1 kb) | Nonsens | 33 |
| Frameshift | 28 | |||
| In-frame | 6. | |||
| Splejsning | 14. | |||
| Missense | 19. | |||
| PKD2 | 4q21-q23 | 15 (5 kb) | Nonsens | 37 |
| Frameshift | 39 | |||
| Splejsning | 17. | |||
| Missense | 6. | |||
| Sletning | 1 |
Molekylære årsager og dannelse af cyste
Proteinerne kodet af de berørte gener polycystin-1 og polycystin-2 samt fibrocystin kodes af PKHD1 genet er placeret i bunden af den primære cilium af de celler i renale tubulus (nyretubuli-celler) . Det primære cilium er en hårtynd celleforlængelse, hvoraf hver celle kun udvikler en. Ifølge den nuværende viden spiller en funktionsfejl i det primære cilium den afgørende rolle i dannelsen af cyster i alle sygdomme, der fører til cyste nyrer. De primære cilier af de rørformede celler stikker ud i den rørformede lumen og bruges sandsynligvis der til at opfatte væskestrømmen. Derudover er det primære cilium involveret i den rumlige tilpasning af den mitotiske spindel under celledeling . De to polycystines danner en calcium- regulerende ionkanal der er permeabel for calciumioner. Polycystinkomplekset spiller en vigtig rolle i det primære cilium med flere signalveje og mechano-sensoriske funktioner. Den fysiologiske funktion af denne celleorganelle forstås stadig stort set ikke.
Cysternes oprindelse kan have sit udgangspunkt i ethvert afsnit af en nefron - fra glomerulum til opsamlingskanaler (tubulus renalis colligens) . Når cyster når en diameter på mere end 0,2 mm, har de ikke længere nogen forbindelse til nyretubuli (tubuli) .
For at cysterne skal dannes, skal antallet af celler inde i cystevæggen øges. Dette sker gennem overdreven spredning af epitelcellerne i nyrerne. Proteinet mTor ( mammamål for rapamycin) er opreguleret . Væske skal også akkumuleres i cyste-lumen på grund af øget sekretion og / eller nedsat dræning. Denne transepitelvæskeudskillelse er afhængig af den sekundære aktive chlorid-sekretion. Sekretionen af chloridioner reguleres af CFTR (cystisk fibrose transmembran konduktansregulator) eller af en calciumafhængig chloridkanal. Begge er placeret i den apikale cellemembran .
Forløb og prognose
Forløbet af ADPKD er langsomt progressivt (progressivt). Selv før nyreinsufficiens indtræffer, kan der påvises en forstyrrelse i urinkoncentrationen (vandabsorption) hos de berørte patienter. I de tidlige stadier af sygdommen nedsættes nyrefunktionen ikke af dannelsen af cyster. Ydelsen falder kun fra en nyrestørrelse på 1000 cm³. Hvis nyrevolumenet er over 1500 cm³, reduceres den glomerulære filtreringshastighed årligt med ca. 4 til 5 ml · min -1 . I gennemsnit stiger volumenet af nyrerne med mere end 5% om året hos patienter med et nyrevolumen på mere end 750 cm³. De første symptomer på sygdommen bemærkes normalt mellem 30 og 40 år. Generelt er der dog en bred vifte af variationer - ofte inden for en familie.
I næsten alle tilfælde fører sygdommen til terminal nyresvigt (ultimativ nyresvigt). Kvinder når dette stadium i gennemsnit seks år senere end mænd.
Yderligere overlevelse er derefter kun garanteret gennem nyreerstatningsterapi, dvs. dialyse eller nyretransplantation. Det er endnu ikke helt forstået, hvorfor polycystiske nyrer i sidste ende fører til nyresygdom i slutstadiet. Mekanismen kan ikke forklares ved trykatrofi af parenkymet alene. Kirurgiske indgreb som punkteringer forsinker ikke sygdommens forløb. Fra histologiske undersøgelser kan det konkluderes, at hypertension er en vigtig faktor for progression (progression) af nyreinsufficiens.
Ud over genetik har patientens miljø og livsstil også indflydelse på forløbet af ADPKD. For eksempel blev det fundet hos kvinder, at flere leverancer og andre østrogene faktorer forværrede sygdomsforløbet betydeligt. Den accelererede vækst af cyster sammenlignet med kvinder og den tidligere nåede af terminal nyresvigt hos mænd tilskrives også hormonelle påvirkninger. Også tobaksrygning påvirker - især blandt mænd - progressionen af ADPKD negativ. En mulig forklaring er de velkendte negative virkninger af rygning på blodkarrene .
Forventede levealder
I en undersøgelse blev 333 patienter fra 31 familier med PKD1 og 291 patienter med PKD2 fra 31 familier sammenlignet med en 398-personers, geografisk identisk kontrolgruppe. PKD1-patienter nåede en gennemsnitsalder på 53,0 år (± 1,8 år; 95% sandsynlighed). På den anden side nåede PKD2-patienterne i gennemsnit 69,1 år (± 2,2 år; 95%), mens befolkningen fra kontrolgruppen var 78,0 år (± 4,2 år; 95%) (se tilstødende grafik).
Årsager til død
Dødsårsagen hos 129 patienter med ADPKD blev analyseret i en retrospektiv undersøgelse. Derefter døde 36% af hjertesygdomme og 24% af infektioner . I 94% af infektionerne var sepsis (blodforgiftning) til stede. De obduktioner afslørede hjertehypertrofi i 89% af alle patienter og koronararteriesygdom i 81% . En neurologisk hændelse resulterede i død hos 12% af patienterne og et brud på hjerne-aneurisme hos 6%. Cerebral blødning forårsaget af hypertension var dødsårsagen hos 5% og et iskæmisk slagtilfælde hos 1% af patienterne. Ingen patienter døde af nyrekræft .
Autosomal recessiv polycystisk nyresygdom
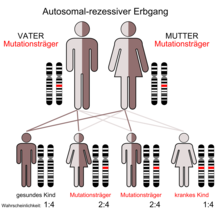
Autosomal recessive polycystisk nyresygdom ( ARPKD ), også kendt som svamp nyre eller Potter I nyre , manifesterer sig i barndommen. Den forekomst af denne sygdom hos nyfødte er i området fra 1: 6.000 til 1: 40.000, med et gennemsnit på 1: 20.000. Sygdommen er derfor relativt sjælden. Den penetrans er færdig. Omkring hver syttende person er bærer af mutationen (se diagram over autosomal recessiv arv). Mutationer i PKHD1 genet - som hos mennesker er placeret på kromosom 6 , gen locus p21.1-p12 - kan føre til dannelse af cystiske nyrer. Proteinet fibrocystin kodet af PKHD1 findes sammen med polycystin-2 i basallegemet af de primære cilier . I apikale domæne af polariserede epitelceller, er det åbenbart involveret i dannelsen af tubuli og / eller opretholdelsen af arkitekturen i lumen på den opsamlingsrøret . Følgelig påvirkes opsamlingskanalerne i det væsentlige af cyste-dannelsen i ARPKD. Autosomal recessiv polycystisk nyresygdom er forbundet med medfødt leverfibrose.
ARPKD manifesterer sig hos patienter i en meget ung alder ( tidlig begyndelse ) . Aldersintervallet er 0 til 20 år. Den gennemsnitlige forventede levetid for de berørte børn er seks år. Der skelnes mellem perinatal (28. uge af graviditeten op til syv dage efter fødslen), neonatal (nyfødt), infantil (barnlig) og ung (ung) form. Jo lavere alder ved starten, jo dårligere er prognosen .
NPH-MCKD-kompleks
Den NPH-MCKD kompleks (nephronophthisis-medullær cystisk nyresygdom) er en gruppe af genetiske sygdomme i nyren, som fører til en cyste nyre. I tilfælde af nefronophthisis er arv autosomal recessiv, mens den er autosomal dominerende i begge former for medullær cystisk nyresygdom. Det almindelige kliniske billede af sygdommene er dannelsen af cystiske nyrer ved den kortikale-medullære grænse (kortikomedullær grænse). Afhængigt af det berørte gen fører alle sygdomme i NPH-MCKD-komplekset til terminal nyresvigt i visse aldersgrupper.
Bardet-Biedl syndrom
Bardet-Biedl syndrom (BBS) er en meget sjælden oligogenetisk arvelig sygdom med en autosomal dominerende arv. Årsagen til sygdommen er mutationer i BBS generne 1 til 12. Foruden dannelsen af polycystiske nyrer, der er degeneration af den nethinden , barndommen fedme , mentalt handicap , misdannelser af den urin og seksuel apparat og polydaktyli (flere fingre) .
Knoldsklerose
Individuelle nyrecyster er almindelige ved autosomal dominant arvelig tuberøs sklerose. Polycystisk nyresygdom er også mindre almindelig. Årsagen til dette er normalt større deletioner, der påvirker både TSC2-genet, som er påvirket af tuberøs sklerose, og PKD1-genet; begge gener er placeret tæt på kromosom 16 .
Oro-facio-digitalt syndrom type 1 (OFD 1)
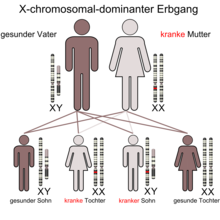
Det oro-facio-digitale syndrom type 1, også kendt som Papillon-Leage-Psaume syndrom, er en meget sjælden X-bundet dominerende arvet sygdom. Udbredelsen hos nyfødte er omkring 1: 250.000. Sygdommen har en række forskellige symptomer, især i ansigt og mund, og en tendens til at have polycystiske nyrer set hos mange patienter. Sidstnævnte diagnosticeres normalt meget sent, når nyresvigt er langt fremme.
Sygdommen er prænatalt dødelig for mænd .
Ved orofazio-digitalt syndrom type 2 , OFD2 eller Mohr syndrom observeres ingen ændringer i nyrerne.
Erhvervede cystiske nyrer
En særlig form for Endstadiumniere, som polycystisk sekundær transformation eller som erhvervet cystisk nyre (engl. Erhvervet cystisk nyresygdom , ACKD ) henvises til 50% af alle patienter, der udvikler 40 ved langvarig dialyse. Hun er en meget alvorlig komplikation i ESRD ( engelsk end-stage renal disease, ESRD ). I tilfælde af transplantationsmodtagere kan både deres egne nyrer og transplantationen blive påvirket. Årsagen til udviklingen af de erhvervede dialyserelaterede cysternyrer er normalt en langvarig dialyse for analgetisk nefropati . Cyster på nyrerne er meget almindelige hos patienter med nyresygdom i slutstadiet. Hyppigheden og størrelsen af cyster øges med dialysens varighed. Begge køn er lige så ramt af sygdommen, uanset patientens alder. Sandsynligheden for, at nyrekræft vil udvikle sig som en yderligere komplikation, øges markant - især hos mandlige patienter.
terapi
Der er i øjeblikket kun ét lægemiddel godkendt til behandling af polycystisk nyresygdom ( tolvaptan , se nedenfor). Cirka 50% af alle ADPKD-patienter - der udgør størstedelen af patienter med polycystisk nyresygdom - har brug for nyreerstatningsterapi i løbet af deres levetid. En kur er kun mulig gennem en nyretransplantation .
Hjælpestoffer
Indstilling af det arterielle blodtryk, sædvanligvis ved hjælp af ACE-hæmmere , er af særlig betydning som et hjælpestof i polycystiske nyrer. Derudover er der en række anbefalinger til patienter med cystiske nyrer, som heller ikke tillader kur, men gør sygdommens progression mere gunstig for patienten.
Da koffein mistænkes for at fremskynde cystevækst, bør patienter undgå drikkevarer, der indeholder koffein, hvis det er muligt. En diæt med lavt saltindhold hjælper med at sænke blodtrykket, hvilket er forbundet med nedsat udskillelse af natriumioner. Ikke-steroide antiinflammatoriske lægemidler , blandede analgetika , visse antibiotika og andre lægemidler, der er giftige for nyrerne, bør så vidt muligt undgås. På den anden side behandles cysteinfektioner så tidligt som muligt med antibiotika, der kan trænge ind i cysten eller galden .
Nyrerstatningsterapi
Kun nyreerstatningsterapi, dvs. dialyse eller nyretransplantation, sikrer patientens overlevelse ved terminal nyresvigt. I de fleste tilfælde udføres dialyse i form af hæmodialyse , da de store nyrer - og ofte leveren - gør bukhulen meget trang, og peritonealdialyse er derfor ikke mulig. Hvis det er muligt, foretrækkes nyretransplantation frem for dialyse. Det muliggør gendannelse af fysisk ydeevne, livskvalitet og patientens sociale integration . Det forbedrer også den forventede levealder markant sammenlignet med dialyse. De lange ventetider for donornyrene er problematiske på grund af det lave antal tilgængelige donornyrer.
Polycystiske nyrer fjernes - i modsætning til tidligere praksis - kun undtagelsestransplantation i undtagelsestilfælde, for eksempel når nyrevolumenet har nået en kritisk størrelse.
Fremtidige terapeutiske tilgange
Behandling af patienter med cystiske nyrer medfører årlige omkostninger på over 1 mia. $ Kun i USA. Denne sum skyldes i det væsentlige omkostningerne til den nyreudskiftningsterapi, der er nødvendig ved terminal nyresvigt.
Multiplikationen og størrelsesforøgelsen af de tyndvæggede, væskefyldte cyster afhænger af to processer: proliferation af celler i cysteepitel og sekretion af væske i cysterne. Begge processer er afhængige af cAMP . cAMP stimulerer Ras / MAP-kinasevejen og fører således til unormal cellevækst. Derudover aktiverer cAMP CFTR - chloridkanalen og fremmer således væskesekretion i cyster. Terapeutiske tilgange, der i øjeblikket testes, adresserer begge cAMP-afhængige processer for at bremse cyste dannelse og vækst.
Der udføres også forskning i den mulige involvering af proteinet C-Met og i forbindelse hermed en terapi med C-Met- hæmmere , som har vist lovende resultater i dyreforsøg med mus .
Billedbehandlingsprocedurer og undersøgelse af nye terapeutiske tilgange
Gennemsnitsalderen ved diagnose af ADPKD er i øjeblikket 27 år. Hvis der opstår nyrefunktion, er der et hurtigt fald i GFR på ~ 5,9 ml / min pr. År. Indtil videre har ingen randomiseret undersøgelse i dette sene stadium af sygdommen været i stand til at demonstrere den gavnlige effekt af en behandling. På grund af den lange presymptomatiske fase og den sene debut af nyreinsufficiens er de primære endepunkter , der normalt undersøges i studier af kronisk nyresygdom, såsom tid til dialysebehandling, fordobling af serumkreatinin eller død, begrænset anvendelse i studier på polycystisk nyre sygdom. Det var af denne grund, at konsortiet til undersøgelser af radiologisk billeddannelse af polycystisk nyresygdom blev oprettet. (CRISP), hvis opgave det er at undersøge billeddannelsesmetoder, der gør det muligt at afgive udsagn om sygdomsforløbet i de tidlige stadier. Et vigtigt resultat af undersøgelserne af CRISP ved anvendelse af magnetisk resonansbilleddannelse er, at cyster hos patienter med ACPKD vokser kontinuerligt og kvantificerbare, og at cystevækst korrelerer med faldet i nyrefunktionen. Det vil sige, at en større stigning i cyste størrelse er forbundet med et hurtigere fald i nyrefunktionen.
HALT-polycystisk nyresygdom (HALT-PKD) er en prospektiv undersøgelse, der i øjeblikket undersøger virkningerne af en blokade af renin-angiotensin-aldosteronsystemet og / eller streng blodtryksregulering i de tidlige stadier af sygdommen på cystevækst eller i senere stadier af sygdommen påvirker serumkreatinindobling, dialyse og død.
Hæmning af celleproliferation
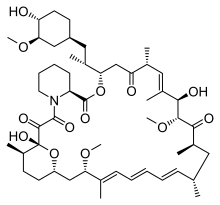
I de senere år er der fundet nye terapeutiske tilgange med stigende molekylærbiologisk viden om årsagerne til PKD. Nogle af disse tilgange er i øjeblikket i klinisk test . Oprindeligt var det dog mere et tilfældigt fund: I en retrospektiv undersøgelse af nogle patienter, der havde modtaget en fremmed nyre, blev det konstateret, at den resterende polycystiske nyre ikke steg i volumen, men at nogle af cysterne trak sig lidt tilbage. Antallet af patienter i den første undersøgelse (n = 4) var ikke statistisk meningsfuld, men effekten kunne påvises statistisk i forskellige dyremodeller . Den åbenlyse årsag til denne forbedring var at tage sirolimus (rapamycin), som blev givet til patienter som et immunsuppressivt lægemiddel. Patienter med en donornyren skal tage immunsuppressiva hele deres liv for at undgå afvisning af det fremmede organ af kroppens eget immunsystem . I humane studier nedsatte behandling med mTOR-hæmmere sirolimus og everolimus stigningen i nyrevolumen, men ikke det progressive fald i nyrefunktionen.
Ud over sirolimus og derivater af denne forbindelse udføres der også forskning på andre potentielle stoffer, hvoraf nogle bruger andre signalveje. Således fx cAMP - antagonister somatostatin og vasopressin potentielt lægemiddel, fordi forhøjede niveauer af cAMP stimulerer spredning og sekretion af cystiske epitelceller.
Triptolid er et lille molekyle isoleret fra et traditionelt kinesisk lægemiddel (Thunder God Vine), der har anti-proliferative og pro- apoptotiske egenskaber. Triptolid fremmer calciumfrigivelse gennem en polycystin-2-afhængig metabolisk vej og hæmmer cyste dannelse og vækst i dyremodeller.
Hæmning af væskesekretion
Antidiuretisk hormon (vasopressin) niveauer øges hos patienter med polycystisk nyresygdom . V2 vasopressin-receptoren i det distale rør og opsamlingskanalen udtrykkes . Dette er de steder på nefronen, hvor cyste dannes. Vasopressin stimulerer dannelsen af cAMP i den distale tubuli via V2-receptoren.
I dyremodellen hæmmer V2-receptorantagonister dannelsen af cAMP, stigningen i nyrernes størrelse og dannelsen af cyster og beskytter nyrefunktionen.
V2-receptorantagonisten tolvaptan viste sig at være sikker og veltolereret hos patienter med ADPKD i fase II / III-studier . En dobbeltblind, placebokontrolleret undersøgelse blev udført hos patienter med ADPKD med normal nyrefunktion og med et nyrevolumen større end 750 ml. Tolvaptan kan bremse sygdommens progression. Tolvaptan er godkendt i Europa til behandling af ADPKD siden maj 2015.
Komplikationer
Typiske komplikationer med cystiske nyrer er forhøjet blodtryk på grund af stimulering af renin-angiotensin-aldosteronsystemet og urinvejsinfektioner .
Urinvejsinfektioner - på grund af de kortere urinveje - påvirker især kvindelige patienter. De fleste tilfælde er infektioner i den urinblæren forårsaget af gram-negative og nosokomielle bakterier. Urinvejsinfektioner behandles symptomatisk, fortrinsvis med lipofile antibiotika . Ekstreme infektioner, såsom pyonephrose (purulent hydronephrosis ), kan føre til fjernelse af den berørte nyre ( nefrektomi ).
Mens forekomsten af nyresten i befolkningen er omkring 5%, påvirker disse aflejringer 10 til 34% af patienterne med polycystiske nyrer. En mulig årsag til den øgede forekomst af nyresten er det lave pH-niveau i urinen hos de berørte.
Afhængig af forfatteren og den gennemførte undersøgelse har 25 til 75% af alle ADPKD-patienter med cystiske nyrer også levercyster . Antallet af levercyster øges med patientens alder. Kvinder har større og højere antal cyster i leveren. På grund af cyster kan leveren forstørres betydeligt og gennemsyres bogstaveligt med cyster. I de fleste tilfælde er parenkymcellernes funktion imidlertid ikke nedsat. For eksempel er leverenzym- og bilirubinniveauer normale. Mere omfattende komplikationer opstår fra pladsbehovet for den undertiden ekstremt forstørrede lever. For eksempel er det muligt, at mellemgulvet er hævet , individuelle sektioner af tarmen indsnævres, hvilket kan gøre det vanskeligt at transportere mad, og større blodkar, såsom den ringere vena cava , kan blokeres .
ARPKD fører til fibrose, skrumpelever og øget tryk i portalvenen ( portalhypertension ) i leveren .
I andre organer som bugspytkirtlen , milten eller æggestokkene er cyster meget mindre almindelige hos patienter med polycystiske nyrer.
En forbindelse mellem polycystiske nyrer og cerebrale aneurismer blev beskrevet allerede i 1904 . Data om prævalensen varierer mellem 4,5 og 22,5%. En mulig tåre (brud) i det berørte blodkar er en af de mest frygtede komplikationer i cystiske nyrer og er dødelig i næsten 50% af tilfældene.
historie
Paris-kirurgen Félix Lejars (1863-1932) brugte først udtrykket polycystiske nyrer i sin afhandling i 1888 . Den canadiske læge William Osler beskrev det i 1915. Indtil midten af det 20. århundrede beskæftigede kun få publikationer dette kliniske billede. I sin afhandling i 1957 var Dalgaard den første til at anerkende den autosomale dominerende arv af ADPKD. I 1985 opdagede Reeders og kolleger PKD1-genlokuset på kromosom 16 hos mennesker.
litteratur
Teknisk artikel
- W. Kühn, G. Walz: Autosomal dominerende polycystisk nyresygdom. I: Dtsch Arztebl. , 104, 2007, s. A3022-A3028.
- I. Ishikawa: Ervervet nyre cystisk sygdom. I: Den cystiske nyre. Kluwer, 1990, ISBN 0-7923-0392-X , s. 351-377.
- JJ Grantham, PA Gabow: Polycystisk nyresygdom. I: Sygdomme i nyrerne. Little Brown, 1988, s. 583-615.
- Joachim Frey : Cystiske nyrer og andre medfødte anomalier. I: Ludwig Heilmeyer (red.): Lærebog i intern medicin. Springer-Verlag, Berlin / Göttingen / Heidelberg 1955; 2. udgave, ibid. 1961, s. 974 f.
Referencebøger
- ML Watson (red.): Polycystisk nyresygdom. Oxford Univ. Presse, 1996, ISBN 0-19-262578-0 .
- HM Sass, P. Schröder (red.): Patientuddannelse i tilfælde af genetisk risiko. LIT Verlag, 2003, ISBN 3-8258-4987-2 , s. 147-198.
Patientoplysninger
- AB Chapman, LM Guay-Woodford: Familien og ADPKD: En guide til børn og forældre. Polycystic Kidney Research Foundation, 1997, ISBN 0-9614567-5-2 .
- Informationsark om cystiske nyrer i et ringbind . PKDeV-patientforening
Populær videnskab
- T. Kotlorz: Nyt håb for nyrepatienter. I: Die Welt , 23. juli 2007
- H. Jänz: Håber på nyren. I: Die Welt , 3. juni 2006
Weblinks
- PKD familiær cystisk nyrer e. V.
- Urologi lærebog: Autosomal dominerende polycystisk nyresygdom (ADPKD)
- zystennieren.de Ruhr University Bochum
- PathoPic - Billeddatabase fra University of Basel: Postmortem angiogram af en cystisk nyre (billede af en prøve)
- PathoPic - Billeddatabase fra University of Basel: ADPKD (Potter Type I) (billede af et eksemplar)
- PathoPic - Billeddatabase fra University of Basel: Polycystisk nyre efter terminal nyresvigt (billede af et præparat)
- PathoPic - Billeddatabase fra University of Basel: ARPKD (Potter Type I) (billede af et eksemplar)
- PathoPic - Billeddatabase fra Universitetet i Basel: To polycystiske nyrer og en transplanteret nyre (billede af en prøve)
Videoer
- Professor Obermüller: Cystiske nyrer forklarede tydeligt - angreb på et højtydende organ på YouTube
- Berørte rapporter på YouTube
Individuelle beviser
- ^ S. Wang et al.: Det autosomale recessive polycystiske nyresygdomsprotein er lokaliseret til primære cilier med koncentration i det basale kropsområde. I: J Am Soc Nephrol . , 15, 2004, s. 592-602. PMID 14978161
- ↑ a b c d e f g h i j k l m n o p q r s t U. Faber: Langvarigt forløb i polycystisk nyredegeneration hos voksne efter nyretransplantation. Dissertation, Heinrich Heine University Düsseldorf, 2000.
- ^ J. Milutinovic et al.: Autosomal dominerende polycystisk nyresygdom: symptomer og kliniske fund. I: QJ Med. , 53, 1984, s. 511-522. PMID 6240069
- ^ LW Elzinga et al.: Kirurgisk behandling af smertefulde polycystiske nyrer. I: Am J Kidney Dis . , 22, 1993, s. 532-527. PMID 8213792
- ↑ LW Elzinga et al.: Kirurgi i styringen af autosomal dominerende polycystisk nyresygdom. I: Am. J. Kidney Dis. , 1992, s. 89-92. PMID 1739090
- ↑ D. Frang et al.: En ny tilgang til behandling af polycystiske nyrer. I: Int. Urol. Nephrol. , 20, 1988, s. 13-21. PMID 3360583
- ↑ LW Elzinga et al.: Cyste-dekompressionskirurgi for autosomal dominerende polycystisk nyresygdom . I: J Am Soc Nephrol. , 2, 1992, s. 1219-1226. PMID 1591362 .
- ↑ BJ Lifson u a.: Rolle og langsigtede resultater af laparoskopisk afortikation ved ensom cystisk og autosomal dominerende polycystisk nyresygdom. I: J Urol . , 159, 1998, s. 702-705. PMID 9474129
- Chap AB Chapman et al.: Overt proteinuri og mikroalbuminuri i autosomal dominerende polycystisk nyresygdom. I: J Am Soc Nephrol. , 5, 1994, s. 1349-1354. PMID 7894001
- ↑ PA Gabow et al:. Renal struktur og hypertension i autosomal dominant polycystisk nyresygdom. I: Kidney International , 38, 1990, s. 1177-1180. PMID 2074659
- ↑ a b P. A. Gabow: Autosomal dominant polycystisk nyresygdom I: NEJM 329, 1993, s. 332-342. PMID 8321262
- ^ AB Chapman, PA Gabow: Hypertension ved autosomal dominerende polycystisk nyresygdom. I: Kidney Int Suppl , 61, 1997, s. 71-73. PMID 9328971
- ^ PA Gabow et al.: Nytte af ultralyd til diagnosticering af autosomal dominerende polycystisk nyresygdom hos børn. I: J Am Soc Nephrol. , 8, 1997, s. 105-110. PMID 9013454
- ^ WC O'Neill et al.: Sonografisk vurdering af sværhedsgraden og progressionen af autosomal dominerende polycystisk nyresygdom: Consortium of Renal Imaging Studies in Polycystic Kidney Disease (CRISP). I: Am J Kidney Dis. , 46, 2005, s. 1058-1064. PMID 16310571
- ↑ KM Koch et al.: Klinisk nefrologi. Urban & Fischer-Verlag, 1999, ISBN 3-437-21730-5 , s. 437-459.
- ↑ V. Osathanondh, EL Potter : patogenesen af polycystiske nyrer. I: Ark. Sti. , 77, 1964, s. 459-465. PMID 14120681
- ↑ B. Hermanns et al:. Patologi og genetik arvelige cystiske nyrer. I: Der Pathologe , 24, 2003, s. 410-420. PMID 14605845
- ↑ ADPKD (autosomal dominerende polycystisk nyresygdom) ( siden er ikke længere tilgængelig , søg i webarkiver ) Universitetshospitalet Aachen; Hentet 30. september 2008.
- ↑ a b c S. Helmig: Befolkningsgenetisk undersøgelse af kattens PKD 1-gen med hensyn til polycystisk syndrom. Afhandling, Justus Liebig University Giessen, 2005.
- ↑ F. Hildebrandt, M. Wolf: Patologi og genetik arvelige cystiske nyrer. I: Medicinsk terapi. Springer, 2005, ISBN 3-540-21226-4 , s. 927-939.
- ↑ a b c d e f g W. Kühn, G. Walz: Autosomal dominerende polycystisk nyresygdom. I: Ärzteblatt , 104/2007, s. A3022 - A3028.
- ^ RG Elles et al.: Diagnose af voksen polycystisk nyresygdom ved genetiske markører og ultralydsbilleddannelse i et frivilligt familieregister. I: J Med Genet , 31, 1994, s. 115-120. PMID 8182715 .
- ↑ LF Fried et al.: Duodenal obstruktion i polycystisk nyresygdom. Sagsrapport og gennemgang af litteraturen. I: Am. J. Nephrol. , 18, 1998, s. 318-320. PMID 9653836
- ↑ a b P.D. Wilson: Polycystisk nyresygdom. I: N Engl J Med. , 350, 2004, s. 151-164. PMID 14711914 .
- ↑ U. Frei, HJ Schober-Halstenberg: Nyrerstatningsterapi i Tyskland. (PDF; 1,4 MB) I: QuaSi-Niere årsrapport 2005/2006. Berlin
- ↑ GM Fick, PA Gabow: arvelig og erhvervet cystisk sygdom i nyrerne. I: Kidney Int. , 46, 1994, s. 951-964. PMID 7861721 .
- ^ R. Rohatgi: Kliniske manifestationer af arvelig cystisk nyresygdom. I: Front Biosci. , 13, 2008, s. 4175-4197. PMID 18508505
- ↑ nyresygdom, medullær cystisk, autosomal dominant, med eller uden hyperurikæmi orpha.net; Hentet 4. oktober 2008.
- Att M. Attanasio et al.: Tab af GLIS2 forårsager nefronophthisis hos mennesker og mus ved øget apoptose og fibrose. I: Nature Genet . , 39, 2007, s. 1018-1024. PMID 17618285
- ↑ a b B. Buchholz: Funktionel interaktion mellem polycystin 2 og TRPV4. Dissertation, Albert Ludwig University of Freiburg, 2004.
- ^ AR Gallagher et al.: Molekylær basis for autosomal dominerende polycystisk nyresygdom. I: Cellular and Molecular Life Sciences , 59, 2002, s. 682-693. PMID 12022474 .
- ↑ ADPKD (autosomal dominerende polycystisk nyresygdom) . ( Side ikke længere tilgængelig , søg i webarkiver ) Universitetshospital Aachen; Hentet 11. november 2008.
- ^ DW Bianchi et al.: Fetologi. McGraw-Hill Professional, 2000, ISBN 0-8385-2570-9 , s.632 .
- ↑ PA Gabow et al.: Faktorer, der påvirker progressionen af nyresygdom i autosomal dominerende polycystisk nyresygdom. I: Kidney Int. , 41, 1992, s. 1311-1319. PMID 1614046
- ^ AC Ong, PC Harris: Molekylær patogenese af ADPKD: polycystinkomplekset bliver komplekst. I: Kidney Int. , 67, 2005, s. 1234-1247. PMID 15780076
- ^ S. Rossetti et al.: Mutationsanalyse af hele PKD1-genet: genetiske og diagnostiske implikationer. I: Am. J. Hum. Genet. , 68, 2001, s. 46-63. PMID 11115377
- ^ GG Germino: Autosomal dominerende polycystisk nyresygdom: en to-hit-model. I: Hosp Pract. , 32, 1997, s. 81-82, 85-88, 91-92. PMID 9078975
- ↑ Y. Pei et al.: Somatiske PKD2-mutationer i individuelle nyre- og levercyster understøtter en "to-hit" -model af cystogenese i type 2 autosomal dominerende polycystisk nyresygdom. I: J Am Soc Nephrol. , 10, 1999, s. 1524-1529. PMID 10405208
- ↑ F. Qian et al:. Den molekylære basis for fokal cystedannelse i human autosomal dominant polycystisk nyresygdom type I. I: Cell , 87, 1996, pp 979-987.. PMID 8978603
- ↑ T. Watnick et al.: Mutationer af PKD1 i ADPKD2-cyster antyder en patogen effekt af trans-heterozygote mutationer. I: Nature Genetics , 25, 2000, s. 143-144. PMID 10835625
- ↑ K. Hackmann: Undersøgelser af ekspressionen af de murine gener Pkd1 og Pkd2, de ortologe gener af den autosomale dominerende polycystiske nyresygdom (ADPKD). (PDF) Afhandling, Bielefeld University, 2005.
- ↑ W. Lu et al.: Sen begyndelse af nyre- og levercyster i Pkd1-målrettede heterozygoter. I: Nature Genetics , 21, 1999, s. 160-161. PMID 9988265
- ↑ G. Wu et al:. Somatisk inaktivering af Pkd2 resulterer i polycystisk nyresygdom. I: Cell , 93, 1998, s. 177-188. PMID 9568711
- ↑ N. Bogdanova et al.: Genetisk heterogenitet af polycystisk nyresygdom i Bulgarien. I: Hum Genet. , 95, 1995, s. 645-650. PMID 7789949
- Da MC Daoust et al.: Bevis for et tredje genetisk sted for autosomal dominerende polycystisk nyresygdom. I: Genomics , 25, 1995, s. 733-736. PMID 7759112
- ^ AD Paterson, Y. Pei: Er der et tredje gen for autosomal dominerende polycystisk nyresygdom? I: Kidney International , 54, 1998, s. 1759-1761. PMID 9844156
- ↑ M. Koptides, CC Deltas: Autosomal dominerende polycystisk nyresygdom: molekylær genetik og molekylær patogenese. I: Hum Genet. , 107, 2000, s. 115-126. PMID 11030408
- ↑ M. Consugar et al.: PKD3 revideret med forbedret PKD1 og PKD2 haplotyping og mutationsscreening. I: J Am Soc Nephrol. , 16, 2005, s. 358A.
- ^ AD Paterson, Y. Pei: PKD3-at være eller ikke være? I: Nephrol Dial Transplant , 14, 1999, s. 631-614. PMID 10570111
- ↑ Y. Pei et al.: Bilineal sygdom og trans-heterozygoter i autosomal dominerende polycystisk nyresygdom. I: Am J Hum Genet. , 68, 2001, s. 355-363. PMID 11156533
- ^ A b S. Rosetti, PC Harris: Genotype-fenotype korrelationer i autosomal dominerende og autosomal recessiv polycystisk nyresygdom. I: J Am Soc Nephrol. , 18, 2007, s. 1374-1380. PMID 17429049
- ↑ a b C. Boucher, R. Sandford: Autosomal dominerende polycystisk nyresygdom (ADPKD, MIM 173900, PKD1 og PKD2 gener, proteinprodukter kendt som polycystin-1 og polycystin-2). I: Eur J Hum Genet. , 12, 2004, s. 347-354. PMID 14872199 .
- Stay C. Stayner, J. Zhou: Polycystinkanaler og nyresygdom. I: Trends in Pharmacological Sciences , 22, 2001, s. 543-546. PMID 11698076
- ^ T. Watnick, G. Germino: Fra cilia til cyste. I: Nature Genetics , 34, 2003, s. 355-356. PMID 12923538
- ^ BK Yoder: Primær cilias rolle i patogenesen af polycystisk nyresygdom. I: J Am Soc Nephrol. , 18, 2007, s. 1381-1388. PMID 17429051
- ↑ BK Yoder et al:. Molecular patogenese autosomal dominant polycystisk nyresygdom. I: Expert Rev Mol Med. , 17, 2006, s. 1-22. PMID 16515728
- ↑ KD Gardner et al.: Hvorfor nyrecyster vokser. I: Am J Physiol. , 266, 1994, F353-359. PMID 8160782
- ↑ D. Rizk, AB Chapman: Cystisk og arvelig nyresygdom. I: Am J Kidney Dis. , 42, 2003, s. 1305-1317. PMID 14655206
- ↑ MHK Shokeir: Ekspression af polycystisk nyresygdom hos voksne i barndommen: en longitudinel undersøgelse. I: Clin. Genet. , 14, 1978, s. 61-72. PMID 688689
- ↑ N. Gretz et al.: Er køn en afgørende faktor for udviklingen af nyresvigt? En undersøgelse af autosomal dominerende polycystisk nyresygdom. I: Am J Kidney Dis. , 14, 1989, s. 178-183. PMID 2672797 .
- ↑ R. Sherstha et al:. Postmenopausal estrogenterapi selektivt stimulerer hepatisk udvidelse i kvinder med autosomal dominant polycystisk nyresygdom. I: Hepatology , 26, 1997, s. 1282-1286. PMID 9362373 .
- ↑ PC Harris et al.: Cystetal, men ikke hastigheden af cystisk vækst er forbundet med det muterede gen i ADPKD. I: J Am Soc Nephrol. , 17, 2006, s. 3013-3019. PMID 17035604
- ^ R. Magistroni et al.: Genotypisk funktionskorrelation i type 2 autosomal dominerende polycystisk nyresygdom. I: J Am Soc Nephrol. , 14, 2003, s. 1164-1174. PMID
- ^ SR Orth et al.: Rygning som en risikofaktor for nyresvigt i slutstadiet hos mænd med primær nyresygdom. I: Kidney Int. , 54, 1998, s. 926-931. PMID 9734618
- ↑ SR Orth et al.: Rygning som en risikofaktor for nyresvigt i slutstadiet hos patienter med primær nyresygdom. I: Bidrag Nephrol. , 130, 2000, s. 109-123. PMID 10892557 .
- ↑ a b N. Hateboer: Sammenligning af fænotyper af polycystisk nyresygdom type 1 og 2. I: The Lancet , 353, 1999, s. 103-107. PMID 10023895
- ↑ GM Fick et al.: Dødsårsager ved autosomal dominerende polycystisk nyresygdom. I: J Am Soc Nephrol. , 5, 1995, s. 2048-2456. PMID 7579053
- ^ Autosomal recessiv polycystisk nyresygdom (ARPKD), fuld genanalyse. Mayo Medical Clinic; adgang den 16. januar 2018.
- ^ R. Witzgall: Ny udvikling inden for cystiske nyresygdomme. (PDF; 250 kB) I: Current Molecular Medicine , 5, 2005, s. 455-465. PMID 16101475 .
- ↑ K. Zerres et al.: Autosomal recessiv polycystisk nyresygdom. I: J Mol Med. , 76, 1998, s. 303-309. PMID 9587064
- ↑ ST Shaikewitz et al:.. Autosomal recessiv polycystisk nyresygdom: Problemer Vedrørende variabilitet kliniske præsentation. I: J Am Soc Nephrol. , 3, 1993, s. 1858-1862. PMID 8338916
- ↑ EF-hætte: Molekylære biologiske undersøgelser af PKD1-genet hos katte. Afhandling, Justus Liebig University Giessen, 2008.
- ↑ MZ Zhang et al.: PKHD1-protein kodet af genet for autosomal recessiv polycystisk nyresygdom associeret med basale kroppe og primære cilier i nyreepitelceller. I: Proc Natl Acad Sci USA , 101, 2004, s. 2311-2316. PMID 14983006
- ↑ LM Guay-Woodford: Nyre cystiske sygdomme: forskellige fænotyper konvergerer på cilium / centrosom-komplekset. I: Pædiatrisk nefrologi , 21, 2006, s. 1369-1376. PMID 16823577
- ↑ T. Benzing et al:. Wnt-signalering i polycystisk nyresygdom . I: J Am Soc Nephrol. , 18, 2007, s. 1389-1398. PMID 17429050
- ↑ SJ Ansley et al.: Basal kropsdysfunktion er en sandsynlig årsag til pleiotropisk Bardet - Biedl syndrom. I: Nature , 425, 2003, s. 628-633. PMID 14520415
- Amp Sampson et al.: Nyre-cystisk sygdom i tuberøs sklerose: rolle polycystisk nyresygdom 1-gen. I: Am J Hum Genet. 1997 okt; 61 (4), s. 843-851. PMID 9382094 .
- ↑ AA Connacher et al.: Orofaciodigital syndrom type I forbundet med polycystiske nyrer og agenese af corpus callosum. I: J. Med. Genet. , 24, 1987, s. 116-122. PMID 3560170
- ↑ SA Fjer et al:. Oral-facial-digital syndrom type 1 er en anden dominant polycystisk nyresygdom: kliniske, radiologiske og histopatologiske træk af en ny slægt. I: Nephrol Dial Transplant . , 12, 1997, s. 1354-1361. PMID 9249769
- ^ E. Prati: Oro-facio-digitalt syndrom type 1. (PDF) I: Orphanet Encyclopedia. Oktober 2004.
- ↑ K. Zerres, S. Rudnik-Schöneborn: Polycystisk nyresygdomme. I: Handbook of Molecular Medicine. Springer-Verlag, bind 7 (del 2), 2000, s. 281-295.
- ↑ a b M. A. Matson, EP Cohen: Erhvervet cystisk nyresygdom: forekomst, prævalens og nyrekræft. I: Medicin (Baltimore) , 69, 1990, s. 217-226. PMID 2374506
- ^ W. Remmele: Pathologie 5. Springer, 1997, ISBN 3-540-61098-7 , s. 172.
- ^ University of Basel: Sekundær cyste nyre efter dialyse på grund af analgetisk nefropati. Billede af en histologisk prøve; Hentet 8. september 2008.
- ↑ FA Belibi et al:. Virkningen af koffein på renale epitelceller fra patienter med autosomal dominant polycystisk nyresygdom. I: J Am Soc Nephrol. , 13, 2002, s. 2723-2729. PMID 12397042
- ↑ M. Schmid et al.: Natriuresis-trykforhold i polycystisk nyresygdom. I: J. Hypertens. , 8, 1990, s. 277-283. PMID 2159509
- ^ BZ Colleen: Polycystisk nyresygdom: En oversigt og kommentar. I: Dialyse og transplantation , 28, 1999, s. 468-474.
- ↑ HH Knispel et al.: Transplantation i autosomal dominerende polycystisk nyresygdom uden nefrektomi. I: Urol. Int. , 56, 1996, s. 75-78. PMID 8659014
- ↑ Y. Pirson et al.: Resultat af nyreerstatningsterapi ved autosomal dominerende polycystisk nyresygdom. I: Nephrol Dial Transplant. , 11, 1996, s. 24-28. PMID 9044324
- ↑ JJ Grantham: Polycystisk nyresygdom: gammel sygdom i en ny sammenhæng. I: Trans Am Clin Climatol Assoc. , 113, 2002, s. 211-224. PMID 12053711
- ↑ JP Calvet: Strategier til at hæmme cyste dannelse i ADPKD. In.: Clin J Am Soc Nephrol . , 2008; 3 (4), s. 1205-1211. PMID 18434615
- ↑ S. Qin, M. Taglienti et al:. Manglende ubiquitinere c-Met fører til hyperaktivering af mTOR signalering i en musemodel for autosomal dominant polycystisk nyresygdom. I: The Journal of clinical investigation , bind 120, nummer 10, oktober 2010, s. 3617-3628, doi: 10.1172 / JCI41531 , PMID 20852388 , PMC 2947217 (fri fuldtekst).
- ↑ AB Chapman: Tilgange til afprøvning af nye behandlinger i autosomal dominant polycystisk nyresygdom: indsigter fra den sprøde og HALT-PKD undersøgelser. I: Clin J Am Soc Nephrol. , 3, 2008, s. 1197-1204. PMID 18579674
- ↑ JJ Grantham et al.: Volumenprogression i polycystisk nyresygdom. I: NEJM , 354, 2006, s. 2122-2230. PMID 16707749
- ↑ JM Shillingford et al.: MTOR-vejen reguleres af polycystin-1, og dens inhibering vender renal cystogenese ved polycystisk nyresygdom. I: Proc Natl Acad Sci. , 103, 2006, s. 5466-5471. PMID 16567633
- ↑ Y. Tao et al.: Rapamycin nedsætter markant sygdomsprogression i en rotte-model af polycystisk nyresygdom. I: J Am Soc Nephrol. , 16, 2005, s. 46-51. PMID 15563559
- ↑ PR Wahl i.a .: Inhibering af mTOR med sirolimus forsinker sygdomsprogression i Han: SPRD-rotter med autosomal dominerende polycystisk nyresygdom (ADPKD). I: Nephrol Dial Transplant. , 21, 2006, s. 598-604. PMID 16221708 .
- ↑ SM Flechner et al:. Transplantation , 74, 2002, pp 1070-1076.. PMID 12438948
- ↑ AL Serra, D. plakat, AD Kistler, F. Krauer, S. Raina, J. Young, KM Rentsch, KS Spanaus, O. Senn, P. Kristanto, H. Scheffel, D. Weishaupt, RP Wüthrich: Sirolimus og nyrevækst i autosomal dominerende polycystisk nyresygdom. I: The New England Journal of Medicine , bind 363, nummer 9, aug. 2010, s. 820-829, ISSN 1533-4406 . doi: 10.1056 / NEJMoa0907419 . PMID 20581391 .
- ↑ G. Walz, K. Budde, M. Mannaa, J. Nürnberger, C. Wanner, C. Sommerer, U. Kunzendorf, B. Banas, WH Hörl, N. Obermüller, W. Arns, H. Pavenstädt, J. Gaedeke, M. Büchert, C. May, H. Gschaidmeier, S. Kramer, KU Eckardt: Everolimus hos patienter med autosomal dominerende polycystisk nyresygdom. I: The New England Journal of Medicine , bind 363, nummer 9, aug. 2010, s. 830-840, ISSN 1533-4406 . doi: 10.1056 / NEJMoa1003491 . PMID 20581392 .
- ↑ a b A. Masoumi et al.: Potentielle farmakologiske indgreb i polycystisk nyresygdom. I: Drugs , 67, 2007, s. 2495-2510. PMID 18034588
- ↑ FA Belibi et al.: Cyklisk AMP fremmer vækst og sekretion i humane polycystiske nyreepitelceller. I: Kidney Int. , 66, 2004, s. 964-973. PMID 15327388
- ↑ T. Yamaguchi et al.: CAMP stimulerer in vitro-spredning af renale cysteepitelceller ved at aktivere den ekstracellulære signalregulerede kinase-vej. I: Kidney Int. , 57, 2000, s. 1460-1471. PMID 10760082
- ^ SJ Leuenroth et al.: Triptolid reducerer cystogenese i en model af ADPKD. I: J Am Soc Nephrol. , 19, 2008, s. 1659-1662. PMID 18650476
- ↑ SJ Leuenroth et al:. Triptolid er en traditionel kinesisk medicin-afledte inhibitor af polycystisk nyresygdom. I: Proc Natl Acad Sci. , 104, 2007, s. 4389-4394. PMID 17360534
- ↑ a b V. E. Torres: Vasopressin-antagonisters rolle. I: Clinical Journal of the American Society of Nephrology , bind 3, nummer 4, juli 2008, s. 1212-1218. doi: 10.2215 / CJN.05281107 . PMID 18434616 . (Anmeldelse).
- ^ VE Torres et al.: Effektiv behandling af en ortolog model af autosomal dominerende polycystisk nyresygdom. I: Nat Med , 10, 2004, s. 363-364. PMID 14991049 .
- ↑ Klinisk undersøgelse (fase III): "TEMPO 3/4 forsøg" Tolvaptan-effektivitet og sikkerhed til styring af polycystisk nyresygdom og dens resultater (TEMPO3 / 4) ved Clinicaltrials.gov fra NIH
- ↑ V. Patel, R. Chowdhury, P. Igarashi: Advances in patogenesen og behandlingen af polycystisk nyresygdom. I: Current Opinion in Nephrology and Hypertension Volume 18, Number 2, March 2009, s. 99-106, ISSN 1535-3842 . doi: 10.1097 / MNH.0b013e3283262ab0 . PMID 19430332 . PMC 282027 (fri fuldtekst). (Anmeldelse).
- ^ VE Torres: Vasopressin-antagonister i polycystisk nyresygdom. I: Seminarer i nefrologi , 2008, 28, s. 306-317. doi: 10.1016 / j.semnephrol.2008.03.003 . PMID 18519091 . (Anmeldelse).
- ↑ VE Torres et al.: Nyresten sygdom i autosomal dominerende polycystisk nyresygdom. I: Am. J. Kidney Dis. , 22, 1993, s. 513-519. PMID 8213789
- ↑ J. Milutinovic et al.: Levercyster hos patienter med autosomal dominerende polycystisk nyresygdom. I: Am. J. Med. , 68, 1980, s. 741-744. PMID 7377224
- ↑ a b E. Higashihara et al.: Kliniske aspekter af polycystisk nyresygdom. I: J. Urol. , 147, 1992, s. 329-332. PMID 1732586 .
- ^ Y. Itai et al.: Hepatobiliære cyster hos patienter med autosomal dominerende polycystisk nyresygdom: prævalens og CT-fund. I: Am. J. Roentgenol. , 164, 1995, s. 339-342. PMID 7839965
- ↑ PA Gabow et al:. Risikofaktorer for udvikling af hepatiske cyster i autosomal dominant polycystisk nyresygdom. I: Hepatology , 11, 1990, s. 1033-1037. PMID 2365280
- ^ E. Levine et al.: Levercyster i autosomal dominerende polycystisk nyresygdom: klinisk og computertomografisk undersøgelse. (PDF) I: Am. J. Roentgenol. , 145, 1985, s. 229-233. PMID 3875218
- ↑ A. Telenti et al:. Hepatisk cyste infektion i autosomal dominant polycystisk nyresygdom. I: Mayo Clin. Proc. , 65, 1990, s. 933-942. PMID 2198396
- ↑ WI Schievink et al.: Sakkulære intrakranielle aneurismer i autosomal dominerende polycystisk nyresygdom. I: J. Am. Soc. Nephrol. 3, 1992, s. 88-95. PMID 1391712 .
- ↑ AB Chapman et al:. Intrakranielle aneurismer i autosomal dominant polycystisk nyresygdom. I: NEJM , 327, 1992, s. 916-920. PMID 1513348
- ↑ F. Lejars: Du gros reins polykystique de l'adult. Afhandling, 1888, Paris
- ↑ B. Schulze: Cystisk nyrer: På vej til en behandlelige sygdom. (PDF) I: MedReport , 44, 2006, s. 5.
- ^ W. Osler: Diagnosen polycystisk nyre. I: Internat Clin. , Philadelphia, 2, 1915, s. 1-5.
- ^ LP Brendan et al.: Udførte Sir William Osler en obduktion på Johns Hopkins Hospital? I: Archives of Pathology & Laboratory Medicine , 2, 132, 2007, s. 261-264.
- ^ OZ Dalgaard: Bilateral polycystisk sygdom i nyrerne. I: Acta Med Scand. , 328, 1957, s. 1-255. PMID 13469269
- ^ ST Reeders et al.: En stærkt polymorf DNA-markør forbundet med voksen polycystisk nyresygdom på kromosom 16. I: Nature , 317, 1985, s. 542-544. PMID 2995836