Kaliumcarbonat
| Strukturel formel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
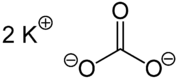
| ||||||||||||||||||||||
| Generel | ||||||||||||||||||||||
| Efternavn | Kaliumcarbonat | |||||||||||||||||||||
| andre navne | ||||||||||||||||||||||
| Molekylær formel | K 2 CO 3 | |||||||||||||||||||||
| Kort beskrivelse |
hvidt fast stof |
|||||||||||||||||||||
| Eksterne identifikatorer / databaser | ||||||||||||||||||||||
| ||||||||||||||||||||||
| ejendomme | ||||||||||||||||||||||
| Molar masse | 138,20 g mol −1 | |||||||||||||||||||||
| Fysisk tilstand |
fast |
|||||||||||||||||||||
| massefylde |
2,428 g cm −3 |
|||||||||||||||||||||
| Smeltepunkt |
891 ° C |
|||||||||||||||||||||
| kogepunkt |
nedbrydning |
|||||||||||||||||||||
| opløselighed |
meget let i vand (1120 g l −1 ved 20 ° C) |
|||||||||||||||||||||
| Sikkerhedsinstruktioner | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toksikologiske data | ||||||||||||||||||||||
| Termodynamiske egenskaber | ||||||||||||||||||||||
| ΔH f 0 |
−1151,0 kJ / mol |
|||||||||||||||||||||
| Så vidt muligt og sædvanligt anvendes SI-enheder . Medmindre andet er angivet, gælder de givne data for standardbetingelser . | ||||||||||||||||||||||
Kaliumcarbonat (teknisk sprog) eller kaliumcarbonat (almindeligt navn : potaske ), K 2 CO 3 , er et alkali og kalium salt af kulsyre . Det danner et hvidt, hygroskopisk pulver med en smeltetemperatur på 891 ° C og en tæthed på 2,428 g · cm −3 . Navnet potash kommer fra den gamle metode til berigelse af kaliumcarbonat fra planteaske (især træaske , men også tangaske ) ved at vaske det ud med vand (deraf navnet "lutesalt") og derefter fordampe det i potter. Det traditionelle navn var også inspiration til de engelske navne kaliumchlorid og kalium , hvorved kaliumchlorid omfatter mange mineral kaliumsalte (fx kaliumchlorid ) og bør snarere oversættes som kalium salt .
Hændelse
Verdens største kaliumsaltaflejringer er i Canada , Rusland , Eritrea , Hviderusland og Tyskland ; Kaliumcarbonat findes også i nogle indre farvande som Det Døde Hav eller Lop Nor-ørkenen . Tidligere blev kaliumchlorid hovedsageligt opnået fra træaske ved udvaskning . Træaskeindholdet i mineralkomponenter er omkring 85%; ca. 14-19% heraf er kaliumcarbonat og natriumcarbonat.
Ekstraktion og præsentation
- Forkolning af kaliumhydroxid :
- Den vigtigste anvendte kilde til CO 2 er forbrændingsgasser.
- Omsætning af kalkmælk ( calciumhydroxidopløsning ) med kaliumsulfat og kulilte ved 30 bar (formiatproces). Det separerede kaliumformiat kalcineres derefter oxidativt:
- Udvaskning af planteaske og efterfølgende fordampning i askehuse (ikke længere historisk eller teknisk vigtig)
- historisk: afbrænding af tandsten ( Tartarus calcinatus er afbrændt tandsten), for eksempel i Paracelsus
Ligesom natriumcarbonat kan kaliumcarbonat ikke opnås ved hjælp af ammoniak-soda-processen, fordi mellemproduktet kaliumhydrogencarbonat (KHCO 3 ) er for opløseligt.
ejendomme
I vand er det meget let og let opløseligt (1120 g / l), hvorved varme frigives. Opløsningen reagerer alkalisk ved dannelsen af hydroxidioner :
- En carbonation reagerer med vand til dannelse af en hydrogencarbonation og en hydroxidion.
Med syrer dannes de tilsvarende kaliumsalte med udviklingen af kuldioxid . Ved stuetemperatur krystalliserer det som et dihydrat fra den vandige opløsning.
Vandfrit kaliumcarbonat krystalliserer monoklinisk , rumgruppe P 2 1 / c (rumgruppe nr. 14) med gitterparametrene a = 5,640 Å , b = 9,839 Å, c = 6,874 Å og β = 98,70 °. Ved 250 ° C skifter dette til den monokliniske β-form (rumgruppe C2 / c (nr. 15) , a = 5,675 Å, b = 9,920 Å, c = 7,018 Å og β = 96,8 °). Ved 450 ° C skifter dette til en sekskantet form.
brug
- Additiv til fremstilling af glas
- Fremstilling af bløde sæber
- Fremstilling af kaliumglas
- Fremstilling af maling
- Fremstilling af fotografiske udviklere
- Fremstilling af gødning (kaliumforsyningskomponent)
- Vandfrit kaliumcarbonat anvendes lejlighedsvis som tørringsmiddel i laboratoriet .
- Hævemiddel til flade bagværk ( kager og honningkager , især julebageri ) og dej med et højt sukkerindhold.
- Tilsætningsstof til kakao som surhedsregulator
- Neutraliseringsmiddel ved anvendelse af saltsyre (E 507) som aromaforstærker .
- Hurtig tørring af rosiner: Ved at fjerne det naturlige vokslag af druerne fordamper fugt lettere.
- Baseprodukt til andre kaliumforbindelser.
- For at fjerne skorpe fra gryderne: læg 1 spsk på skorpen i gryden, lad den stå natten over og kog den næste dag med en kop vand; resterne løsnes fra bunden af gryden på en skællende måde.
- Slipmiddel til gipsstøbning ( skulptur )
- Elektrolytkomponent i smeltede carbonatbrændselsceller
- Tobaksadditiv til snus (i Tyskland i henhold til tobaksforordningen )
- Additiv til indtagelse af visse vanedannende stoffer
- Tilsætningsstof i nogle håndvask flydende sæber
- Miljøvenligt afisningsmiddel (i stedet for afisningssalt ) til sort is på gader og fortove
- Fordi det altid indeholder radioaktivt kalium-40, kan kaliumchlorid bruges til studentereksperimenter om radioaktivitet
- I mange århundreder i Europa blev kaliumcarbonat i form af bøgaske brugt til mavebeklædning og andre tekstiler lavet af linned og senere også af bomuld . Asken lægges i sække og føjes til en trætønde fyldt med lag vasketøj. Ved at hælde varmt vand over posen blev der frigivet et lud, der havde en rensende og let blegende virkning. Lugen blev derefter vasket ud med vand ved vaskefontænet eller floden. Fremkomsten af ostemasse og senere kunstige rengøringsmidler i begyndelsen af det 20. århundrede gjorde denne metode forældet.
- En del af brandslukningsmidler
Sodapotash fordøjelse
Den soda- kaliumchlorid fordøjelse anvendes til tungtopløselige (jordalkali) sulfater, stærkt anneales (sure eller amfotere) oxider, silicater og sølvhalogenider; fordøjelsen finder sted i en Na 2 CO 3 / K 2 CO 3 smelte. ZrO 2 , Zr 3 (PO 4 ) 4 , Al 2 O 3 , Cr 2 O 3 og Fe 2 O 3 kun delvist opløst. En blanding af sodavand og kaliumchlorid anvendes til denne smeltefordøjelse, fordi det sænker smeltepunktet sammenlignet med rene salte ( eutektisk blanding ). Derudover skubber det enorme overskud af carbonat reaktionsligevægten på produktsiden.
Et eksempel på sulfater:
Individuelle beviser
- ↑ Indtastning af E 501: Kaliumcarbonat i den europæiske database om tilsætningsstoffer til fødevarer, adgang til den 1. juli 2020.
- ↑ Indtastning af POTASSIUM CARBONATE i EU-Kommissionens CosIng-database , der blev åbnet den 11. august 2020.
- ↑ en b c d e f g indtastning på kaliumcarbonat i GESTIS stof database af den IFA , adgang den 22. februar 2017. (JavaScript krævet)
- ↑ Indtastning af kaliumcarbonat i ChemIDplus- databasen fra United States National Library of Medicine (NLM)
- ↑ David R. Lide (red.): CRC Handbook of Chemistry and Physics . 90. udgave. (Internetversion: 2010), CRC Press / Taylor og Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, s. 5-20.
- ^ USGS (US Mineral Resources Program): Potash. (PDF; 88 kB) Fra januar 2010.
- ↑ Indtastning på træaske. I: Leksikon for kemi. Spektrum der Wissenschaft Verlagsgesellschaft, adgang til den 3. september 2018 .
- Try Indtastning af kaliumcarbonat. I: Römpp Online . Georg Thieme Verlag, adgang den 12. november 2014.
- ↑ Friedrich Dobler: Theophrastus Paracelsus 'kemiske fundament for medicin: Eksperimentel gennemgang af hans antimonpræparater. I: Publications of the International Society for the History of Pharmacy , New Series, 10, 1957, s. 76–86, her: s. 80.
- ^ Friedrich Dobler: Conrad Gessner som farmaceut. Von Ostheim AG, Zürich 195, s. 104.
- ↑ Y. Idemoto, JW Richardson, N. Koura, S. Kohara, CK Loong: Crystal struktur (Li x K 1-x ) 2 CO 3 (x = 0,0.43,0.5,0.62,1) ved neutron pulverdiffraktionsmønster analyse. I: Journal of Physics and Chemistry of Solids , 59, 1998, s. 363-376, doi: 10.1016 / S0022-3697 (97) 00209-6 .
- B HY Becht, B. Struikmans: En monoklinisk højtemperaturmodifikation af kaliumcarbonat . I: Acta Crystallographica , B32, 1976, s. 3344-3346, doi: 10.1107 / S0567740876010303 .
- ^ SJ Schneider, EM Levin: Polymorfi af K 2 CO 3 . I: Journal of the American Ceramic Society , 56 (4), 1973, s. 218-219, doi: 10.1111 / j.1151-2916.1973.tb12461.x .
- ↑ Undersøgelse foretaget af University of Natural Resources and Life Sciences, Wien om virkningen af kvælstofholdige optøningsmidler Optøningsmiddelundersøgelse 2000 (PDF; 1,6 MB)
- ↑ LVR Institute for Regional Studies and Regional History: Bagning af vasketøj med bøgaske
- ↑ Georg Pless: Erstatning af visse miljøskadelige brandslukningsmidler i udvalgte anvendelsesområder . Red.: Institut for Brandvæsen Sachsen-Anhalt. Heyrothsberge 2003 ( Umweltbundesamt.de [PDF]).
Weblinks
- Stephanie Summermatter: Potash. I: Schweiziske historiske leksikon .







