Glat muskulatur
Glat muskulatur er en af tre typer muskler, der findes hos mennesker og dyr. Det forekommer i væggene i alle hule organer undtagen hjertet, som kan "trække sig sammen", hvilket betyder at de kan reducere deres klare bredde ( lumen ). Disse er for eksempel blodkarrene, organerne i fordøjelseskanalen og luftvejene. Derudover forekommer glat muskulatur forskellige andre steder såsom huden.
Navnet på de glatte muskler refererer til deres mikroskopiske struktur: mens skeletmusklerne og hjertemusklerne viser synlige tværgående striber under mikroskopet , gør de glatte muskler ikke det. I modsætning til skeletmuskulaturen kan den ikke kontraheres vilkårligt, men har andre kontrolmekanismer, der spænder fra muskulære ( myogene ) mekanismer til kontrol af det vegetative nervesystem eller enteriske nervesystem ( neurogen kontrol ) og til kontrol med hormoner , neurotransmittereog andre messenger-stoffer er tilstrækkelige. Bortset fra disse ligheder danner de glatte muskler en meget heterogen (forskellig) gruppe, der kan opdeles i yderligere undergrupper. For eksempel kan man skelne musklerne i de enkelte organsystemer fra hinanden (f.eks. Glatte muskler i blodkarrene, luftvejene osv.) Eller differentiere faseglatte muskler (afslappet i hvile eller rytmisk sammentrukket) fra toniske ( konstant kontrakt).
embryologi
Ligesom skeletmuskelceller, glatte muskelceller er af mesodermal oprindelse undtagen i iris i øjet .
konstruktion
Konstruktion på mobilniveau

Glat muskel består af glatte muskelceller , der har et spindelformet udseende, ca. to til ti mikrometer brede og ca. 20 (i blodkar) til 800 µm (i en gravid kvindes livmoder ) lange. Den aflange cellekerne er placeret i midten, i dens ender er de fleste af celleorganellerne såsom mitokondrier , ribosomer eller det ru endoplasmatiske retikulum .
Hvis glatte muskelceller vises i stort antal, danner de tætte lag, tråde eller gitterlignende systemer afhængigt af organet. Hver celle er omgivet af en membran, basalmembranen . Cellerne er forbundet med hinanden via proteinsystemer uden for cellerne ( ekstracellulær matrix ). Denne forbindelse mellem cellerne sikrer, at hele muskelgruppen kan udøve en kraft. Nogle glatte muskelceller har også små sener, som de fastgør til bindevævet .
I elektronmikroskopbilledet er de langsgående orienterede, parallelle filamenter inde i cellen, kompressionszoner inde i cellen og på cellemembranen og grober ( caveolae ) på cellemembranen synlige. I nogle muskelceller findes der også et system med glatte rør nær disse caveolae; det antages, at begge kan være involveret i muskelcellens sammentrækningsmekanisme.
Struktur på molekylært niveau

På højre side kan du se, hvordan actinfilamenterne (røde) mellem myosinhovederne (grønne) bevæger sig mod hinanden og dermed forkorter muskelen.
I modsætning til de stribede muskler synes cytoplasmaet (inde i cellen) homogent under lysmikroskopet , men der er et stort antal strukturer i glatte muskelceller. To forskellige systemer i kombination er ansvarlige for sammentrækningen af en glat muskelcelle: cytoskeletalsystemet og myofilamenterne.
Cytoskelet
Den cytoskelettet af en celle er en ramme af proteiner inde i cellen, der understøtter det, giver den dens form og udfører andre opgaver. De mellemliggende filamenter nedbrydes, og i tilfælde af vaskulære muskelceller er vimentin og ikke-muskulært actin nødvendigt til sammentrækning af en glat muskelcelle . Disse passerer gennem muskelcellen og spænder fra kompressionszoner inde i cellen, de tætte kroppe , til kompressionszoner på indersiden af cellemembranen, fastgørelsespladerne eller tætte plaques . Disse kompressionszoner indeholder α-actinin og plectin og kan sammenlignes med Z-skiverne i stribede muskler.
Myofilamenter
Myofilamenterne udgør den egentlige mekanisme til sammentrækning ( kontraktile apparater ) og i tilfælde af glatte muskler består de af glat muskulatur α-actin og isoformer af myosin . De er sandsynligvis arrangeret i skrå stier gennem cellen. Actinfilamenterne er forankret i de nævnte tætte legemer og tætte plaketter . Myosinfilamenterne er i kontakt med flere actinfilamenter og kan binde til disse actinfilamenter med deres hovedregion . Det specielle arrangement af actin- og myosinfilamenterne til hinanden gør det muligt for glatte muskelceller at forkorte til en tredjedel af deres oprindelige længde. I stribede muskelceller har actin- og myosinfilamenterne et regelmæssigt arrangement, således at typiske striber vises i det mikroskopiske billede.
Actinfilamenterne i de glatte muskelceller har også kontakt med integriner i området med de tætte plaques , der spænder over cellemembranen og er forbundet med proteiner i den ekstracellulære matrix på ydersiden af cellen. Dette sikrer kontakten mellem muskelcellerne.
sammentrækning
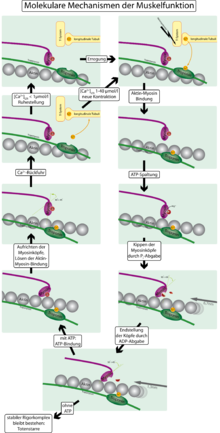
Sammentrækningsmekanismen for de glatte muskler svarer i det væsentlige til muskelkontraktionen af de stribede muskler og fungerer grundlæggende som følger: Hoveddomænet for myosinet, myosinhovedet, er allerede bundet til et actinfilament i hvile. Vinklen mellem hoveddomænet (tung kæde) og den lette kæde er 90 °. Derudover har myosinhovedet bundet ATP . Hvis muskelen nu er trukket sammen, er der en kraftig stigning i Ca 2+ koncentrationen i cellen (fra ca. 10 −7 til 10 −6 til 10 −5 mmol / l). Denne Ca 2+ binder nu til proteinet calmodulin , som igen aktiverer enzymet myosin let kæde kinase ( MLKK ). MLKK fosforylerer myosin let kæde, dvs. H. Phosphat tilsættes til myosins molekylære struktur. Dette giver myosin ATPase- aktiviteten og spalter derfor ATP bundet til hoveddomænet. Dette trin giver den nødvendige energi. Spaltningsprodukterne, nemlig ADP og fosfat, forlader myosinhovedet, og dette foldes over, vinklen mellem den tunge kæde og den lette kæde er nu kun 45 °. Dermed “forskyder” myosinhovedet actinfilamentet lidt: der oprettes en bevægelse. Denne bevægelse kaldes et kraftstreg. De enkelte actinfilamenter blev skubbet mod hinanden, så længden af musklen blev forkortet samlet, dvs. den er trukket sammen.
I det næste trin er det nu nødvendigt at bryde båndet mellem myosinhovedet og actinfilamentet. For at gøre dette bindes et ATP-molekyle igen, bindingen frigøres, en vinkel på 90 ° mellem den tunge og lette kæde indstilles igen, og mekanismen kan starte forfra. Så det er en cyklus, krydsbroen. Denne cyklus gør det muligt at gentage kraftslaget, så musklerne kan forkorte sig maksimalt. I tilfælde af glatte muskelceller er dette maksimum ca. en tredjedel af den oprindelige længde, hvilket er betydeligt længere end i tilfælde af skeletmuskulatur. Imidlertid er sammentrækningen også meget langsommere.
Stigningen i Ca 2+ sammentrækning kan skyldes tre forskellige mekanismer:
- Elektromekanisk kobling:
- Elektromekanisk kobling beskriver den proces, hvorved handlingspotentialer fører til muskelkontraktion. Handlingspotentialer repræsenterer ionstrømme, som er karakteriseret ved omfordeling af visse ioner på cellemembranen og som bevæger sig langs cellemembranen. Spændingen skifter mellem rummet uden for og inde i cellen. Disse handlingspotentialer kan være forårsaget af pacemakerceller eller af nervesites. Under alle omstændigheder fører en sådan spændingsændring til, at spændingsafhængige Ca2 + -kanaler åbner og calcium strømmer ind i cellen udefra, hvilket fører til den ovenfor beskrevne sammentrækning. Sådanne spændingsændringer kan også opstå gennem en langvarig ændring i spænding (depolarisering) på grund af en ændring i ledningsevnen for kaliumioner. Man taler her om den metaboliske sammentrækning .
- Farmakomekanisk kobling:
- I tilfælde af farmakomekanisk kobling fører hormoner, neurotransmittere eller lægemidler til en stigning i Ca2 + koncentrationen og dermed til en sammentrækning. Hormoner og neurotransmittere såsom noradrenalin kan binde sig til receptorer på celleoverfladen og øge aktiviteten af enzymet phospholipase C inde i cellen. Phospholipase C danner inositoltriphosphat (IP 3 ), som igen binder til IP 3- receptoren, som er placeret på det sarkoplasmatiske retikulum (en celleorganel). Dette fører til frigivelse af calcium fra det sarkoplasmatiske retikulum i det indre af cellen og dermed til sammentrækning.
- Derudover kan den farmakomekaniske kobling direkte ændre aktiviteten af MLKK-enzymet (Ca 2+ sensibilisering). For eksempel reguleres sammentrækningen af blodkarrene af aktivatorer af Rho-kinasen i det parasympatiske nervesystem. En stigning i aktiviteten af myosin let kædefosfatase (MLKP) kaldes derimod Ca2 + desensibilisering, da MLKP har den modsatte virkning til MLKK, nemlig dephosphorylerende myosin og dermed forhindrer krydsbroen.
- Mekanisk kobling: strækningsafhængige calciumkanaler kan åbne direkte, når de strækkes, og udløse en tilstrømning af calcium og dermed sammentrækning. Dette kaldes Bayliss-effekten .
Kontraktionsformer
Strukturelle forskelle og de deraf følgende funktionelle forskelle gør det muligt at opdele glat muskelvæv i enkelt-enheder og multi-enhedstyper . Blandede former er v. en. hyppig i de vaskulære muskler .
Enhedstype
Hvis flere muskelceller er forbundet med hinanden af visse proteiner, taler man om muskelvæv af typen med en enkelt enhed. Proteinerne danner en slags kanal mellem cellerne, mellemrumsknuderne ( nexus ), så ioner og messenger-stoffer såsom anden messenger hurtigt kan komme fra en celle til en anden. Dette fører til en elektrisk kobling mellem cellerne: Hvis ionkoncentrationen i en celle ændres (f.eks. Inden for rammerne af et handlingspotentiale), overføres denne ændring direkte til den nærliggende celle, og dette exciteres også. Derfor trækker muskelcellerne af den enkelte enhedstype næsten synkront sammen.
Muskelcellerne i en sådan celleklynge stimuleres af spontant aktive pacemakerceller ( myogen tone ) og forekommer i hule organer såsom livmoderen eller i små blodkar. Imidlertid varierer frekvensen af sådanne forbindelser også inden for organet og ændringer i livmoderen under graviditeten. Aktiviteten af pacemakercellerne kan reguleres af vegetative nerveceller eller hormoner.
Type med flere enheder

Sammentrækninger, der er afhængige af nabocellerne, finder ikke sted eller kun i meget begrænset omfang i multienhedstypen. I stedet er hver muskelcelle innerveret af nervefibre i det vegetative nervesystem eller også reguleret af hormoner. Til dette formål udsender nervecellerne i umiddelbar nærhed sendere fra åreknuder (fortykninger) . Man taler derfor om neurogen tone . Da afstanden mellem varicositeterne og de glatte muskelceller er meget større (ca. 50 til 100 nm) end afstanden i “reelle” synapser, taler man også om “synapses à distance”.
Lempelse
Til afslapning ( afslapning ) opstår ved et fald i Ca 2+ -spejl forårsaget af manglen på nerveimpulser og andre spændende begivenheder. Calcium transporteres fra det indre af cellen tilbage til det ekstracellulære rum eller reticulum ved Na + / Ca 2+ antiportere og Ca 2+ - ATPaser ( SERCA ). Ca2 + -calmodulin-komplekset adskiller sig (nedbrydes), og MLKP dephosphorylerer de lette kæder i myosinmolekylet. Som et resultat, ATPase-aktiviteten af myosinhovederne bukker under, og krydsbroen kan ikke længere fortsætte.
Derudover er den følgende mekanisme til aktiv afslapning kendt: Aktivering af endotel-nitrogenoxidsyntase frigiver messenger-stoffet nitrogenoxid (NO), en gastransmitter, i det tilsvarende vaskulære afsnit. Nitrogenoxid (NO), som er konstitutivt dannet af det vaskulære endotel, kan diffundere ind i de tilstødende glatte muskelceller og aktivere den opløselige guanylatcyclase der . Den fortløbende stigning i cGMP- niveauet fører til en aktivering af proteinkinase G , som aktiverer myosin let kæde-phosphatase (MLKP) ved phosphorylering og dermed fører til lempelse af de glatte muskelceller. Stimuleringen af β-adrenoreceptorerne, fx ved hjælp af adrenalin, fører til en aktivering af MLKP og dermed til en lempelse af muskelcellen via stigningen i cAMP- niveauet og aktivering af proteinkinase A. (se regulering).
regulering
Der er flere mekanismer til regulering af glat muskeltonus, hvoraf to er vist nedenfor:
- Myogen regulering beskriver den spændende indflydelse af pacemakercellerne: glatte muskelceller eller specialiserede fibroblastlignende celler genererer langsomme depolarisationsbølger, der kan føre til handlingspotentialer. Denne proces kan fremmes ved strækning via stræk-afhængige Ca 2 kanaler. Denne type regulering findes i typen med en enhed.
-
Neurogen regulering kræver, at næsten enhver muskelcelle er innerveret . Her finder regulering sted via nerveimpulser fra det autonome nervesystem, som består af det sympatiske og parasympatiske nervesystem . I fordøjelseskanalen er det enteriske nervesystem også involveret:
- Sympatisk: De sympatiske nervecellelegemer er placeret i rygmarven og trækkes til grænsesnorens paravertebrale ganglier eller til prævertebral ganglier, hvor de forbinder via kolinerge synapser til den anden neuron relativt fjernt fra orgelet. Den anden neuron innerverer i sidste ende blandt andet glatte muskler via adrenerge synapser. Effekten afhænger af receptoren: α1-receptoren medierer en sammentrækning af musklerne (fx i blodkar, iris, lukkemusklene i fordøjelseskanalen og urinblæren), mens β2-receptoren har nøjagtig den modsatte effekt: den aktiveres , bronkierne, blodkar i skeletmuskler og hjertet udvides. Det skal bemærkes, at virkningen på β2-receptoren kun i ringe grad forårsages af nervefibre, fordi de tilsvarende muskler kun er meget utilstrækkeligt innerverede. Stimuleringen af catecholaminer, især adrenalin og noradrenalin fra blodbanen, er af meget større fysiologisk relevans. Alle disse effekter af det sympatiske nervesystem på organismen gavner generelt forberedelsen af kroppen til større fysisk anstrengelse ("kamp-eller-flugt").
- Parasympatisk: I stedet for en organ fjernforbindelse mellem præ- og postganglionäres Neuron som i det sympatiske nervesystem er med parasympatisk et relativt organ tæt sammenkobling før: De preganglioniske fibre fra rygmarven eller vagusnerven trækker Cilarganglion , otic ganglion , submandibular ganglion og pterygopalatin ganglion eller ganglier, der er i umiddelbar nærhed af eller endda i selve orgelet. De postganglioniske fibre når derefter de glatte muskelceller via muskarine, kolinerge receptorer. M1-, M3- og M5-receptorer gælder for de glatte muskler og får bronkialmusklerne og andre muskler til at trække sig sammen. I karene forklares effekten via endotelet: Acetylcholin formodes at binde til M3-receptorer på endotelceller, som igen frigiver muskelafslappende stoffer til glatte muskelceller.
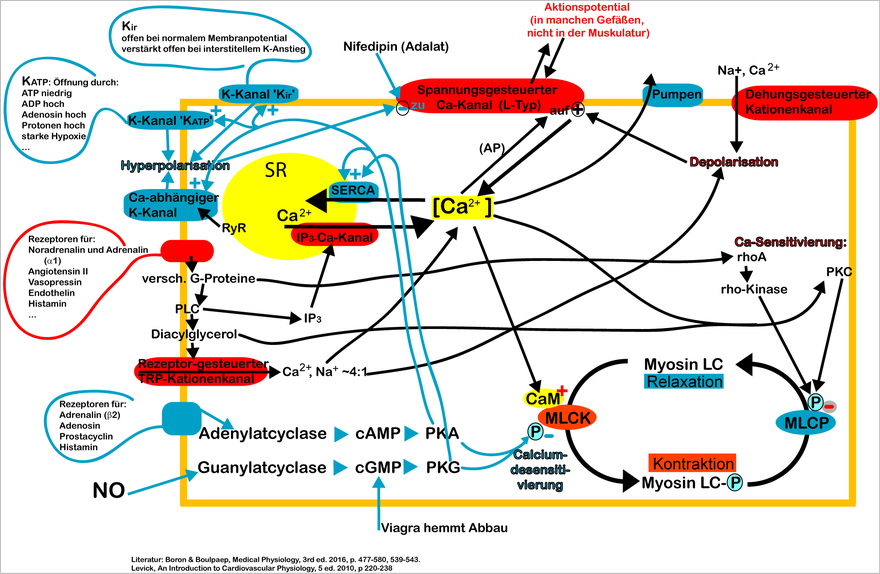
Myosin LC: Myosin let kæde. MLCK: myosin let kæde kinase. MLCP: myosin let kæde phosphatase. CaM: calmodulin. ℗: fosforylering. PLC: phospholipase C. PKA, PKC, PKG: proteinkinase A, C eller G. NO: nitrogenoxid. SR: Sarcoplasmic reticulum. AP: handlingspotentiale.
Ikke vist: Chloride-Kanal, butiksstyret Ca-kanal (TRPC1), Kalikum-Kanal K V , Phospholamban, α2-Receptor og andre.
fungere
Glatte muskler kan opretholde en langvarig tone ( tonisk kontinuerlig sammentrækning ) på grund af deres struktur og de processer, der er beskrevet under sammentrækning . Både peristaltikken i maven , tarmene og urinvejene og reguleringen af blodtrykket i arteriernes indre vægge er baseret på virkningen af glatte muskler. Under fødslen muliggør den rytmisk sammentrækning ( fase-rytmisk sammentrækning ) af livmoderen ( fødsel ).
Matrixproduktion
Glatte muskelceller bruges til at syntetisere kollagen og andre komponenter i den ekstracellulære matrix , såsom B. proteoglycaner , elastin og laminin .
patologi
Neoplasmer i glatte muskelceller kaldes leiomyomer . De findes hovedsageligt i livmoderen og mave-tarmkanalen . Hvis tumoren bliver ondartet, kaldes den leiomyosarkom .
Se også
Individuelle beviser
- ↑ Renate Lüllmann-Rauch: Pocket lærebog histologi . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 238 og 260 .
- ↑ a b c d Renate Lüllmann-Rauch: Pocket lærebog histologi . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 264 .
- ↑ Jan C. Behrends et al:. Dual serier: Physiology . 3. udgave. Thieme, Stuttgart 2016, ISBN 978-3-13-138413-3 , s. 74 og 76 .
- ↑ a b Renate Lüllmann-Rauch: Pocket lærebog histologi . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 260 .
- ^ A b Ernst Mutschler: Anatomi, fysiologi, menneskers patofysiologi. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2007, ISBN 978-3-8047-2342-9 , 6. udgave.
- ↑ a b c Renate Lüllmann-Rauch: histologi til lommebog . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 261 .
- ↑ a b Renate Lüllmann-Rauch: Pocket lærebog histologi . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 262 .
- ↑ Renate Lüllmann-Rauch: Pocket lærebog histologi . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 262 og 263 .
- ↑ a b c d e f g h C. C. Behrends et al.: Dual series: Physiology . 3. udgave. Thieme, Stuttgart 2016, ISBN 978-3-13-138413-3 , s. 76 .
- ↑ a b c Renate Lüllmann-Rauch: histologi til lommebog . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 263 .
- ↑ a b Jan C. Behrends et al.: Dual series: Physiology . 3. udgave. Thieme, Stuttgart 2016, ISBN 978-3-13-138413-3 , s. 75 .
- ↑ a b c d Jan C. Behrends et al.: Dual series: Physiology . 3. udgave. Thieme, Stuttgart 2016, ISBN 978-3-13-138413-3 , s. 74 .
- ↑ Renate Lüllmann-Rauch: Pocket lærebog histologi . 5. udgave. Thieme, Stuttgart 2015, ISBN 978-3-13-129245-2 , s. 264 og 265 .
- ↑ Jan C. Behrends et al:. Dual serier: Physiology . 3. udgave. Thieme, Stuttgart 2016, ISBN 978-3-13-138413-3 , s. 569 .
- ↑ Jan C. Behrends et al:. Dual serier: Physiology . 3. udgave. Thieme, Stuttgart 2016, ISBN 978-3-13-138413-3 , s. 560 til 565 samt 570 og 572 .
- ↑ Jan C. Behrends et al:. Dual serier: Physiology . 3. udgave. Thieme, Stuttgart 2016, ISBN 978-3-13-138413-3 , s. 564, 572 og 573 .